Описание препарата Ксеплион (суспензия для внутримышечного введения пролонгированного действия, 100 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2014 году
Дата согласования: 13.11.2014
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Суспензия для внутримышечного введения пролонгированного действия | 1 мл |
| активное вещество: | |
| палиперидон | 100 мг |
| (эквивалентно 156 мг палиперидона пальмитата) | |
| вспомогательные вещества: полисорбат 20 — 12 мг; макрогол 4000 (полиэтиленгликоль 4000) — 30 мг; лимонной кислоты моногидрат — 5 мг; натрия гидрофосфат — 5 мг; натрия дигидрофосфата моногидрат — 2,5 мг; натрия гидроксид — 2,84 мг; вода для инъекций — до 1 мл |
Описание лекарственной формы
Белая или почти белая суспензия, свободная от посторонних включений.
Фармакологическое действие
Фармакологическое действие
—
нейролептическое.
Фармакодинамика
Механизм действия
Палиперидона пальмитат гидролизуется до палиперидона. Последний является центральнодействующим активным антагонистом преимущественно серотониновых 5-HT2A-рецепторов, а также дофаминовых D2-рецепторов, адренергических α1— и α2-рецепторов и гистаминовых Н1-рецепторов. Палиперидон не связывается с холинергическими м-рецепторами и с адренергическими β1— и β2-рецепторами. Фармакологическая активность (+) и (−) энантиомеров палиперидона количественно и качественно одинакова.
Предполагается, что терапевтическая эффективность препарата при шизофрении обусловлена комбинированной блокадой D2— и 5-HT2A-рецепторов.
Фармакокинетика
Всасывание и распределение
Из-за исключительно низкой растворимости в воде палиперидона пальмитат после в/м введения медленно растворяется и всасывается в системный кровоток. После однократного в/м введения концентрация палиперидона в плазме крови медленно увеличивается, достигая максимума через 13–14 дней (медиана) после введения в дельтовидную мышцу и 13–17 дней после введения в ягодичную мышцу. Высвобождение вещества обнаруживается уже в 1-й день и сохраняется по меньшей мере 126 дней. Характеристики высвобождения активного компонента и схема дозирования препарата Ксеплион обеспечивают длительное поддержание терапевтической концентрации. После однократного введения дозы 25–150 мг в дельтовидную мышцу Cmax в среднем на 28% больше, чем после введения в ягодичную мышцу. В начале терапии введение препарата в дельтовидную мышцу помогает быстрее достичь терапевтической концентрации палиперидона (150 мг в 1-й день и 100 мг на 8-й день), чем введение в ягодичную мышцу. После многократных инъекций разница в воздействии менее очевидна. Среднее отношение Cmax и Css палиперидона после введения 4 инъекций препарата Ксеплион в дозе 100 мг в ягодичную мышцу равнялось 1,8, а после введения в дельтовидную мышцу — 2,2. При дозах палиперидона 25–150 мг AUC палиперидона изменялась пропорционально дозе, а Cmax при дозах более 50 мг увеличивалась в меньшей степени, чем пропорционально дозе.
Медиана T1/2 палиперидона после введения препарата Ксеплион в дозах 25–150 мг колебалась в пределах 25–49 дней.
После введения препарата (−)-энантиомер палиперидона частично превращается в (+)-энантиомер, и отношение AUC (+)- и (−)-энантиомеров составляет примерно 1,6–1,8.
В популяционном анализе кажущийся Vd палиперидона равнялся 391 л; палиперидон связывается с белками плазмы крови на 74%.
Метаболизм и выведение
За неделю после однократного перорального приема 1 мг препарата 14С-палиперидона с немедленным высвобождением активного компонента с мочой в неизмененном виде выводится 59% введенной дозы; это указывает на отсутствие существенного метаболизма препарата в печени. Примерно 80% введенной радиоактивности обнаруживалось в моче и 11% — в кале. Известны 4 пути метаболизма препарата in vivo, но ни один из них не обусловливает метаболизм более чем 6,5% введенной дозы: дезалкилирование, гидроксилирование, дегидрогенизация, отщепление бензизоксазольной группы. Хотя исследования in vitro позволяют предположить определенную роль изоферментов CYP2D6 и CYP3A4 в метаболизме палиперидона, данных о существенной роли этих изоферментов в метаболизме палиперидона in vivo нет. Популяционный фармакокинетический анализ не выявил заметного различия клиренса палиперидона после перорального приема препарата людьми с активным и слабым метаболизмом CYP2D6. Исследования с использованием микросом печени человека in vitro показали, что палиперидон существенно не ингибирует метаболизм ЛС изоферментами CYP1A2, CYP2A6, CYP2D6, CYP2E1, CYP3A4 и CYP3A5.
В исследованиях in vitro палиперидон проявлял свойства субстрата P-гликопротеина, а в высоких концентрациях — свойства слабого ингибитора P-гликопротеина. Соответствующих данных in vivo нет, и клиническая значимость этих сведений неясна.
В целом, концентрация палиперидона в плазме крови в период нагрузки после в/м введения препарата Ксеплион лежала в том же диапазоне, что и после приема палиперидона пролонгированного действия перорально в дозах между 6 и 12 мг. Использованная схема нагрузки палиперидона обеспечивает поддержание концентрации в этом диапазоне даже в конце междозового интервала (8-й и 36-й день). Индивидуальные различия фармакокинетики палиперидона после введения препарата Ксеплион у разных пациентов были меньше, чем после приема палиперидона пролонгированного действия перорально. Из-за различия характера изменения медианы концентрации палиперидона в плазме крови при применении этих препаратов, следует проявлять осторожность при прямом сравнении их фармакокинетики.
Особые категории больных
Нарушение функции печени. Палиперидон не подвергается существенному метаболизму в печени. Хотя применение препарата Ксеплион у больных с нарушением функции печени легкой или средней степени тяжести не изучалось, при таких нарушениях функции печени коррекция дозы не требуется. В исследовании применение палиперидона перорально у больных с нарушением функции печени средней степени тяжести (класс В по Чайлд-Пью) концентрация свободного палиперидона в плазме крови была такой же, как у здоровых добровольцев. У больных с нарушением функции печени тяжелой степени применение палиперидона не изучалось.
Нарушение функции почек. Для больных с нарушением функции почек легкой степени тяжести дозу палиперидона следует уменьшить; Ксеплион не рекомендуется применять у больных с нарушением функции почек средней степени тяжести и тяжелой степени. Было изучено распределение палиперидона после однократного приема внутрь таблетки палиперидона пролонгированного действия 3 мг больными с разной степенью нарушения функций почек. С уменьшением Cl креатинина выведение палиперидона ослаблялось: при нарушении функций почек легкой степени тяжести (Cl креатинина 50–80 мл/мин) — на 32%, при средней степени тяжести (Cl креатинина 30–50 мл/мин) — на 64%, при тяжелой степени (Cl креатинина 10–30 мл/мин) — на 71%, в результате чего AUC0–∞ увеличилась по сравнению со здоровыми добровольцами соответственно в 1,5, 2,6 и 4,8 раза. Исходя из небольшого количества данных о применении препарата Ксеплион у больных с нарушением функции почек легкой степени тяжести и результатов моделирования фармакокинетики, рекомендуемая нагрузочная доза палиперидона для таких больных составляет 75 мг в 1-й и 8-й день; после этого ежемесячно (каждые 4 нед) вводят по 50 мг.
Пожилые больные. Возраст сам по себе не является фактором, требующим коррекции дозы. Однако такая коррекция может потребоваться из-за возрастного уменьшения Cl креатинина.
Раса. Популяционный фармакокинетический анализ результатов исследования палиперидона для приема внутрь не выявил различия фармакокинетики палиперидона после приема препарата людьми разных рас.
Пол. Клинически значимых различий фармакокинетики палиперидона у мужчин и женщин не найдено.
Влияние курения на фармакокинетику препарата. Согласно исследованиям с использованием микросом печени человека in vitro, палиперидон не является субстратом CYP1A2, поэтому курение не должно влиять на фармакокинетику палиперидона. В соответствии с этими данными in vitro, популяционный фармакокинетический анализ не выявил различия фармакокинетики палиперидона у курящих и некурящих людей.
Показания
Лечение шизофрении и профилактика рецидивов шизофрении.
Противопоказания
гиперчувствительность к палиперидону или любому компоненту препарата;
больные с известной гиперчувствительностью к рисперидону (т.к. палиперидон является активным метаболитом рисперидона).
С осторожностью
Ортостатическая гипотензия. Обладая активностью α-адреноблокатора, палиперидон у некоторых больных может вызывать ортостатическую гипотензию. Ксеплион следует с осторожностью применять у больных с сердечно-сосудистыми заболеваниями (например сердечная недостаточность, инфаркт или ишемия миокарда, нарушение сердечной проводимости), нарушениями мозгового кровообращения или состояниями, предрасполагающими к снижению АД (например обезвоживание, уменьшение ОЦК, применение гипотензивных препаратов).
Судороги. Как и другие нейролептики, Ксеплион следует с осторожностью применять у больных, имеющих в анамнезе судороги или другие состояния, при которых может снижаться судорожный порог.
Регуляция температуры тела. С применением нейролептиков связывают ухудшение способности организма снижать температуру тела. Рекомендуется проявлять осторожность при назначении препарата Ксеплион больным, которые могут подвергаться воздействиям, повышающим температуру тела, например сильная физическая нагрузка, высокая температура окружающей среды, воздействие препаратов с активностью м-холинолитиков, а также обезвоживание.
Интервал QT. Как и в случае других нейролептиков, следует проявлять осторожность при назначении препарата Ксеплион больным, имеющим в анамнезе аритмию или врожденное удлинение интервала QT, либо принимающим препараты, удлиняющие интервал QT.
Учитывая действие палиперидона на ЦНС, следует с осторожностью применять Ксеплион в комбинации с другими ЛС, действующими на ЦНС, и алкоголем. Палиперидон может ослаблять эффект леводопы и агонистов дофамина.
Следует проявлять осторожность при назначении препарата Ксеплион пожилым пациентам с деменцией, пациентам с болезнью Паркинсона или деменцией с тельцами Леви (см. «Особые указания»).
Применение при беременности и кормлении грудью
Безопасность применения препарата Ксеплион в/м или палиперидона перорально при беременности у людей не установлена. При применении высоких доз палиперидона перорально наблюдалось небольшое увеличение смертности плодов у животных. Ксеплион при в/м введении не влиял на течение беременности крыс, но высокие дозы его были токсичны для беременных самок. Дозы палиперидона при приеме внутрь и препарата Ксеплион при в/м введении, которые создают концентрации, превышающие максимальные терапевтические дозы у человека соответственно в 20–22 раза и в 6 раз, не влияли на потомство лабораторных животных.
Ксеплион можно применять при беременности только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода. Влияние препарата Ксеплион на схватки и роды у людей неизвестно.
В случае если женщина принимала антипсихотические препараты (включая палиперидон) в III триместре беременности, у новорожденных существует риск возникновения экстрапирамидных расстройств и/или синдрома отмены различной степени тяжести. Эти симптомы могут включать ажитацию, гипертонию, гипотонию, тремор, сонливость, респираторные нарушения и нарушение вскармливания.
В исследованиях применения палиперидона у животных и рисперидона у людей обнаружено выведение палиперидона с грудным молоком. Поэтому женщины, получающие Ксеплион, не должны кормить детей грудью.
Способ применения и дозы
Только для в/м введения.
У больных, никогда не принимавших палиперидон перорально или рисперидон перорально или парентерально, перед началом лечения препаратом Ксеплион рекомендуется в течение 2–7 дней проверить переносимость палиперидона или рисперидона перорально.
Рекомендуется начинать лечение препаратом Ксеплион с дозы 150 мг в 1-й день и 100 мг через 1 нед (обе инъекции в дельтовидную мышцу). Рекомендуется поддерживающая доза 75 мг 1 раз в мес; эффект может наблюдаться от приема бoльших или меньших доз в диапазоне 25–150 мг, в зависимости от индивидуальной переносимости и/или эффективности. После второй дозы последующие поддерживающие инъекции можно проводить в дельтовидную или ягодичную мышцы.
Поддерживающую дозу можно корректировать ежемесячно. При этом следует учитывать длительное высвобождение активного компонента из палиперидона пальмитата, т.к. эффект изменения дозы может полностью проявиться только через несколько месяцев.
Пропуск дозы
Избегание пропуска доз. Вторую нагрузочную дозу палиперидона рекомендуется вводить через 1 нед после первой дозы. Если это невозможно, то ее можно ввести на 2 дня раньше или позже. Аналогично, третью и последующие дозы рекомендуется вводить ежемесячно, но если это невозможно, то инъекцию можно сделать на 7 дней раньше или позже.
Если вторая инъекция препарата Ксеплион не была сделана вовремя (1 нед ± 2 дня), рекомендуется возобновление лечения в зависимости от времени, которое прошло со дня первой инъекции.
Пропуск второй начальной дозы (срок менее 4 нед). Если со дня первой инъекции прошло менее 4 нед, пациенту следует ввести вторую инъекцию в дозе 100 мг в дельтовидную мышцу как можно скорее. Третью инъекцию препарата Ксеплион в дозе 75 мг следует сделать в дельтовидную или ягодичную мышцы через 5 нед после первой инъекции (не учитывая время второй инъекции). В дальнейшем должен соблюдаться ежемесячный курс инъекций в дозе от 25 до 150 мг в дельтовидную или ягодичную мышцы, в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск второй начальной дозы (срок от 4 до 7 нед). Если со дня первой инъекции препарата Ксеплион прошло от 4 до 7 нед лечение возобновляют введением двух инъекций в дозировке 100 мг по следующей схеме: первую инъекцию в дельтовидную мышцу делают как можно скорее; через 1 нед делают вторую инъекцию в дельтовидную мышцу, затем продолжают ежемесячный курс инъекций в дельтовидную или ягодичную мышцы в дозе от 25 до 150 мг, в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск второй начальной дозы (более 7 нед). Если с момента первой инъекции препарата Ксеплион прошло более 7 нед лечение начинают также, как в случае инициации лечения препаратом Ксеплион.
Пропуск поддерживающей дозы (срок от 1 мес до 6 нед). После начала лечения рекомендуется проводить инъекции препарата Ксеплион ежемесячно. Если с момента последней инъекции прошло менее 6 нед, то следует как можно скорее ввести очередную дозу, равную предыдущей. После этого вводить препарат ежемесячно.
Пропуск поддерживающей дозы (срок от 6 нед до 6 мес). Если с момента последней инъекции препарата Ксеплион прошло более 6 нед, рекомендуется следующее:
— для пациентов стабилизированных дозой от 25 мг до 100 мг:
1) делают инъекцию препарата в дельтовидную мышцу как можно скорее в той дозе, на которой прошла стабилизация состояния пациента до пропуска инъекции;
2) следующую инъекцию в дельтовидную мышцу (такая же доза) делают через неделю на 8-й день;
3) далее возобновляют ежемесячный курс инъекций в дельтовидную или ягодичную мышцы в дозе от 25 до 150 мг, в зависимости от индивидуальной переносимости и/или эффективности;
— для пациентов стабилизированных дозой 150 мг:
1) как можно скорее вводят дозу 100 мг в дельтовидную мышцу;
2) через 1 нед вводят еще одну дозу 100 мг (8-й день) в дельтовидную мышцу;
3) далее возобновляют ежемесячный курс инъекций в дельтовидную или ягодичную мышцы в дозе от 25 до 150 мг, в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск поддерживающей дозы (срок >6 мес). Если с момента последней инъекции препарата Ксеплион прошло более 6 мес, то лечение начинают заново, как описано выше — для начала лечения/
Способ введения
Препарат медленно вводят глубоко в мышцу. Инъекции должен проводить только медицинский работник. Всю дозу вводят за один раз; нельзя вводить дозу за несколько инъекций. Нельзя вводить препарат в сосуды или п/к. Следует избегать случайного попадания в кровеносный сосуд. Для этого перед началом введения препарата поршень шприца оттягивают назад для проверки на предмет попадания иглы в крупный кровеносный сосуд. В случае если при этом в шприц поступает кровь, следует извлечь иглу и шприц из мышцы пациента и утилизировать их.
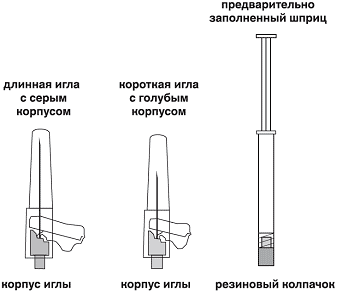
Рекомендуемый размер иглы для ведения препарата Ксеплион в дельтовидную мышцу определяется массой тела пациента. Для больных массой тела ?90 кг рекомендуется длинная игла с серым корпусом из набора. Для больных массой тела <90 кг рекомендуется короткая игла с голубым корпусом из набора. Следует поочередно вводить препарат в правую и левую дельтовидные мышцы.
Для введения препарата Ксеплион в ягодичную мышцу рекомендуется длинная игла с серым корпусом из набора. Инъекции нужно проводить в верхний наружный квадрант ягодицы. Следует поочередно вводить препарат в правую и левую ягодичные мышцы.
Одновременное применение палиперидона пальмитата и палиперидона перорально или рисперидона перорально или парентерально не изучалось. Поскольку палиперидон является основным активным метаболитом рисперидона, то следует учитывать возможность аддитивного действия палиперидона при применении этих препаратов одновременно с препаратом Ксеплион.
Особые группы пациентов
Больные с нарушением функции печени. Применение препарата Ксеплион у больных с нарушением функции печени не изучалось. Исходя из результатов исследования палиперидона для приема внутрь, для больных с нарушением функции печени легкой или средней степени тяжести коррекция дозы не требуется. Применение препарата Ксеплион у больных с нарушением функции печени тяжелой степени не изучалось.
Больные с нарушением функции почек. Применение препарата Ксеплион у больных с нарушением функции почек систематически не изучалось. У больных с нарушением функции почек легкой степени тяжести (Cl креатинина от ?50 до <80 мл/мин), рекомендуется начинать применение препарата Ксеплион с дозы 100 мг в 1-й день и 75 мг через 1 нед (обе инъекции в дельтовидную мышцу). После этого через 1 мес вводят инъекцию в дозе 50 мг в дельтовидную или ягодичную мышцы и далее изменяют дозу от 25 до 100 мг, в зависимости от индивидуальной переносимости и/или эффективности.
Ксеплион не рекомендуется применять у больных с нарушением функции почек средней или тяжелой степени (Cl креатинина <50 мл/мин).
Пожилые больные. В целом, для пожилых больных с нормальной функцией почек рекомендуется та же доза препарата Ксеплион, что и для более молодых больных с нормальной функцией почек. У пожилых больных функция почек может быть снижена, и на таких больных распространяются приведенные выше рекомендации для больных с нарушением функции почек.
Подростки и дети. Безопасность и эффективность применения препарата Ксеплион у больных моложе 18 лет не изучалась.
Другие особые категории больных. Коррекция дозы препарата Ксеплион в зависимости от пола, расы больных и курения не требуется.
Перевод с других нейролептиков
Данные о переводе больных шизофренией с других нейролептиков на Ксеплион или его применении одновременно с другими нейролептиками систематически не собирались. Для пациентов, которые никогда не принимали пероральный палиперидон или пероральный или инъекционный рисперидон, должна быть исследована переносимость с пероральным палиперидоном или пероральным рисперидоном перед началом лечения препаратом Ксеплион. В начале лечения препаратом Ксеплион ранее применявшиеся перорально нейролептики можно отменить. Ксеплион следует назначать, как описано выше. Если пациент получает инъекционные нейролептики пролонгированного действия, лечение препаратом Ксеплион начинают сразу с поддерживающей дозы в момент очередной запланированной инъекции. Следует продолжать лечение препаратом Ксеплион 1 раз в мес. Начальная доза на первой неделе лечения не требуется.
У пациентов, которые были стабилизированы различными дозами препарата Рисполепт Конста®, суспензия для в/м введения пролонгированного действия, Css активного вещества могут достигать схожих значений в течение поддерживающей терапии препаратом Ксеплион 1 раз в мес согласно схеме, указанной в таблице.
Таблица
| Последняя доза (Рисполепт Конста®) | Начальная доза (Ксеплион) |
| 25 мг каждые 2 недели | 50 мг 1 раз в месяц |
| 37,5 мг каждые 2 недели | 75 мг 1 раз в месяц |
| 50 мг каждые 2 недели | 100 мг 1 раз в месяц |
Отмену предыдущего антипсихотика следует провести в соответствии с инструкцией по медицинскому применению. При отмене препарата Ксеплион следует учитывать длительное высвобождение активного компонента. Как и в случае с другими нейролептиками, следует периодически оценивать необходимость продолжения применения средств профилактики развития экстрапирамидных расстройств.
Состав комплекта препарата
В комплект препарата входят: предварительно заполненный шприц с препаратом, 2 иглы для в/м инъекций (в дельтовидную и ягодичную мышцы) — длинная игла с серым корпусом и короткая игла с голубым корпусом.
Указания по применению комплекта препарата
Шприц предназначен только для однократного введения.
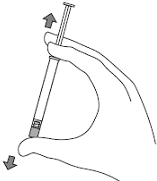
1. Интенсивно встряхнуть шприц в течение 10 с для получения однородной суспензии.
2. Выбрать соответствующую иглу.
Для введения в дельтовидную мышцу больным массой тела <90 кг использовать короткую иглу (с голубым корпусом), а больным массой тела ?90 кг — длинную иглу (с серым корпусом).
Для введения в ягодичную мышцу использовать длинную иглу (с серым корпусом).
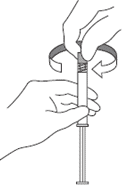
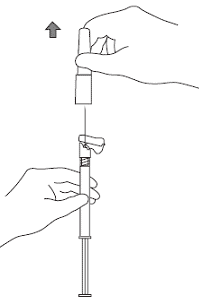
3. Держа шприц вертикально, снять с него резиновый колпачок путем аккуратного вращения по часовой стрелке.
4. Наполовину открыть упаковку безопасной иглы, взяться за колпачок иглы через упаковку и вставить шприц в люэровский колпачок иглы путем аккуратного вращения по часовой стрелке.
5. Снять с иглы колпачок, потянув его вдоль иглы. Не следует вращать колпачок, т.к. это может ослабить соединение иглы со шприцем.
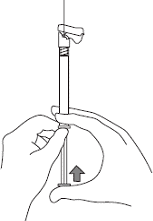
6. Направить шприц иглой вверх и выдавить из шприца воздух, слегка надавив на поршень.
7. Ввести все содержимое шприца в выбранную мышцу (дельтовидную или ягодичную). Не вводить препарат в кровеносный сосуд или п/к.
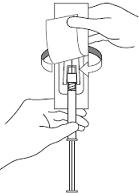
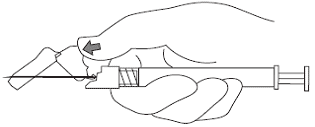
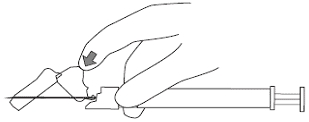
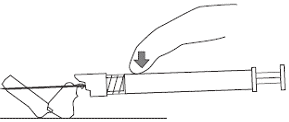
8. После завершения инъекции привести защиту иглы в рабочее положение большим (см. рис. 7) или указательным (см. рис. 
Побочные действия
Большинство нежелательных побочных реакций были слабыми или средней тяжести.
Ниже указаны нежелательные реакции, наблюдавшиеся у пациентов. Частоту нежелательных реакций классифицировали следующим образом: очень часто (≥10%); часто (≥1% и <10%); нечасто (≥0,1% и <1%); редко (≥0,01% и <0,1%) и очень редко (<0,01%).
Инфекции: часто — инфекции верхних дыхательных путей; нечасто — акродерматит, бронхит, воспаление подкожной жировой клетчатки, инфекции уха, инфекции глаза, грипп, онихомикоз, пневмония, инфекции дыхательных путей, синусит, подкожный абсцесс, тонзиллит, инфекции мочевыделительной системы.
Со стороны иммунной системы: нечасто — гиперчувствительность.
Со стороны кровеносной и лимфатической системы: нечасто — нейтропения, уменьшение количества белых кровяных клеток; редко — тромбоцитопения; очень редко — агранулоцитоз.
Со стороны эндокринной системы: редко — неадекватная секреция АДГ.
Метаболические нарушения: часто — повышение массы тела; нечасто — анорексия, гипергликемия, снижение аппетита, повышение аппетита, снижение массы тела, полидипсия, сахарный диабет; редко — гипогликемия; очень редко — диабетический кетоацидоз, водная интоксикация.
Психические расстройства: очень часто — бессонница, возбуждение; часто — ночные кошмары, беспокойство; нечасто — депрессия, нарушение сна, мании.
Со стороны нервной системы: очень часто — головная боль; часто — акатизия, головокружение, экстрапирамидные симптомы, сонливость, паркинсонизм (в т.ч. акинезия, брадикинезия, ригидность по типу зубчатого колеса, слюнотечение, экстрапирамидные симптомы, отклонение глабеллярного рефлекса, мышечная ригидность, скованность в мышцах, скелетно-мышечная неподвижность); нечасто — нарушение координации, цереброваскулярные нарушения, судороги (в т.ч. эпилептические судороги), рассеянность внимания, постуральное головокружение, дизартрия, дискинезия (в т.ч. атетоз, хорея, хореоатетоз, нарушение движения, мышечные сокращения, клонические судороги), дистония (в т.ч. блефароспазм, спазм шеи, эмпростотонус, спазм лица, ларингоспазм, непроизвольные мышечные сокращения, миотония, движения глазного яблока, опистотонус, орофарингеальный спазм, плеврототонус, сардоническая улыбка, тетания, паралич языка, спазм языка, кривошея, судорожное стискивание челюстей), гипестезия, парестезия, психомоторная гиперактивность, обморок, тяжелая дискинезия, тремор.
Офтальмологические нарушения: нечасто — сухость глаз, увеличение слезотечения, окулярная гиперемия, непроизвольное движение глазного яблока, нечеткость зрительного восприятия.
Со стороны органа слуха и равновесия: нечасто — вертиго, боль в ухе.
Со стороны ССС: часто — повышение АД; нечасто — AV блокада, брадикардия, нарушение проводимости, нарушения на ЭКГ, увеличение интервала QT на ЭКГ, сердцебиение, синдром постуральной ортостатической тахикардии, синусовая аритмия, тахикардия, фибрилляция предсердий, ортостатическая гипотензия; редко — тромбоз глубоких вен; очень редко — эмболия легочной артерии.
Со стороны дыхательной системы: нечасто — кашель, диспноэ, носовое кровотечение, заложенность носа, боль в глоточно-гортанной области, заложенность дыхательных путей, свистящее дыхание, заложенность легких; очень редко — синдром апноэ во сне.
Желудочно-кишечные нарушения: часто — боль в верхней части живота, запор, диарея, сухость слизистой оболочки полости рта, тошнота, зубная боль, рвота, дискомфорт в области живота; нечасто — диспепсия, дисфагия, недержание кала, метеоризм, гастроэнтерит, отек языка, дисгевзия; редко — панкреатит.
Со стороны гепатобилиарной системы: очень редко — желтуха.
Со стороны костно-мышечной системы и соединительной ткани: часто — боль в конечностях, скелетно-мышечная боль; нечасто — артралгия, боль в спине, скованность суставов, опухание суставов, мышечные спазмы, боль в шее.
Со стороны кожи: нечасто — акне, сухость кожи, экзема, эритема, гиперкератоз, крапивница, зуд, сыпь, алопеция; редко — ангиоэдема.
Со стороны мочевыделительной системы: нечасто — дизурия, поллакиурия, недержание мочи; редко — задержка мочевыведения.
Со стороны репродуктивной системы и молочных желез: нечасто — аменорея, галакторея, гинекомастия, сексуальная дисфункция, нарушения эякуляции, эректильная дисфункция, вагинальные выделения; очень редко — приапизм.
Влияние на течение беременности, послеродовые и перинатальные состояния: очень редко — синдром отмены у новорожденных.
Прочие: часто — астенические расстройства, слабость, местные реакции (боль, зуд, уплотнение в месте инъекции); нечасто — дискомфорт в области груди, озноб, отек лица, нарушение походки, уплотнение в месте укола, отек (в т.ч. генерализованный отек, периферический отек, мягкий отек), жажда, повышенная температура тела; редко — гипотермия, абсцесс в месте введения инъекции, воспаление подкожной клетчатки в месте введения инъекции, гематома в месте введения инъекции; очень редко — киста в месте введения инъекции, некроз в месте введения инъекции, язва в месте введения инъекции.
Изменения лабораторных показателей: нечасто — увеличение активности ГГТ, ферментов печени, трансаминаз, концентрации холестерина в крови, концентрации триглицеридов в крови, гипергликемия.
Взаимодействие
Палиперидон может увеличивать интервал QT, поэтому его следует с осторожностью сочетать с другими ЛС, увеличивающими интервал QT: антиаритмические ЛС, в т.ч. хинидин, прокаинамид, амиодарон, соталол; антипсихотические ЛС (хлорпромазин, тиоридазин), антибиотики, в т.ч. гатифлоксацин, моксифлоксацин.
Поскольку палиперидона пальмитат гидролизуется до палиперидона, то при оценке возможности лекарственного взаимодействия следует учитывать результаты исследований палиперидона для приема внутрь.
Способность препарата Ксеплион влиять на другие препараты
Не ожидается, что палиперидон будет проявлять клинически значимое фармакокинетическое взаимодействие с препаратами, метаболизируемыми изоферментами системы цитохрома Р450. Исследования с использованием микросом печени человека in vitro показали, что палиперидон существенно не ослабляет метаболизм веществ изоферментами CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4 и CYP3A5. Поэтому не ожидается, что палиперидон будет клинически значимо уменьшать клиренс препаратов, метаболизируемых этими изоферментами. Также не ожидается, что палиперидон будет проявлять свойства индуктора изоферментов, т.к. в исследованиях in vitro палиперидон не индуцировал активность изоферментов CYPA2, CYPC19 или CYP3A4.
Палиперидон в высоких концентрациях является слабым ингибитором Р-гликопротеина. Однако данных in vivo в этом отношении нет, и клиническая значимость этого явления не известна.
Учитывая действие палиперидона на ЦНС, следует с осторожностью применять Ксеплион в комбинации с другими ЛС центрального действия и алкоголем.
Палиперидон может ослаблять эффект леводопы и агонистов дофаминовых рецепторов.
Из-за способности препарата Ксеплион вызывать ортостатическую гипотензию может наблюдаться аддитивное усиление этого эффекта при применении препарата Ксеплион совместно с другими препаратами, обладающими такой способностью.
Одновременный прием перорального палиперидона в дозировке 12 мг 1 раз в день и таблеток натрия дивалпроекса пролонгированного действия в дозировке 500–2000 мг 1 раз в день не влияет на фармакокинетику вальпроата.
Фармакокинетическое взаимодействие между препаратом Ксеплион и литием маловероятно.
Способность других препаратов влиять на Ксеплион
Палиперидон не является субстратом изоферментов CYP1A2, CYP2A6, CYP2C9, CYP2C19 и CYP3A5. Это позволяет предположить слабую вероятность взаимодействия с ингибиторами и индукторами этих изоферментов. Хотя исследования in vitro показывают возможность минимального участия CYP2D6 и CYP3A4 в метаболизме палиперидона, в настоящее время нет данных о том, что эти ферменты могут играть существенную роль в метаболизме палиперидона in vitro или in vivo. Исследования in vitro свидетельствуют о том, что палиперидон является субстратом P-гликопротеина.
Палиперидон в ограниченной степени метаболизируется изоферментом CYP2D6. В исследовании взаимодействия палиперидона для приема внутрь с активным ингибитором CYP2D6 пароксетином у здоровых добровольцев не обнаружено клинически значимого изменения фармакокинетики палиперидона.
Прием палиперидона с длительным высвобождением активного компонента (1 раз в день) перорально одновременно с карбамазепином (200 мг 2 раза в день) приводил к снижению средней Cmax и AUC палиперидона примерно на 37%. Это снижение в значительной степени обусловлено увеличением почечного клиренса палиперидона на 35%, вероятно, за счет активации почечного P-гликопротеина карбамазепином. При начале применения карбамазепина дозу препарата Ксеплион следует пересмотреть и, при необходимости, увеличить. Наоборот, при отмене карбамазепина дозу препарата Ксеплион следует пересмотреть и, при необходимости, уменьшить.
Палиперидон при физиологических значениях рН является катионом и в основном выводится в неизмененном виде через почки — половина путем фильтрации, а половина — путем активной секреции. Одновременное применение триметоприма, который ингибирует систему активного транспорта катионов в почках, не влияло на фармакокинетику палиперидона.
При одновременном назначении перорального палиперидона пролонгированного действия в дозировке 12 мг 1 раз в день и таблеток пролонгированного действия натрия дивалпроекса 2 табл. по 500 мг 1 раз в день наблюдалось увеличение Cmax и AUC палиперидона на 50%, вероятно в результате увеличения абсорбции препарата при пероральном приеме. Поскольку не наблюдалось значительного влияния на общий клиренс, не ожидается клинически значимого взаимодействия между дивалпроексом натрия, таблетки длительного высвобождения, и препаратом Ксеплион. Следует рассмотреть возможность уменьшения дозы препарата Ксеплион при одновременном назначении с вальпроатом на основании клинической оценки пациента. Исследований взаимодействия с препаратом Ксеплион не проводилось.
Фармакокинетическое взаимодействие лития и палиперидона маловероятно.
Применение препарата Ксеплион совместно с рисперидоном
Применение препарата Ксеплион совместно с рисперидоном не изучалось. Поскольку палиперидон является активным метаболитом рисперидона, то при одновременном применении препарата Ксеплион и рисперидона следует учитывать повышение концентрации палиперидона в плазме крови.
Передозировка
Поскольку Ксеплион предназначен для введения медработниками, то вероятность его передозировки мала.
Симптомы: в целом, ожидаемые признаки и симптомы соответствуют усилению известного фармакологического действия палиперидона, т.е. сонливость, заторможенность, тахикардия, снижение АД, удлинение интервала QT, экстрапирамидные симптомы. Полиформная желудочковая тахикардия типа «пируэт» и фибрилляция желудочков были отмечены при передозировке перорального палиперидона. В случае острой передозировки следует учитывать возможность получения пациентами нескольких препаратов.
Лечение: при оценке потребности в лечении и восстановлении больных следует учитывать длительное высвобождение активного вещества и большой T1/2 палиперидона. Специфического антидота для палиперидона не существует. Следует осуществлять общие поддерживающие меры, обеспечить и поддерживать проходимость дыхательных путей, достаточную вентиляцию легких и насыщение крови кислородом. Следует немедленно начать контроль функции ССС, включая постоянный мониторинг ЭКГ для выявления возможной аритмии. В случае снижения АД крови и циркуляторного коллапса следует предпринимать соответствующие меры, например в/в введение растворов и/или симпатомиметиков. При развитии тяжелых экстрапирамидных симптомов применяют антихолинергические препараты. Следует тщательно контролировать состояние больного до его восстановления.
Особые указания
Злокачественный нейролептический синдром
При применении нейролептиков, в т.ч. палиперидона, зарегистрировано развитие злокачественного нейролептического синдрома (ЗНС), характеризуемого гипертермией, мышечной ригидностью, нестабильностью вегетативной нервной системы, нарушением сознания и повышением концентрации креатинфосфокиназы сыворотки крови. Кроме того, могут наблюдаться миоглобинурия (рабдомиолиз) и острая почечная недостаточность. При появлении симптомов, позволяющих предположить ЗНС, все нейролептики, включая Ксеплион, отменяют.
Поздняя дискинезия
Применение препаратов, обладающих свойствами антагонистов дофаминовых рецепторов, сопровождается развитием поздней дискинезии, характеризующейся ритмичными, непроизвольными движениями, главным образом языка и/или лицевых мышц. При появлении симптомов поздней дискинезии следует рассмотреть возможность отмены всех нейролептиков, включая Ксеплион.
Гипергликемия и сахарный диабет
При лечении препаратом Ксеплион наблюдались гипергликемия, сахарный диабет и обострение уже имеющегося сахарного диабета. Установление взаимосвязи между применением атипичных антипсихотических препаратов и нарушением обмена глюкозы осложнено повышенным риском развития сахарного диабета у пациентов с шизофренией и распространенностью сахарного диабета в общей популяции. Учитывая эти факторы, взаимосвязь между применением атипичных антипсихотических препаратов и развитием побочных действий, связанных с гипергликемией, установлена не полностью. У всех пациентов необходимо проводить клинический контроль на наличие симптомов гипергликемии и сахарного диабета (см. «Побочные действия»).
Увеличение массы тела
При лечении атипичными антипсихотиками наблюдалось значительное увеличение массы тела. Необходимо проводить контроль массы тела пациентов.
Пожилые больные с деменцией
Перекрестный анализ результатов исследований показал повышенную смертность пожилых больных с деменцией, получавших атипичные нейролептики, в т.ч. рисперидон, арипипразол, оланзапин и кветиапин, по сравнению с плацебо. Среди больных, получавших рисперидон и плацебо, смертность составляла соответственно 4 и 3,1%.
Применение препарата Ксеплион у пожилых больных с деменцией не изучалось. Поскольку палиперидон является активным метаболитом рисперидона, то следует учитывать опыт применения рисперидона. Для пожилых пациентов с деменцией, принимающих рисперидон, наблюдалась повышенная смертность у пациентов, принимавших фуросемид и рисперидон по сравнению с группой, принимавшей только рисперидон и группой, принимавшей только фуросемид. Не установлено патофизиологических механизмов, объясняющих данное наблюдение. Тем не менее, следует соблюдать особую осторожность при назначении препарата в таких случаях. Не обнаружено увеличения смертности у пациентов, одновременно принимающих другие диуретики вместе с рисперидоном. Независимо от лечения, дегидратация является общим фактором риска смертности и должна тщательно контролироваться у пожилых пациентов с деменцией.
Нарушения мозгового кровообращения
В плацебо-контролируемых исследованиях обнаружена повышенная частота нарушений мозгового кровообращения (преходящих и инсульта), в т.ч. со смертельным исходом, у пожилых больных с деменцией, получавших некоторые атипичные нейролептики, в т.ч. рисперидон, арипипразол и оланзапин, по сравнению с применением плацебо.
Лейкопения, нейтропения, агранулоцитоз
Лейкопения, нейтропения и агранулоцитоз отмечались при применении антипсихотических средств, в т.ч. при применении препарата Ксеплион. Агранулоцитоз отмечался очень редко в течение постмаркетинговых наблюдений. Пациентам с клинически значимым уменьшением количества лейкоцитов в анамнезе или препаратзависимой лейкопенией/нейтропенией рекомендуется проведение полного анализа крови в течение первых месяцев терапии; прекращение лечения препаратом Ксеплион должно быть рассмотрено при первом клинически значимом уменьшении количества лейкоцитов при отсутствии других возможных причин. Пациентам с клинически значимой нейтропенией рекомендуется наблюдаться на предмет повышения температуры или возникновения симптомов инфекции и начинать лечение немедленно при возникновении таких симптомов. Пациенты с тяжелой формой нейтропении (абсолютное количество нейтрофилов менее 1·109/л) должны прекратить применение препарата Ксеплион до тех пор, пока количество лейкоцитов не нормализуется.
Венозный тромбоэмболизм
При применении антипсихотических препаратов были отмечены случаи венозной тромбоэмболии. Поскольку пациенты, принимающие антипсихотические препараты, часто имеют риск развития венозной тромбоэмболии, все возможные факторы риска должны быть выявлены до и во время лечения препаратом Ксеплион и должны быть предприняты предупреждающие меры.
Болезнь Паркинсона и деменция с тельцами Леви
Врач должен сопоставить риск и пользу применения нейролептиков, включая Ксеплион, у больных с болезнью Паркинсона или деменцией с тельцами Леви, т.к. у обеих этих категорий больных может быть повышен риск развития ЗНС и риск повышенной чувствительности к нейролептикам. Проявления повышенной чувствительности могут включать спутанность сознания, притупление болевой чувствительности, неустойчивость позы с частыми падениями, а также экстрапирамидные симптомы.
Приапизм
Имеются данные о способности препаратов, обладающих свойствами α-адреноблокаторов, вызывать приапизм. Приапизм зарегистрирован в рамках постмаркетингового контроля применения палиперидона.
Противорвотное действие
В доклинических исследованиях палиперидона обнаружено противорвотное действие. Появление этого эффекта у пациента может маскировать признаки и симптомы передозировки некоторых лекарств или, например, такие состояния, как непроходимость кишечника, синдром Рейе или опухоль мозга.
Введение
При в/м введении следует проявлять осторожность во избежание случайного попадания препарата в кровеносный сосуд.
Влияние на способность управлять автомобилем или выполнять работы, требующие повышенной скорости физических и психических реакций. Ксеплион может нарушать выполнение действий, требующих концентрации внимания и быстроты психомоторных реакций, и может влиять на зрение. Поэтому больным следует рекомендовать не управлять транспортными средствами и движущимися механизмами, пока не будет установлена их индивидуальная чувствительность.
Форма выпуска
Суспензия для внутримышечного введения пролонгированного действия, 100 мг/1 мл. По 0,25, 0,5, 0,75, 1 или 1,5 мл препарата в шприце из циклолефинового сополимера. В комплект препарата входят 2 иглы для в/м инъекций (в дельтовидную и ягодичную мышцы). Предварительно заполненный шприц с препаратом и 2 иглы в пластиковом поддоне, закрытом ПЭ пленкой, помещают в картонную пачку.
Производитель
Производство, упаковка и выпускающий контроль: Янссен Фармацевтика Н.В., Беерсе, Турнхоутсевег, 30, В-2340, Бельгия.
Держатель регистрационного удостоверения: ООО «Джонсон & Джонсон», Россия.
121614, Москва, ул. Крылатская, 17/2.
Тел.: (495) 755-83-57; факс: (495) 755-83-58.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Rec.INN
зарегистрированное ВОЗ
Лекарственное взаимодействие
Входит в состав препаратов:
список
Фармакологическое действие
Антипсихотическое средство (нейролептик) центрального действия. Активный антагонист преимущественно серотониновых 5-НТ2A-рецепторов, а также допаминовых D2-рецепторов, α1— и α2— адренорецепторов и гистаминовых Н1-рецепторов. Палиперидон не связывается с м-холинорецепторами и с β1— и β2— адренорецепторами.
Фармакологическая активность (+)- и (-)-энантиомеров палиперидона количественно и качественно одинакова.
Предполагается, что терапевтическая эффективность при шизофрении обусловлена комбинированной блокадой допаминовых D2— и серотониновых 5-НТ2A-рецепторов.
Фармакокинетика
Из-за исключительно низкой растворимости в воде палиперидона пальмитат после в/м введения медленно растворяется и всасывается в системный кровоток. После однократного в/м введения концентрация палиперидона в плазме крови медленно увеличивается, достигая Cmax через 13-14 сут (медиана) после введения в дельтовидную мышцу и 13-17 сут после введения в ягодичную мышцу. Высвобождение вещества обнаруживается уже в 1-й день и сохраняется, по меньшей мере, 126 дней. Характеристики высвобождения активного вещества и схема дозирования препарата Ксеплион обеспечивают длительное поддержание терапевтической концентрации. После однократного введения в дозе 25-150 мг в дельтовидную мышцу Cmax в среднем на 28% больше, чем после введения в ягодичную мышцу. В начале терапии введение препарата в дельтовидную мышцу помогает быстрее достичь терапевтической концентрации палиперидона (150 мг в 1-й день и 100 мг на 8-й день), чем введение в ягодичную мышцу. После многократных инъекций разница в воздействии менее очевидна. Среднее отношение Cmax и Css палиперидона после введения 4 инъекций препарата Ксеплион в дозе 100 мг в ягодичную мышцу равнялось 1.8, а после введения в дельтовидную мышцу — 2.2. При дозах палиперидона 25-150 мг AUC палиперидона изменялась пропорционально дозе, а Cmax при дозах более 50 мг увеличивалась в меньшей степени, чем пропорционально дозе.
После введения препарата (-)-энантиомер палиперидона частично превращается в (+)-энантиомер, отношение AUC (+)- и (-)-энантиомеров составляет примерно 1.6-1.8.
В целом, концентрация палиперидона в плазме крови в период нагрузки после в/м введения препарата Ксеплион лежала в том же диапазоне, что и после приема палиперидона пролонгированного действия перорально с высвобождением активного компонента в дозах между 6 и 12 мг. Использованная схема нагрузки палиперидона обеспечивает поддержание концентрации в этом диапазоне даже в конце интервала между применением (8-й и 36-й дни).
Распределение
В популяционном анализе кажущийся Vd палиперидона равнялся 391 л.
Связывание палиперидона с белками плазмы составляет 74%.
Метаболизм и выведение
Медиана T1/2 палиперидона после введения препарата Ксеплион в дозах 25-150 мг колебалась в пределах 25-49 дней.
После однократного перорального приема 1 мг препарата 14C-палиперидона с немедленным высвобождением активного вещества за неделю с мочой в неизмененном виде выводится 59% введенной дозы; это указывает на отсутствие существенного метаболизма препарата в печени. Примерно 80% введенной радиоактивности обнаруживалось в моче и 11% — в кале. Известны 4 пути метаболизма препарата in vivo, но ни один из них не обуславливает метаболизм более, чем на 6.5% введенной дозы: дезалкилирование, гидроксилирование, дегидрогенизация, отщепление бензизоксазольной группы. Хотя исследования in vitro позволяют предположить определенную роль изоферментов CYP2D6 и CYP3A4 в метаболизме палиперидона, данных о существенной роли этих изоферментов в метаболизме палиперидона in vivo нет. Популяционный фармакокинетический анализ не выявил заметного различия клиренса палиперидона после перорального приема препарата людьми с активным и слабым метаболизмом CYP2D6. Исследования с использованием микросом печени человека in vitro показали, что палиперидон существенно не ингибирует метаболизм лекарственных средств изоферментами CYP1A2, CYP2A6, CYP2D6, CYP2E1, CYP3A4 и CYP3A5.
В исследованиях in vitro палиперидон проявлял свойства субстрата Р-гликопротеина, а в высоких концентрациях — свойства слабого ингибитора Р-гликопротеина. Соответствующих данных in vivo нет, и клиническая значимость этих сведений неясна.
Фармакокинетика в особых клинических случаях
Палиперидон не подвергается существенному метаболизму в печени. Хотя применение препарата Ксеплион у пациентов с нарушением функции печени легкой или средней степени тяжести не изучалось, при таких нарушениях функции печени коррекция дозы не требуется. В исследовании применение палиперидона перорально у пациентов с нарушением функции печени средней степени тяжести (класс В по шкале Чайлд-Пью) концентрация свободного палиперидона в плазме крови была такой же, как у здоровых добровольцев. У больных с нарушением функции печени тяжелой степени применение палиперидона не изучалось.
Для пациентов с нарушением функции почек легкой степени тяжести дозу палиперидона следует уменьшить; Ксеплион не рекомендуется применять у пациентов с нарушением функции почек средней степени тяжести и тяжелой степени. Было изучено распределение палиперидона после однократного приема внутрь таблетки палиперидона пролонгированного действия 3 мг больными с разной степенью нарушения функций почек. С уменьшением КК выведение палиперидона ослаблялось: при нарушении функций почек легкой степени тяжести (КК 50-80 мл/мин) — на 32%, при средней степени тяжести (КК 30-50 мл/мин) — на 64%, при тяжелой степени (КК 10-30 мл/мин) — на 71%, в результате этого AUC0-∞ увеличилась по сравнению со здоровыми добровольцами соответственно в 1.5, 2.6 и 4.8 раза. Исходя из небольшого количества данных о применении препарата Ксеплион у пациентов с нарушением функции почек легкой степени тяжести и из результатов моделирования фармакокинетики, рекомендуемая нагрузочная доза палиперидона для таких пациентов составляет 75 мг в 1-й и 8-й дни; после этого ежемесячно (каждые 4 недели) вводят по 50 мг.
Пациентам пожилого возраста коррекция дозы не требуется. Однако такая коррекция может быть необходимой из-за возрастного уменьшения КК.
Популяционный фармакокинетический анализ результатов исследования палиперидона для приема внутрь не выявил различия фармакокинетики палиперидона после приема препарата людьми разных рас.
Клинически значимых различий фармакокинетики палиперидона у мужчин и женщин не обнаружено.
Согласно исследованиям с использованием микросом печени человека in vitro, палиперидон не является субстратом CYP1A2, поэтому курение не должно влиять на фармакокинетику палиперидона. В соответствии с этими данными, популяционный фармакокинетический анализ не выявил различия фармакокинетики палиперидона у курящих и не курящих людей.
Показания активного вещества
ПАЛИПЕРИДОН
Лечение шизофрении; профилактика рецидивов шизофрении.
Режим дозирования
Для в/м введения: начальная доза — 150 мг в 1-й день и 100 мг через 1 неделю (обе инъекции в дельтовидную мышцу). В дальнейшем рекомендуется доза 75 мг ежемесячно. Доза может быть увеличена или уменьшена в диапазоне 25-150 мг в зависимости от индивидуальной переносимости и/или эффективности. После второй дозы последующие инъекции можно проводить в дельтовидную или ягодичную мышцу.
Для приема внутрь: рекомендуемая доза составляет 6 мг 1 раз/сут. Постепенное повышение начальной дозы не требуется. У некоторых пациентов терапевтический эффект вызывают более низкие или более высокие дозы в пределах рекомендуемого диапазона 3-12 мг 1 раз/сут. В случае необходимости увеличения дозы рекомендуется повышать дозу на 3 мг/сут с интервалами более 5 сут.
Пациентам с нарушением функции почек требуется коррекция режима дозирования.
Побочное действие
Инфекции: часто — инфекции верхних дыхательных путей.
Со стороны обмена веществ: нечасто — снижение аппетита, повышение аппетита.
Со стороны психики: очень часто — бессонница; часто — возбуждение, кошмарные сновидения; нечасто — беспокойство.
Со стороны нервной системы: очень часто — головная боль; часто — акатизия, головокружение, экстрапирамидные симптомы, сонливость; нечасто — судороги, постуральное головокружение, слюнотечение, дизартрия, дискинезия, дистония, ЗНС, летаргия, оромандибулярная дистония, паркинсонизм, психомоторная гиперреактивность, обморок; при приеме внутрь — большие и малые судорожные припадки, тремор.
Со стороны органов чувств: нечасто — окулогирный криз, непроизвольное движение глазного яблока, нечеткость зрительного восприятия, вертиго.
Со стороны сердечно-сосудистой системы: часто — повышение АД; нечасто — брадикардия, блокада ножек пучка Гиса, синдром постуральной ортостатической тахикардии, тахикардия, ортостатическая гипотензия; при приеме внутрь — AV-блокада I степени, ощущение сердцебиения, синусовая аритмия, синусовая тахикардия, снижение АД, ишемия миокарда, изменения на ЭКГ.
Со стороны пищеварительной системы: часто — боль в верхней части живота, запор, диарея, сухость слизистой оболочки полости рта, тошнота, зубная боль, рвота; нечасто — дискомфорт в животе, гиперсекреция слюны, дискомфорт в желудке.
Со стороны костно-мышечной системы: часто — боль в конечностях; при приеме внутрь — мышечная ригидность.
Дерматологические реакции: нечасто — генерализованный зуд, сыпь.
Со стороны репродуктивной системы: нечасто — аменорея, нарушение эрекции, галакторея, гинекомастия, нерегулярные менструации, сексуальная дисфункция.
Аллергические реакции: анафилактическая реакция.
Со стороны лабораторных показателей: нечасто — повышение концентрации сывороточного пролактина, холестерина и глюкозы в крови.
Прочие: часто — астенические расстройства, слабость, местные реакции (боль, зуд, уплотнение в месте инъекции), увеличение массы тела; при приеме внутрь — периферические отеки.
Противопоказания к применению
Повышенная чувствительность к палиперидону; повышенная чувствительность к рисперидону (т.к.палиперидон является активным метаболитом рисперидона).
Применение при беременности и кормлении грудью
Палиперидон можно применять при беременности только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода. Влияние палиперидона на схватки и роды у человека неизвестно.
Применение нейролептиков в III триместре беременности сопровождается развитием обратимых экстрапирамидных расстройств у новорожденных.
В исследованиях применения палиперидона у животных и рисперидона у людей обнаружено, что палиперидон выделяется с грудным молоком. При необходимости применения в период лактации следует прекратить грудное вскармливание.
Особые указания
Палиперидон обладает альфа-адреноблокирующей активностью и у некоторых пациентов может вызывать ортостатическую гипотензию, поэтому необходима осторожность при применении у пациентов с сердечно-сосудистыми заболеваниями (например, с сердечной недостаточностью, инфарктом или ишемией миокарда, нарушением сердечной проводимости), нарушениями мозгового кровообращения или состояниями, предрасполагающими к снижению АД (например, обезвоживание, уменьшение ОЦК, применение гипотензивных препаратов).
Как и другие нейролептики, палиперидон следует с осторожностью применять у пациентов, имеющих в анамнезе судороги или другие состояния, при которых возможно снижение судорожного порога.
С применением нейролептиков связывают ухудшение способности организма снижать температуру тела, поэтому необходима осторожность при применении препарата у пациентов, которые могут подвергаться воздействиям, повышающим температуру тела, например, сильной физической нагрузке, высокой температуре окружающей среды, воздействию препаратов с м-холинолитической активностью, а также обезвоживанию.
Как и в при применении других нейролептиков, необходима осторожность при применении палиперидона у пациентов, имеющих в анамнезе указания на аритмию или врожденное удлинение интервала QT, либо принимающим препараты, удлиняющие интервал QT.
Учитывая действие палиперидона на ЦНС, следует с осторожностью применять палиперидон в комбинации с другими лекарственными средствами, действующими на ЦНС, и алкоголем.
Палиперидон может ослаблять эффект леводопы и агонистов допамина.
С осторожность применять у пациентов пожилого возраста с деменцией, пациентов с болезнью Паркинсона или деменцией с тельцами Леви.
При применении нейролептиков, в т.ч. палиперидона, зарегистрировано развитие ЗНС, который характеризуется гипертермией, мышечной ригидностью, нестабильностью вегетативной нервной системы, нарушением сознания и повышением концентрации КФК в сыворотке. Кроме того, могут наблюдаться миоглобинурия (рабдомиолиз) и острая почечная недостаточность. При появлении симптомов, позволяющих предположить ЗНС, все нейролептики, включая палиперидон, следует отменить.
Применение препаратов, обладающих свойствами антагонистов допаминовых рецепторов, сопровождается развитием поздней дискинезии, характеризующейся ритмичными, непроизвольными движениями, главным образом языка и/или лицевых мышц. При появлении симптомов поздней дискинезии следует рассмотреть возможность отмены всех нейролептиков, включая палиперидон.
В период лечения рекомендуется контролировать состояние больных сахарным диабетом и больных, имеющих факторы риска развития сахарного диабета.
Имеются данные о способности препаратов, обладающих свойствами альфа-адреноблокаторов, вызывать приапизм. Такое явление зарегистрировано в рамках постмаркетингового контроля применения палиперидона для приема внутрь.
В доклинических исследованиях палиперидона обнаружено противорвотное действие. Появление этого эффекта у пациента может маскировать признаки и симптомы передозировки некоторых лекарств или, например, такие состояния, как непроходимость кишечника, синдром Рейе или опухоль мозга.
Влияние на способность к управлению транспортными средствами и механизмами
Палиперидон может нарушать выполнение действий, требующих концентрации внимания и быстроты психомоторных реакций, и может влиять на зрение. Поэтому пациентам следует рекомендовать не управлять транспортными средствами и движущимися механизмами, пока не будет установлена их индивидуальная чувствительность.
Лекарственное взаимодействие
Палиперидон способен увеличивать интервал QT, поэтому необходима осторожность при одновременном применении с другими лекарственными средствами, увеличивающими интервал QT: антиаритмики (в т.ч. хинидин, прокаинамид, амиодарон, соталол); антипсихотические лекарственные средства (хлорпромазин, тиоридазин); антибиотики (в т.ч. гатифлоксацин, моксифлоксацин).
Учитывая действие палиперидона на ЦНС, необходима осторожность при комбинации с другими лекарственными средствами центрального действия и алкоголем.
Палиперидон может ослаблять эффект леводопы и агонистов допаминовых рецепторов.
Из-за способности палиперидона вызывать ортостатическую гипотензию может наблюдаться аддитивное усиление этого эффекта при одновременном применении с другими препаратами, обладающими такой способностью.
Палиперидон не является субстратом изоферментов CYP1A2, CYP2A6, CYP2C9, CYP2C19 и CYP3A5. Это позволяет предположить слабую вероятность взаимодействия с ингибиторами и индукторами этих изоферментов. Хотя исследования in vitro показывают возможность минимального участия CYP2D6 и CYP3A4 в метаболизме палиперидона, в настоящее время нет данных о том, что эти ферменты могут играть существенную роль в метаболизме палиперидона in vitro или in vivo. Исследования in vitro свидетельствуют о том, что палиперидон является субстратом Р-гликопротеина.
Прием палиперидона с длительным высвобождением активного компонента (1 раз/сут) перорально одновременно с карбамазепином (200 мг 2 раза/сут) приводил к снижению средней Сmax и AUC палиперидона примерно на 37%. Это снижение в значительной степени обусловлено увеличением почечного клиренса палиперидона на 35%, вероятно, за счет активации почечного Р-гликопротеина карбамазепином. Очень небольшое уменьшение количества палиперидона, которое выводится почками в неизмененном виде, позволяет предположить, что карбамазепин лишь слабо влияет на путь выведения, опосредуемый через метаболизм в печени, или биодоступность палиперидона. При начале применения карбамазепина дозу палиперидона следует пересмотреть и, при необходимости, увеличить. Наоборот, при отмене карбамазепина дозу палиперидона следует пересмотреть и, при необходимости, уменьшить.
Палиперидон при физиологической рН является катионом и в основном выводится в неизмененном виде почками — половина путем фильтрации, а половина — путем активной секреции. Одновременное применение триметоприма, который ингибирует систему активного транспорта катионов в почках, не влияло на фармакокинетику палиперидона.
Ксеплион — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
– ЛСР-009014/10
Торговое название препарата
– Ксеплион
Международное непатентованное название:
– палиперидон
Лекарственная форма:
– суспензия для внутримышечного введения пролонгированного действия
Состав
Каждый предварительно заполненный шприц содержит:
Активное вещество: 100 мг палиперидона в 1 мл суспензии (эквивалентно 156 мг палиперидона пальмитата).
Вспомогательные вещества: полисорбат 20 – 12 мг, макрогол 4000 (полиэтиленгликоль 4000) – 30 мг, лимонной кислоты моногидрат – 5 мг, натрия гидрофосфат – 5 мг, натрия дигидрофосфата моногидрат – 2,5 мг, натрия гидроксид – 2,84 мг, вода для инъекций – до 1 мл.
Описание
Белая или почти белая суспензия, свободная от посторонних включений
Фармакотерапевтическая группа:
– антипсихотическое средство (нейролептик).
Код АТХ
– N05AX
Фармакологические свойства
Фармакодинамика
Механизм действия
Палиперидона пальмитат гидролизуется до палиперидона. Последний является центральнодействующим активным антагонистом преимущественно серотониновых 5-HT2A-рецепторов, а также дофаминовых D2-рецепторов, адренергических ?1— и ?2— рецепторов и Н1-гистаминовых рецепторов. Палиперидон не связывается с холинергическими м-рецепторами и с адренергическими ?1— и ?2— рецепторами. Фармакологическая активность (+) и (-) энантиомеров палиперидона количественно и качественно одинакова.
Предполагается, что терапевтическая эффективность препарата при шизофрении обусловлена комбинированной блокадой D2 и 5-HT2A -рецепторов.
Фармакокинетика
Всасывание и распределение
Из-за исключительно низкой растворимости в воде палиперидона пальмитат после внутримышечного введения медленно растворяется и всасывается в системный кровоток. После однократного внутримышечного введения концентрация палиперидона в плазме крови медленно увеличивается, достигая максимума через 13-14 дней (медиана) после введения в дельтовидную мышцу и 13-17 дней после введения в ягодичную мышцу. Высвобождение вещества обнаруживается уже в 1-ый день и сохраняется, по меньшей мере, 126 дней. Характеристики высвобождения активного компонента и схема дозирования препарата Ксеплион обеспечивают длительное поддержание терапевтической концентрации. После однократного введения дозы 25 — 150 мг в дельтовидную мышцу максимальная концентрация (Сmax) в среднем на 28% больше, чем после введения в ягодичную мышцу. В начале терапии введение препарата в дельтовидную мышцу помогает быстрее достичь терапевтической концентрации палиперидона (150 мг в 1-ый день и 100 мг на 8-ой день), чем введение в ягодичную мышцу. После многократных инъекций разница во воздействии менее очевидна. Среднее отношение максимальной и равновесной концентраций палиперидона после введения 4-х инъекций препарата Ксеплион в дозе 100 мг в ягодичную мышцу равнялось 1,8, а после введения в дельтовидную мышцу – 2,2. При дозах палиперидона 25-150 мг площадь под кривой «концентрация-время» (AUC) палиперидона изменялась пропорционально дозе, а Сmax при дозах более 50 мг увеличивалась в меньшей степени, чем пропорционально дозе.
Медиана периода полувыведения палиперидона после введения препарата Ксеплион в дозах 25-150 мг колебалась в пределах 25 — 49 дней.
После введения препарата (-)-энантиомер палиперидона частично превращается в (+)-энантиомер, и отношение AUC (+)- и (-)-энантиомеров составляет примерно 1,6-1,8.
В популяционном анализе кажущийся объем распределения палиперидона равнялся 391 л; палиперидон связывается с белками плазмы крови на 74%.
Метаболизм и выведение
За неделю после однократного перорального приема 1 мг препарата 14С-палиперидона с немедленным высвобождением активного компонента с мочой в неизмененном виде выводится 59% введенной дозы; это указывает на отсутствие существенного метаболизма препарата в печени. Примерно 80% введенной радиоактивности обнаруживалось в моче и 11% — в кале. Известны 4 пути метаболизма препарата in vivo, но ни один из них не обуславливает метаболизма более чем 6,5% введенной дозы: дезалкилирование, гидроксилирование, дегидрогенизация, отщепление бензизоксазольной группы. Хотя исследования in vitro позволяют предположить определенную роль изоферментов CYP2D6 и CYP3A4 в метаболизме палиперидона, данных о существенной роли этих изоферментов в метаболизме палиперидона in vivo нет. Популяционный фармакокинетический анализ не выявил заметного различия клиренса палиперидона после перорального приема препарата людьми с активным и слабым метаболизмом CYP2D6. Исследования с использованием микросом печени человека in vitro показали, что палиперидон существенно не ингибирует метаболизм лекарственных средств изоферментами CYP1A2, CYP2A6, CYP2D6, CYP2E1, CYP3A4 и CYP3A5.
В исследованиях in vitro палиперидон проявлял свойства субстрата P-гликопротеина, а в высоких концентрациях — свойства слабого ингибитора P-гликопротеина. Соответствующих данных in vivo нет, и клиническая значимость этих сведений неясна.
В целом, концентрация палиперидона в плазме крови в период нагрузки после внутримышечного введения препарата Ксеплион лежала в том же диапазоне, что и после приема палиперидона пролонгированного действия перорально с высвобождением активного компонента в дозах между 6 и 12 мг. Использованная схема нагрузки палиперидона обеспечивает поддержание концентрации в этом диапазоне даже в конце междозового интервала (8-ой и 36-ой день). Индивидуальные различия фармакокинетики палиперидона после введения препарата Ксеплион у разных пациентов были меньше, чем после приема палиперидона пролонгированного действия перорально. Из-за различия характера изменения медианы концентрации палиперидона в плазме крови при применении двух препаратов, следует проявлять осторожность при прямом сравнении их фармакокинетики.
Особые категории больных
Нарушение функции печени.
Палиперидон не подвергается существенному метаболизму в печени. Хотя применение препарата Ксеплион у больных с нарушением функции печени легкой или средней степени тяжести не изучалось, при таких нарушениях функции печени коррекция дозы не требуется. В исследовании применение палиперидона перорально у больных с нарушением функции печени средней степени тяжести (класс В по Чайлду-Пью) концентрация свободного палиперидона в плазме крови была такой же, как у здоровых добровольцев. У больных с нарушением функции печени тяжелой степени применение палиперидона не изучалось.
Нарушение функции почек.
Для больных с нарушением функции почек легкой степени тяжести дозу палиперидона следует уменьшить; Ксеплион не рекомендуется применять у больных с нарушением функции почек средней степени тяжести и тяжелой степени. Было изучено распределение палиперидона после однократного приема внутрь таблетки палиперидона пролонгированного действия 3 мг больными с разной степенью нарушения функций почек. С уменьшением клиренса креатинина (КК) выведение палиперидона ослаблялось: при нарушении функций почек легкой степени тяжести (КК 50-80 мл/мин) — на 32%, при средней степени тяжести (КК 30-50 мл/мин) – на 64%, при тяжелой степени (КК 10-30 мл/мин) – на 71%, в результате чего AUC0-? увеличилась по сравнению со здоровыми добровольцами соответственно в 1,5, 2,6 и 4,8 раза. Исходя из небольшого количества данных о применении препарата Ксеплион у больных с нарушением функции почек легкой степени тяжести и из результатов моделирования фармакокинетики, рекомендуемая нагрузочная доза палиперидона для таких больных составляет 75 мг в 1-ый и 8-ой день; после этого ежемесячно (каждые 4 недели) вводят по 50 мг.
Пожилые больные.
Возраст сам по себе не является фактором, требующим коррекции дозы. Однако такая коррекция может потребоваться из-за возрастного уменьшения КК.
Раса.
Популяционный фармакокинетический анализ результатов исследования палиперидона для приема внутрь не выявил различия фармакокинетики палиперидона после приема препарата людьми разных рас.
Пол.
Клинически значимых различий фармакокинетики палиперидона у мужчин и женщин не найдено.
Влияние курения на фармакокинетику препарата.
Согласно исследованиям с использованием микросом печени человека in vitro, палиперидон не является субстратом CYP1A2, поэтому курение не должно влиять на фармакокинетику палиперидона. В соответствии с этими данными in vitro, популяционный фармакокинетический анализ не выявил различия фармакокинетики палиперидона у курящих и не курящих людей.
Показания к применению:
Лечение шизофрении и профилактика рецидивов шизофрении.
Противопоказания:
Гиперчувствительность к палиперидону или любому компоненту препарата. Поскольку палиперидон является активным метаболитом рисперидона, Ксеплион противопоказан больным с известной гиперчувствительностью к рисперидону.
C осторожностью
Следует с осторожностью применять Ксеплион в следующих случаях (см. более подробную информацию в разделе «Особые указания»):
— У больных с сердечно-сосудистыми заболеваниями (например, сердечной недостаточностью, инфарктом или ишемией миокарда, нарушением сердечной проводимости), нарушениями мозгового кровообращения или состояниями, предрасполагающими к снижению артериального давления (например, обезвоживание, уменьшение объема циркулирующей крови, применение гипотензивных препаратов).
— У больных, имеющих в анамнезе судороги или другие состояния, при которых может снижаться судорожный порог.
— У больных, которые могут подвергаться воздействиям, повышающим температуру тела, например, сильной физической нагрузке, высокой температуре окружающей среды, воздействию препаратов с активностью м холинолитиков, а также обезвоживанию.
— У больных, имеющих в анамнезе аритмию или врожденное удлинение интервала Q-T, либо принимающих препараты, удлиняющие интервал Q-T.
— При применении в комбинации с другими лекарственными средствами, действующими на ЦНС, и алкоголем. Палиперидон может ослаблять эффект леводопы и агонистов дофамина.
— У пациентов с деменцией, пациентов с болезнью Паркинсона или деменцией с тельцами Леви.
— У пациентов с возможными пролактин-зависимыми опухолями.
— У пациентов с нарушением функции печени или почек.
Применение при беременности и лактации
Беременность
Безопасность применения препарата Ксеплион внутримышечно или палиперидона перорально при беременности у людей не установлена. При применении высоких доз палиперидона перорально наблюдалось небольшое увеличение смертности плодов у животных. Ксеплион при внутримышечном введении не влиял на течение беременности крыс, но высокие дозы его были токсичны для беременных самок. Дозы палиперидона при приеме внутрь и препарата Ксеплион при внутримышечном введении, которые создают концентрации, превышающие максимальные терапевтические дозы у человека соответственно в 20-22 раза и в 6 раз, не влияли на потомство лабораторных животных.
Ксеплион можно применять при беременности только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода. Влияние препарата Ксеплион на схватки и роды у людей неизвестно.
В случае если женщина принимала антипсихотические препараты (включая палиперидон) в третьем триместре беременности, у новорожденных существует риск возникновения экстрапирамидных расстройств и/или синдрома отмены различной степени тяжести. Эти симптомы могут включать ажитацию, гипертонию, гипотонию, тремор, сонливость, респираторные нарушения и нарушение вскармливания.
Грудное вскармливание
В исследованиях применения палиперидона у животных и рисперидона у людей обнаружено выведение палиперидона с грудным молоком. Поэтому женщины, получающие Ксеплион, не должны кормить детей грудью.
Способ применения и дозы
У больных, никогда не принимавших палиперидон перорально или рисперидон перорально или парентерально, перед началом лечения препаратом Ксеплион рекомендуется в течение 2 — 7 дней проверить переносимость палиперидона или рисперидона перорально.
Рекомендуется начинать лечение препаратом Ксеплион с дозы 150 мг в 1-ый день и 100 мг через 1 неделю (обе инъекции в дельтовидную мышцу). Рекомендуется поддерживающая доза 75 мг 1 раз в месяц; эффект может наблюдаться от приема больших или меньших доз, в диапазоне 25 — 150 мг в зависимости от индивидуальной переносимости и/или эффективности. После второй начальной дозы последующие поддерживающие инъекции можно проводить в дельтовидную или ягодичную мышцу.
Поддерживающую дозу можно корректировать ежемесячно. При этом следует учитывать длительное высвобождение активного компонента из палиперидона пальмитата, так как эффект изменения дозы может полностью проявиться только через несколько месяцев.
Пропуск дозы
Избегание пропуска доз.
Вторую нагрузочную дозу палиперидона рекомендуется вводить через 1 неделю после первой дозы. Если это невозможно, то ее можно ввести на 4 дня раньше или позже. Аналогично, третью и последующие дозы рекомендуется вводить ежемесячно, но если это невозможно, то инъекцию можно сделать на 7 дней раньше или позже.
Если вторая инъекция препарата Ксеплион не была сделана вовремя (одна неделя ± 4 дня), рекомендуется возобновление лечения в зависимости от времени, которое прошло со дня первой инъекции.
Пропуск второй начальной дозы (срок менее 4 недель).
Если со дня первой инъекции прошло менее 4 недель, пациенту следует ввести вторую инъекцию в дозе 100 мг в дельтовидную мышцу как можно скорее. Третью инъекцию препарата Ксеплион в дозе 75 мг следует сделать в дельтовидную или ягодичную мышцу через 5 недель после первой инъекции (не учитывая время второй инъекции). В дальнейшем должен соблюдаться ежемесячный курс инъекций в дозе от 25 мг до 150 мг в дельтовидную или ягодичную мышцу в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск второй начальной дозы (срок от 4 до 7 недель).
Если со дня первой инъекции препарата Ксеплион прошло от 4 до 7 недель, лечение возобновляют введением двух инъекций в дозировке 100 мг по следующей схеме: первую инъекцию в дельтовидную мышцу делают как можно скорее; через 1 неделю делают вторую инъекцию в дельтовидную мышцу, затем продолжают ежемесячный курс инъекций в дельтовидную или ягодичную мышцу в дозе от 25 мг до 150 мг в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск второй начальной дозы (более 7 недель).
Если с момента первой инъекции препарата Ксеплион прошло более 7 недель, лечение начинают так же, как в случае инициации лечения препаратом Ксеплион.
Пропуск поддерживающей дозы (срок от 1 месяца до 6 недель).
После начала лечения рекомендуется проводить инъекции препарата Ксеплион ежемесячно. Если с момента последней инъекции прошло менее 6 недель, то следует как можно скорее ввести очередную дозу, равную предыдущей. После этого вводить препарат ежемесячно.
Пропуск поддерживающей дозы (срок от > 6 недель до 6 месяцев).
Если с момента последней инъекции препарата Ксеплион прошло более 6 недель, рекомендуется следующее:
Для пациентов, стабилизированных дозой от 25 мг до 100 мг:
1) Делают инъекцию препарата в дельтовидную мышцу как можно скорее в той дозе, на которой прошла стабилизация состояния пациента до пропуска инъекции;
2) Следующую инъекцию в дельтовидную мышцу (такая же доза) делают через неделю на 8-й день;
3) Далее возобновляют ежемесячный курс инъекций в дельтовидную или ягодичную мышцу в дозе от 25 мг до 150 мг в зависимости от индивидуальной переносимости и/или эффективности.
Для пациентов, стабилизированных дозой 150 мг:
1) Как можно скорее вводят дозу 100 мг в дельтовидную мышцу;
2) Через 1 неделю вводят еще одну дозу 100 мг (8-й день) в дельтовидную мышцу;
3) Далее возобновляют ежемесячный курс инъекций в дельтовидную или ягодичную мышцу в дозе от 25 мг до 150 мг в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск поддерживающей дозы (срок > 6 месяцев).
Если с момента последней инъекции препарата Ксеплион прошло более 6 месяцев, то лечение начинают заново, как описано выше для начала лечения.
Способ применения
Ксеплион предназначен только для внутримышечного введения. Препарат медленно вводят глубоко в мышцу. Инъекции должен проводить только медицинский работник. Всю дозу вводят за один раз; нельзя вводить дозу за несколько инъекций. Нельзя вводить препарат в сосуды или подкожно. Следует избегать случайного попадания в кровеносный сосуд. Для этого перед началом введения препарата поршень шприца оттягивают назад для проверки на предмет попадания иглы в крупный кровеносный сосуд. В случае, если при этом в шприц поступает кровь, следует извлечь иглу и шприц из мышцы пациента и утилизировать их.
Рекомендуемый размер иглы для введения препарата Ксеплион в дельтовидную мышцу определяется массой тела пациента. Для больных с массой тела ?90 кг рекомендуется длинная игла с серым корпусом из набора. Для больных с массой тела Для введения препарата Ксеплион в ягодичную мышцу рекомендуется длинная игла с серым корпусом из набора. Инъекции нужно проводить в верхний наружный квадрант ягодицы. Следует поочередно вводить препарат в правую и левую ягодичную мышцу.
Поскольку палиперидон является основным активным метаболитом рисперидона, следует соблюдать осторожность при одновременном применении в течение длительного периода времени препарата Ксеплион и рисперидона или пероральной формы палиперидона. Данные по безопасности одновременного применения препарата Ксеплион и других антипсихотиков ограничены.
Больные с нарушением функции печени
Применение препарата Ксеплион у больных с нарушением функции печени не изучалось. Исходя из результатов исследования палиперидона для приема внутрь, для больных с нарушением функции печени легкой или средней степени тяжести коррекции дозы не требуется. Применение препарата Ксеплион у больных с нарушением функций печени тяжелой степени не изучалось.
Больные с нарушением функции почек
Применение препарата Ксеплион у больных с нарушением функции почек систематически не изучалось. У больных с нарушением функции почек легкой степени тяжести (клиренс креатинина от ≥ 50 до Ксеплион не рекомендуется применять у больных с нарушением функции почек средней или тяжелой степени (клиренс креатинина Пожилые больные
В целом, для пожилых больных с нормальной функцией почек рекомендуется та же доза препарата Ксеплион, что и для более молодых больных с нормальной функцией почек. У пожилых больных функция почек может быть снижена, и на таких больных распространяются приведенные выше рекомендации для больных с нарушением функции почек.
Подростки и дети
Безопасность и эффективность применения препарата Ксеплион у больных моложе 18 лет не изучалась.
Другие особые категории больных
Коррекции дозы препарата Ксеплион в зависимости от пола, расы больных и курения не требуется.
Перевод с других нейролептиков
Данные о переводе больных шизофренией с других нейролептиков на Ксеплион или о его применении одновременно с другими нейролептиками систематически не собирались. Для пациентов, которые никогда не принимали пероральный палиперидон или пероральный или инъекционный рисперидон, должна быть исследована переносимость с пероральным палиперидоном или пероральным рисперидоном перед началом лечения препаратом Ксеплион. В начале лечения препаратом Ксеплион ранее применявшиеся перорально нейролептики можно постепенно отменить. Ксеплион следует назначать, как описано выше в разделе «Способ применения и дозы». Если пациент получает инъекционные нейролептики пролонгированного действия, лечение препаратом Ксеплион начинают сразу с поддерживающей дозы в момент очередной запланированной инъекции. Следует продолжать лечение препаратом Ксеплион 1 раз в месяц. Начальная доза на первой неделе лечения не требуется.
У пациентов, которые были стабилизированы различными дозами препарата Рисполепт Конста®, суспензия для внутримышечного введения пролонгированного действия, равновесные концентрации активного вещества могут достигать схожих значений в течение поддерживающей терапии препаратом Ксеплион 1 раз в месяц согласно следующей схеме:
| Последняя доза Рисполепт Конста® |
Начальная доза Ксеплион |
| 25 мг каждые 2 недели | 50 мг 1 раз в месяц |
| 37,5 мг каждые 2 недели | 75 мг 1 раз в месяц |
| 50 мг каждые 2 недели | 100 мг 1 раз в месяц |
Отмену предыдущего антипсихотика следует провести в соответствии с инструкцией по медицинскому применению. При отмене препарата Ксеплион следует учитывать длительное высвобождение активного компонента. Как и в случае с другими нейролептиками, следует периодически оценивать необходимость продолжения применения средств профилактики развития экстрапирамидных расстройств.
Побочное действие
Наиболее частыми нежелательными реакциями, зарегистрированными в клинических исследованиях, были бессонница, головная боль, беспокойство, инфекции верхних дыхательных путей, реакции в месте введения, паркинсонизм, повышение веса, акатизия, возбуждение, седация, сонливость, тошнота, констипация, головокружение, скелетно-мышечная боль, тахикардия, тремор, боль в животе, рвота, диарея, усталость, дистония. Из них дозозависимыми оказались седация и сонливость.
Большинство нежелательных побочных реакций (НПР) были слабыми или средней тяжести.
Ниже указаны нежелательные реакции, наблюдавшиеся у пациентов. Частоту нежелательных реакций классифицировали следующим образом: очень часто (≥ 10 %), часто (≥ 1 % и Инфекции:
часто – инфекции мочевыделительной системы, грипп, инфекции верхних дыхательных путей;
нечасто – акародерматит, бронхит, воспаление подкожной жировой клетчатки, инфекции уха, инфекции глаза, пневмония, инфекции дыхательных путей, синусит, подкожный абсцесс, тонзиллит, цистит;
редко — онихомикоз.
Со стороны иммунной системы:
нечасто – гиперчувствительность;
редко – анафилактические реакции.
Нарушения со стороны кровеносной и лимфатической системы:
нечасто – анемия, снижение гематокрита, увеличение количества эозинофилов, уменьшение количества белых кровяных клеток;
редко – тромбоцитопения, нейтропения, агранулоцитоз.
Нарушения со стороны эндокринной системы:
часто – гиперпролактинемия;
редко – неадекватная секреция антидиуретического гормона;
с неизвестной частотой – глюкоза в моче.
Метаболические нарушения:
часто – гипергликемия, снижение массы тела, увеличение концентрации триглицеридов в плазме крови, повышение массы тела;
нечасто – гиперинсулинемия, анорексия, снижение аппетита, повышение аппетита, сахарный диабет, увеличение концентрации холестерина в крови;
редко – полидипсия, гипогликемия, водная интоксикация, диабетический кетоацидоз.
Психиатрические расстройства:
очень часто – бессонница;
часто – беспокойство, депрессия, возбуждение;
нечасто – снижение либидо, нервозность, ночные кошмары, состояние замешательства, нарушение сна, мании;
редко – аноргазмия, эмоциональная уплощенность.
Нарушения со стороны нервной системы:
очень часто – головная боль;
часто – седация, дистония, дискинезия, тремор, акатизия, головокружение, экстрапирамидные симптомы, сонливость, паркинсонизм;
нечасто – судороги (в том числе эпилептические судороги), рассеянность внимания, постуральное головокружение, дизартрия, гипоэстезия, парэстезия, психомоторная гиперактивность, обморок, тяжелая дискинезия, дисгевзия;
редко – злокачественный нейролептический синдром, церебральная ишемия, отсутствие реакции на раздражители, потеря сознания, снижение уровня сознания, диабетическая кома, нарушения равновесия, нарушения координации, дрожание головы.
Офтальмологические нарушения:
нечасто – сухость глаз, нечеткость зрительного восприятия, конъюнктивит;
редко – глаукома, светобоязнь, увеличение слезотечения, окулярная гиперемия, непроизвольное движение глазного яблока, ротаторный нистагм.
Нарушения со стороны органа слуха и равновесия:
нечасто – вертиго, шум в ушах, боль в ухе.
Нарушения со стороны сердечно-сосудистой системы:
часто – брадикардия, тахикардия, повышение артериального давления;
нечасто – снижение артериального давления, атриовентрикулярная блокада, нарушение проводимости, нарушения на электрокардиограмме, увеличение интервала QT на электрокардиограмме, сердцебиение, синдром постуральной ортостатической тахикардии, фибрилляция предсердий, ортостатическая гипотензия;
редко – тромбоз глубоких вен, синусовая аритмия, эмболия легочной артерии, ишемия, приливы.
Нарушения со стороны дыхательной системы:
часто — кашель, заложенность носа;
нечасто – диспноэ, носовое кровотечение, боль в глоточно-гортанной области, свистящее дыхание, заложенность легких;
редко – гипервентиляция, аспирационная пневмония, заложенность дыхательных путей, дисфония, синдром апноэ во сне.
Желудочно-кишечные нарушения:
часто – диспепсия, боль в верхней части живота, запор, диарея, тошнота, зубная боль, рвота;
нечасто – дискомфорт в области живота, сухость слизистой оболочки полости рта, метеоризм, гастроэнтерит;
редко – панкреатит, недержание кала, отек языка, дисфагия, кишечная непроходимость, каловые камни, хейлит.
Нарушения со стороны гепатобилиарной системы:
часто — повышение активности печеночных трансаминаз;
нечасто – увеличение активности гамма-глутамилтрансферазы, увеличение активности ферментов печени;
редко – желтуха.
Нарушения со стороны костно-мышечной системы и соединительной ткани:
часто – боль в спине, боль в конечностях, скелетно-мышечная боль;
нечасто – артралгия, скованность суставов, мышечные спазмы, боль в шее;
редко — опухание суставов, рабдомиолиз, повышение активности креатинфосфокиназы, мышечная слабость, анормальное положение.
Нарушения со стороны кожи
часто – кожная сыпь;
нечасто – акне, сухость кожи, экзема, эритема, крапивница, зуд, алопеция;
редко – ангиоэдема, гиперкератоз, изменения цвета кожи, себорейный дерматит, перхоть, лекарственная сыпь.
Нарушения со стороны мочевыделительной системы:
нечасто – дизурия, поллакиурия, недержание мочи;
редко – задержка мочевыведения.
Нарушения со стороны репродуктивной системы и молочных желез:
нечасто – задержка менструации, нарушения менструации, аменорея, галакторея, гинекомастия, сексуальная дисфункция, нарушения эякуляции, эректильная дисфункция, вагинальные выделения;
редко – приапизм, боль в молочных железах, дискомфорт в молочных железах, нагрубание молочных желез, увеличение молочных желез, выделения из молочных желез.
Влияние на течение беременности, послеродовые и перинатальные состояния:
редко – синдром отмены у новорожденных.
Прочие:
часто – лихорадка, астенические расстройства, слабость, местные реакции (боль, зуд, уплотнение в месте инъекции);
нечасто – боль в груди, дискомфорт в области груди, отек лица, нарушение походки, недомогание, уплотнение в месте укола, отеки (в том числе генерализованный отек, периферический отек, мягкий отек), падение;
редко – озноб, повышение температуры тела, снижение температуры тела, жажда, синдром отмены, киста в месте введения, гипотермия, абсцесс в месте введения инъекции, воспаление подкожной клетчатки в месте введения инъекции, гематома в месте введения инъекции.
Нежелательные реакции, зарегистрированные при применении рисперидона
Палиперидон является активным метаболитом рисперидона, поэтому профили побочных реакций рисперидона и палиперидона взаимосвязаны. В дополнение к вышеперечисленным, при применении рисперидона были отмечены следующие побочные реакции, которые могут возникнуть и при применении препарата Ксеплион:
Нарушения со стороны нервной системы:
нарушение мозгового кровообращения.
Офтальмологические нарушения:
интраоперационный синдром дряблой радужки.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
хрипы.
Общие нарушения и нарушения в месте введения (наблюдались при применении инъекционной формы рисперидона):
некроз в месте введения инъекции, язва в месте введения инъекции.
Описание отдельных побочных реакций
Анафилактические реакции
Редкие случаи анафилактических реакций при введении препарата Ксеплион были зафиксированы в постмаркетинговом периоде у пациентов, ранее хорошо переносивших терапию пероральными формами рисперидона или палиперидона.
Реакции в месте введения
Наиболее часто сообщавшейся реакцией в месте введения была боль, которая в большинстве случаев была слабой или средней степени тяжести. Согласно оценке с использованием визуальной аналоговой шкалы, частота и интенсивность боли со временем снижалась во всех клинических исследованиях II и III фазы. Инъекции в дельтовидную мышцу воспринимаются как немного более болезненные по сравнению с инъекциями в ягодичную мышцу. Другие реакции в месте введения в основном были легкой степени тяжести и включали уплотнение (часто), зуд (нечасто) и узелки (редко).
Экстрапирамидные симптомы (ЭС)
ЭС включают следующие термины: паркинсонизм (включает гиперсаливацию, скелетно-мышечную скованность, паркинсонизм, слюнотечение, ригидность по типу «зубчатого колеса», брадикинезию, гипокинезию, маскоподобное лицо, мышечное напряжение, акинезию, ригидность затылочных мышц, мышечную ригидность, паркинсоническую походку, нарушение глабеллярного рефлекса и паркинсонический тремор покоя), акатизию (включает акатизию, возбужденное состояние, гиперкинезию и синдром беспокойных ног), дискинезию (включает дискинезию, подергивание мышц, хореоатетоз, атетоз и миоклонию), дистонию (включает дистонию, гипертонию, кривошею, непроизвольные мышечные сокращения, миогенную контрактуру, блефароспазм, движение глазного яблока, паралич языка, спазм лица, ларингоспазм, миотонию, опистотонус, орофарингеальный спазм, плеврототонус, спазм языка и судорожное стискивание челюстей) и тремор. В данный список включен более широкий спектр симптомов, которые могут иметь не экстрапирамидное происхождение.
Снижение веса
В 13-недельном клиническом исследовании с использованием начальной дозы 150 мг было показано, что аномальное увеличение массы тела > 7 % является дозозависимым. Увеличение массы тела отмечалось с частотой 5 % в группе плацебо и с частотой 6 %, 8 % и 13 % при применении Ксеплиона в дозе 25 мг, 100 мг и 150 мг соответственно.
В течение 33-недельного открытого периода перехода на терапию Ксеплионом или поддерживающей терапии Ксеплионом долгосрочного клинического исследования 12 % пациентов, получавших лечение Ксеплионом, соответствовали данному критерию (увеличение массы тела на > 7 % от двойной слепой фазы до конечной точки).
Класс-эффекты
При применении антипсихотиков возможны удлинение интервала QT, возникновение желудочковых аритмий (желудочковая фибрилляция, желудочковая тахикардия), внезапная необъяснимая смерть, остановка сердца и тахикардия типа «пируэт». При применении антипсихотиков сообщается о случаях развития (с неизвестной частотой) венозного тромбоэмболизма, включая случаи легочной эмболии и тромбоза глубоких вен.
Передозировка
Поскольку Ксеплион предназначен для введения медработниками, то вероятность его передозировки пациентами мала.
Симптомы
В целом, ожидаемые признаки и симптомы соответствуют усилению известного фармакологического действия палиперидона, т.е. сонливость, заторможенность, тахикардия, снижение артериального давления, удлинение интервала Q-T, экстрапирамидные симптомы. Полиформная желудочковая тахикардия типа «пируэт» и фибрилляция желудочков были отмечены при передозировке перорального палиперидона. В случае острой передозировки следует учитывать возможность получения пациентами нескольких препаратов.
Лечение
При оценке потребности в лечении и восстановлении больных следует учитывать длительное высвобождение активного вещества и большой период полувыведения палиперидона. Специфического антидота для палиперидона не существует. Следует осуществлять общие поддерживающие меры, обеспечить и поддерживать проходимость дыхательных путей, достаточную вентиляцию легких и насыщение крови кислородом. Следует немедленно начать контроль функции сердечно-сосудистой системы, включая постоянный мониторинг ЭКГ для выявления возможной аритмии. В случае снижения артериального давления крови и циркуляторного коллапса следует предпринимать соответствующие меры, например, внутривенное введение растворов и/или симпатомиметиков. При развитии тяжелых экстрапирамидных симптомов применяют антихолинергические препараты. Следует тщательно контролировать состояние больного до его восстановления.
Взаимодействие с другими лекарственными средствами
Как и другие антипсихотики, палиперидон может увеличивать интервал Q-T, поэтому его следует с осторожностью сочетать с другими лекарственными средствами, увеличивающими интервал Q-T, такими как антиаритмические лекарственные средства (в т.ч. хинидин, дизопирамид, прокаинамид, амиодарон, соталол), антигистаминные лекарственные средства, антипсихотические лекарственные средства (хлорпромазин, тиоридазин); антибиотики (в т.ч. гатифлоксацин, моксифлоксацин), некоторые лекарственные средства против малярии (в т.ч. мефлохин).
Поскольку палиперидона пальмитат гидролизуется до палиперидона, то при оценке возможности лекарственного взаимодействия следует учитывать результаты исследований палиперидона для приема внутрь.
Способность препарата Ксеплион влиять на другие препараты
Не ожидается, что палиперидон будет проявлять клинически значимое фармакокинетическое взаимодействие с препаратами, метаболизируемыми изоферментами системы цитохрома Р450. Исследования с использованием микросом печени человека in vitro показали, что палиперидон существенно не ослабляет метаболизм веществ изоферментами CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4 и CYP3A5. Поэтому не ожидается, что палиперидон будет клинически значимо уменьшать клиренс препаратов, метаболизируемых этими изоферментами. Также не ожидается, что палиперидон будет проявлять свойства индуктора изоферментов, т.к. в исследованиях in vitro палиперидон не индуцировал активность изоферментов CYPA2, CYPC19 или CYP3A4.
Палиперидон в высоких концентрациях является слабым ингибитором Р-гликопротеина. Однако данных in vivo в этом отношении нет, и клиническая значимость этого явления неизвестна.
Учитывая действие палиперидона на ЦНС, следует с осторожностью применять Ксеплион в комбинации с другими лекарственными средствами центрального действия и алкоголем. Палиперидон может ослаблять эффект леводопы и агонистов дофаминовых рецепторов.
Из-за способности препарата Ксеплион вызывать ортостатическую гипотензию может наблюдаться аддитивное усиление этого эффекта при применении препарата Ксеплион совместно с другими препаратами, обладающими такой способностью.
Следует с осторожностью сочетать палиперидон с лекарственными средствами, снижающими судорожный порог, такими как фенотиазины, бутирофеноны, трициклические производные, селективные ингибиторы обратного захвата серотонина, трамадол, мефлохин и т.д.)
Одновременный прием перорального палиперидона в дозировке 12 мг 1 раз в день и таблеток натрия дивалпроекса пролонгированного действия (в дозировке 500 – 2000 мг 1 раз в день) не влияет на фармакокинетику вальпроата.
Фармакокинетическое взаимодействие между препаратом Ксеплион и литием маловероятно.
Способность других препаратов влиять на Ксеплион
Палиперидон не является субстратом изоферментов CYP1A2, CYP2A6, CYP2C9, CYP2C19 и CYP3A5. Это позволяет предположить слабую вероятность взаимодействия с ингибиторами и индукторами этих изоферментов. Хотя исследования in vitro показывают возможность минимального участия CYP2D6 и CYP3A4 в метаболизме палиперидона, в настоящее время нет данных о том, что эти ферменты могут играть существенную роль в метаболизме палиперидона in vitro или in vivo. Исследования in vitro свидетельствуют о том, что палиперидон является субстратом P-гликопротеина.
Палиперидон в ограниченной степени метаболизируется изоферментом CYP2D6. В исследовании взаимодействия палиперидона для приема внутрь с активным ингибитором CYP2D6 пароксетином у здоровых добровольцев не обнаружено клинически значимого изменения фармакокинетики палиперидона.
Прием палиперидона с длительным высвобождением активного компонента (1 раз в день) перорально одновременно с карбамазепином (200 мг 2 раза в день) приводил к снижению средней Сmax и AUC палиперидона примерно на 37%. Это снижение в значительной степени обусловлено увеличением почечного клиренса палиперидона на 35%, вероятно, за счет активации почечного P-гликопротеина карбамазепином. Очень небольшое уменьшение количества препарата, выводимого через почки в неизмененном виде, позволяет предположить, что карбамазепин лишь слабо влияет на метаболизм в печени или биодоступность палиперидона. При начале применения карбамазепина дозу препарата Ксеплион следует пересмотреть и, при необходимости, увеличить. Наоборот, при отмене карбамазепина дозу препарата Ксеплион следует пересмотреть и, при необходимости, уменьшить.
Палиперидон при физиологической рН является катионом и в основном выводится в неизмененном виде через почки – половина путем фильтрации, а половина – путем активной секреции. Одновременное применение триметоприма, который ингибирует систему активного транспорта катионов в почках, не влияло на фармакокинетику палиперидона.
При одновременном назначении перорального палиперидона пролонгированного действия в дозировке 12 мг 1 раз в день и таблеток пролонгированного действия натрия дивалпроекса (2 таблетки по 500 мг 1 раз в день) наблюдалось увеличение Cmax и AUC палиперидона на 50%, вероятно, в результате увеличения абсорбции препарата при пероральном приеме. Поскольку не наблюдалось значительного влияния на общий клиренс, не ожидается клинически значимого взаимодействия между дивалпроексом натрия, таблетки длительного высводобождения, и препаратом Ксеплион. Следует рассмотреть возможность уменьшения дозы препарата Ксеплион при одновременном назначении с вальпроатом на основании клинической оценки пациента. Исследований взаимодействия с препаратом Ксеплион не проводилось.
Фармакокинетическое взаимодействие лития и палиперидона маловероятно.
Применение препарата Ксеплион совместно с рисперидоном или с пероральной формой палиперидона
Поскольку палиперидон является активным метаболитом рисперидона, следует соблюдать осторожность при одновременном применении в течение длительного периода времени препарата Ксеплион и рисперидона или пероральной формы палиперидона. Данные по безопасности одновременного применения препарата Ксеплион и других антипсихотиков ограничены.
Особые указания
Интервал QT
Следует соблюдать осторожность при применении палиперидона у пациентов с известными сердечно-сосудистыми заболеваниями или с удлинением интервала QT в анамнезе, а также при совместном применении лекарственных средств, которые могут приводить к удлинению интервала QT.
Злокачественный нейролептический синдром
При применении нейролептиков, в том числе палиперидона, зарегистрировано развитие злокачественного нейролептического синдрома (ЗНС), характеризуемого гипертермией, мышечной ригидностью, нестабильностью вегетативной нервной системы, нарушением сознания и повышением концентрации креатинфосфокиназы сыворотки крови. Кроме того, могут наблюдаться миоглобинурия (рабдомиолиз) и острая почечная недостаточность. При появлении симптомов, позволяющих предположить ЗНС, все нейролептики, включая Ксеплион, отменяют.
Поздняя дискинезия
Применение препаратов, обладающих свойствами антагонистов дофаминовых рецепторов, сопровождается развитием поздней дискинезии, характеризующейся ритмичными, непроизвольными движениями, главным образом языка и/или лицевых мышц. При появлении симптомов поздней дискинезии следует рассмотреть возможность отмены всех нейролептиков, включая Ксеплион.
Гипергликемия и сахарный диабет
При лечении препаратом Ксеплион наблюдались гипергликемия, сахарный диабет и обострение уже имеющегося сахарного диабета. Установление взаимосвязи между применением атипичных антипсихотических препаратов и нарушением обмена глюкозы осложнено повышенным риском развития сахарного диабета у пациентов с шизофренией и распространенностью сахарного диабета в общей популяции. Учитывая эти факторы, взаимосвязь между применением атипичных антипсихотических препаратов и развитием побочных действий, связанных с гипергликемией, установлена не полностью. У всех пациентов необходимо проводить клинический контроль на наличие симптомов гипергликемии и сахарного диабета (см. раздел «Побочное действие»).
Увеличение массы тела
При лечении атипичными антипсихотиками наблюдалось значительное увеличение массы тела. Необходимо проводить контроль массы тела пациентов.
Гиперпролактинемия
Исследования культур ткани указывают на то, что рост опухоли молочной железы у человека может стимулироваться пролактином. Несмотря на то, что до сих пор в клинических и эпидемиологических исследованиях не была продемонстрирована прямая связь с применением антипсихотиков, следует соблюдать осторожность при применении палиперидона у пациентов с возможными пролактин-зависимыми опухолями.
Ортостатическая гипотензия
Обладая активностью альфа-адреноблокатора, палиперидон у некоторых больных может вызывать ортостатическую гипотензию. Ксеплион следует с осторожностью применять у больных с сердечно-сосудистыми заболеваниями (например, сердечной недостаточностью, инфарктом или ишемией миокарда, нарушением сердечной проводимости), нарушениями мозгового кровообращения или состояниями, предрасполагающими к снижению артериального давления (например, обезвоживание, уменьшение объема циркулирующей крови, применение гипотензивных препаратов).
Судороги
Как и другие нейролептики, Ксеплион следует с осторожностью применять у больных, имеющих в анамнезе судороги или другие состояния, при которых может снижаться судорожный порог.
Почечная недостаточность
Концентрация палиперидона в плазме повышена у пациентов с нарушением функции почек. У пациентов с нарушением функции почек легкой степени рекомендуется коррекция дозы. Ксеплион не рекомендуется применять у больных с нарушением функции почек средней или тяжелой степени (клиренс креатинина Печеночная недостаточность
Применение препарата Ксеплион у больных с нарушением функций печени тяжелой степени (класс С по шкале Чайлд-Пью) не изучалось. Следует соблюдать осторожность при применении палиперидона у таких пациентов.
Пожилые больные с деменцией
Перекрестный анализ результатов исследований показал повышенную смертность пожилых больных с деменцией, получавших атипичные нейролептики, в том числе рисперидон, арипипразол, оланзапин и кветиапин, по сравнению с плацебо. Среди больных, получавших рисперидон и плацебо, смертность составляла соответственно 4% и 3,1%.
Применение препарата Ксеплион у пожилых больных с деменцией не изучалось. Поскольку палиперидон является активным метаболитом рисперидона, то следует учитывать опыт применения рисперидона. Для пожилых пациентов с деменцией, принимающих рисперидон, наблюдалась повышенная смертность у пациентов, принимавших фуросемид и рисперидон, по сравнению с группой, принимавшей только рисперидон, и группой, принимавшей только фуросемид. Не установлено патофизиологических механизмов, объясняющих данное наблюдение. Тем не менее, следует соблюдать особую осторожность при назначении препарата в таких случаях. Не обнаружено увеличения смертности у пациентов, одновременно принимающих другие диуретики вместе с рисперидоном. Независимо от лечения, дегидратация является общим фактором риска смертности и должна тщательно контролироваться у пожилых пациентов с деменцией.
Нарушения мозгового кровообращения
В плацебо-контролируемых исследованиях обнаружена повышенная частота нарушений мозгового кровообращения (преходящих и инсульта), в том числе со смертельным исходом, у пожилых больных с деменцией, получавших некоторые атипичные нейролептики, в том числе рисперидон, арипипразол и оланзапин, по сравнению с применением плацебо.
Лейкопения, нейтропения, агранулоцитоз
Лейкопения, нейтропения и агранулоцитоз отмечались при применении антипсихотических средств, в т. ч. при применении препарата Ксеплион. Агранулоцитоз отмечался очень редко в течение постмаркетинговых наблюдений. Пациентам с клинически значимым уменьшением количества лейкоцитов в анамнезе или препарат-зависимой лейкопенией/нейтропенией рекомендуется проведение полного анализа крови в течение первых месяцев терапии, прекращение лечения препаратом Ксеплион должно быть рассмотрено при первом клинически значимом уменьшении количества лейкоцитов при отсутствии других возможных причин. Пациентам с клинически значимой нейтропенией рекомендуется наблюдаться на предмет повышения температуры или возникновения симптомов инфекции и начинать лечение немедленно при возникновении таких симптомов. Пациенты с тяжелой формой нейтропении (абсолютное количество нейтрофилов менее 1 х 109/л) должны прекратить применение препарата Ксеплион до тех пор, пока количество лейкоцитов не нормализуется.
Венозный тромбоэмболизм
При применении антипсихотических препаратов были отмечены случаи венозной тромбоэмболии. Поскольку пациенты, принимающие антипсихотические препараты, часто имеют риск развития венозной тромбоэмболии, все возможные факторы риска должны быть выявлены до и во время лечения препаратом Ксеплион, и должны быть предприняты предупреждающие меры.
Болезнь Паркинсона и деменция с тельцами Леви
Врач должен сопоставить риск и пользу применения нейролептиков, включая Ксеплион, у больных с болезнью Паркинсона или деменцией с тельцами Леви, так как у обеих этих категорий больных может быть повышен риск развития злокачественного нейролептического синдрома (ЗНС) и риск повышенной чувствительности к нейролептикам. Проявления повышенной чувствительности могут включать спутанность сознания, притупление болевой чувствительности, неустойчивость позы с частыми падениями, а также экстрапирамидные симптомы.
Приапизм
Имеются данные о способности препаратов, обладающих свойствами альфа-адреноблокаторов, вызывать приапизм. Приапизм зарегистрирован в рамках постмаркетингового контроля применения палиперидона.
Влияние на регуляцию температуры тела
С применением нейролептиков связывают ухудшение способности организма снижать температуру тела. Рекомендуется проявлять осторожность при назначении препарата Ксеплион больным, которые могут подвергаться воздействиям, повышающим температуру тела, например, сильной физической нагрузке, высокой температуре окружающей среды, воздействию препаратов с активностью м холинолитиков, а также обезвоживанию.
Противорвотное действие
В доклинических исследованиях палиперидона обнаружено противорвотное действие. Появление этого эффекта у пациента может маскировать признаки и симптомы передозировки некоторых лекарств или, например, такие состояния, как непроходимость кишечника, синдром Рейе или опухоль мозга.
Введение
При внутримышечном введении следует проявлять осторожность во избежание случайного попадания препарата в кровеносный сосуд.
Интраоперационный синдром дряблой радужки (ИСДР)
ИСДР наблюдался во время проведения оперативного вмешательства по поводу наличия катаракты у пациентов, получающих терапию препаратами, являющимися антагонистами ?1-адренорецепторов, такими, как Ксеплион.
ИСДР увеличивает риск возникновения осложнений, связанных с органом зрения, во время и после проведения операционного вмешательства. Врач, проводящий такую операцию, должен быть заблаговременно проинформирован о том, что пациент принимал или принимает в настоящее время препараты, обладающие активностью антагонистов ?1-адренорецепторов. Потенциальная польза отмены терапии антагонистами ?1-адренорецепторов перед оперативным вмешательством не установлена, и должна оцениваться с учетом рисков, связанных с отменой терапии антипсихотическими препаратами.
Влияние на вождение автомобиля и работу с механизмами
Ксеплион может нарушать выполнение действий, требующих концентрации внимания и быстроты психомоторных реакций, и может влиять на зрение. Поэтому больным следует рекомендовать не управлять транспортными средствами и движущимися механизмами, пока не будет установлена их индивидуальная чувствительность.
Форма выпуска:
Суспензия для внутримышечного введения пролонгированного действия, 25 мг/0,25 мл, 50 мг/0,50 мл, 75 мг/0,75 мл, 100 мг/1мл, 150мг/1,5 мл
По 0,25, 0,50, 0,75, 1,00, 1,50 мл препарата в шприц из циклолефинового сополимера. В комплект препарата входят 2 иглы для внутримышечных инъекций (в дельтовидную и ягодичную мышцу). Предварительно заполненный шприц с препаратом и 2 иглы в пластиковом поддоне, закрытом полиэтиленовой пленкой, помещают вместе с инструкцией по применению в картонную пачку.
Предварительно заполненный шприц
Указания по применению
Шприц предназначен только для однократного введения.
1. Интенсивно встряхните шприц в течение 10 секунд для получения однородной суспензии.
2. Выберите соответствующую иглу. Для введения в ДЕЛЬТОВИДНУЮ мышцу больным массой тела Для введения в ЯГОДИЧНУЮ мышцу используют длинную иглу (с серым корпусом).
3. Держа шприц вертикально, снимите с него резиновый колпачок путем аккуратного вращения по часовой стрелке.
4. Наполовину откройте упаковку безопасной иглы, возьмитесь за колпачок иглы через упаковку и вставьте шприц в люеровский колпачок иглы путем аккуратного вращения по часовой стрелке.
5. Снимите с иглы колпачок, потянув его вдоль иглы. Не вращайте колпачок, так как это может ослабить соединение иглы со шприцем.
6. Направьте шприц иглой вверх и выдавите из шприца воздух, слегка надавив на поршень.
7. Введите все содержимое шприца в выбранную мышцу (дельтовидную или ягодичную). Не вводите препарат в кровеносный сосуд или подкожно.
8. После завершения инъекции приведите защиту иглы в рабочее положение большим (рис. 8а) или указательным (рис. 8b) пальцем или надавив шприцем о твердую поверхность (рис. 8с). Защита иглы должна зафиксироваться со щелчком. Шприц с иглой уничтожьте так, как это полагается.
8a
8b
8c
Срок годности
2 года. Не применять после истечения срока годности.
Условия хранения
При температуре не выше 30 °С. Хранить в недоступном для детей месте.
Условия отпуска из аптек:
По рецепту
Производитель
Производство, упаковка и выпускающий контроль:
Янссен Фармацевтика Н.В., Беерсе, Турнхоутсевег, 30, В-2340, Бельгия
Держатель регистрационного удостоверения:
ООО «Джонсон & Джонсон», Россия, 121614, Москва, ул. Крылатская, 17/2
Купить Ксеплион в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Инвега® (6 мг)
МНН: Палиперидон
Производитель: Янссен Силаг Мануфэкчуринг ЛЛС
Анатомо-терапевтическо-химическая классификация: Paliperidone
Номер регистрации в РК:
№ РК-ЛС-5№019528
Информация о регистрации в РК:
06.06.2017 — 06.06.2022
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
1 351.77 KZT
- Скачать инструкцию медикамента
Торговое название
Инвега®
Международное непатентованное название
Палиперидон
Лекарственная форма
Таблетки, покрытые оболочкой, с пролонгированным высвобождением
3 мг, 6 мг, 9 мг
Состав
Одна таблетка 3 мг содержит
активное вещество – палиперидон 3 мг,
вспомогательные вещества: макрогол 200К, натрия хлорид, повидон (К29-32), стеариновая кислота, бутилгидрокситолуол, железа оксид желтый (Е172), макрогол 7000К, железа оксид красный (Е172), гидроксиэтилцеллюлоза, макрогол 3350, целлюлозы ацетат (398-10), краситель белый, карнаубский воск, чернила водорастворимые черные
Одна таблетка 6 мг содержит
активное вещество – палиперидон 6 мг,
вспомогательные вещества: макрогол 200К, натрия хлорид, повидон (К29-32), стеариновая кислота, бутилгидрокситолуол, железа оксид красный (Е172), макрогол 7000К, гидроксиэтилцеллюлоза, макрогол 3350, целюлозы ацетат (398-10), краситель бежевый, карнаубский воск, чернила водорастворимые черные
Одна таблетка 9 мг содержит
активное вещество – палиперидон 9 мг,
вспомогательные вещества: макрогол 200К, натрия хлорид, повидон (К29-32), стеариновая кислота, бутилгидрокситолуол, железа оксид черный (Е172), макрогол 7000К, железа оксид красный (Е172), гидроксиэтилцеллюлоза, макрогол 3350, целлюлозы ацетат (398-10), краситель розовый, карнаубский воск, чернила водорастворимые черные
Описание
Таблетки капсуловидной формы белого (для дозировки 3 мг), бежевого (для дозировки 6 мг), розового (для дозировки 9 мг) цвета. Таблетки имеют надпись «PAL 3», «PAL 6» или «PAL 9» (соответственно дозировке – 3 мг, 6 мг или 9 мг). Выпускные отверстия могут быть видимы или невидимы при визуальном осмотре.
Фармакотерапевтическая группа
Психотропные препараты. Нейролептики (Антипсихотики). Нейролептики другие. Палиперидон.
Код АТХ N05AX13
Фармакологические свойства
Фармакокинетика
Фармакокинетические характеристики палиперидона после приема внутрь являются прямо дозопропорциональными в клиническом диапазоне рекомендуемых доз (3 – 12 мг один раз в сутки).
После приема разовой дозы препарата уровни палиперидона в плазме крови стабильно возрастают, и максимальная концентрация (Cmax) достигается через 24 ч. Стабильная концентрация палиперидона достигается после 4-5 дней приема препарата один раз в сутки.
Особенности высвобождения субстанции из лекарственного препарата Инвега® обеспечивают меньшие флюктуации максимальных и минимальных концентраций палиперидона, чем при использовании обычных лекарственных форм.
После приема палиперидона внутрь, происходит взаимное превращение (+) и (-) энантиомеров, и соотношение площади под фармакокинетической кривой AUC (+)/AUC (-) в равновесном состоянии составляет примерно 1,6. Абсолютная биодоступность палиперидона после перорального приема составляет 28%.
После однократного приема 15 мг Инвега® в виде таблетки пролонгированного действия вместе с жирной высококалорийной пищей Cmax и AUC увеличиваются, в среднем, на 42-60% и 46-54% соответственно относительно этих же показателей при приеме таблетки натощак. Таким образом, наличие или отсутствие в желудке пищи во время приема палиперидона может повысить или снизить концентрацию палиперидона в плазме.
Палиперидон быстро распределяется в тканях и жидкостях организма. Кажущийся объем распределения составляет 487 л. Степень связывания с белками плазмы крови равна 74%. Палиперидон связывается преимущественно с альфа1-кислым гликопротеином и альбумином.
Через 1 неделю после приема одной таблетки (1 мг14С-палиперидона немедленного высвобождения), 59% дозы выделяется с мочой в неизмененном виде, т.е. палиперидон не подвергается интенсивному метаболизму в печени. Около 80% палиперидона выводится с мочой и примерно 11% — через желудочно-кишечный тракт. Известны четыре пути метаболизма палиперидона in vivo, ни один из которых не охватывает более 6,5% дозы: деалкилирование, гидроксилирование, дегидрирование и расщепление бензизоксазола. Ферменты CYP2D6 и CYP3A4 могут играть определенную роль в метаболизме палиперидона, однако нет доказательств того, что эти изоферменты играют значимую роль в метаболизме палиперидона. Не было выявлено существенных различий кажущегося клиренса палиперидона после приема препарата между сильными и слабыми метаболизаторами субстратов CYP2D6. Исследования микросом клеток печени человека in vitro показали, что палиперидон не существенно влияет на метаболизм лекарственных препаратов, метаболизируемых ферментами цитохрома Р450, включая CYP1A2, CYP2A6, CYP2C8/9/10, СYP2D6, CYP2E1, CYP3A4 и CYP3A5. Конечный период полувыведения палиперидона составляет около 23 ч.
Печеночная недостаточность
Палиперидон не подвергается интенсивному метаболизму в печени. В исследовании, в которое включались пациенты, страдавшие печеночной недостаточностью средней степени выраженности (класса B по Чайлд-Пью), концентрации свободного палиперидона в плазме крови были подобны значениям у здоровых добровольцев. Сведения об использовании препарата при тяжелой печеночной недостаточности (класса С по Чайлд-Пью) отсутствуют.
Почечная недостаточность
Дозу палиперидона необходимо снижать у пациентов с умеренным и тяжелым нарушением функции почек. Элиминация палиперидона снижается по мере уменьшения клиренса креатинина. Общий клиренс палиперидона снижен на 32% у пациентов с легкими нарушениями функции почек (клиренс креатинина 50- 80 мл/мин), на 64% у пациентов с умеренными нарушениями функции почек (клиренс креатинина 30- < 50 мл/мин) и на 71% у пациентов с тяжелыми нарушениями функции почек (клиренс креатинина 10-30 мл/мин), средний конечный период полувыведения палиперидона составил 24, 40 и 51 ч у пациентов с легкими, умеренными и тяжелыми нарушениями функции почек соответственно; у людей с нормальной функцией почек (клиренс креатинина ≥80 мл/мин) этот показатель составляет 23 ч.
Пожилые пациенты
Результаты исследования фармакокинетики после приема препарата Инвега® у пациентов пожилого возраста (≥ 65 лет; n = 26) свидетельствуют о снижении на 20% кажущегося равновесного клиренса палиперидона по сравнению с аналогичным значением у более молодых пациентов (в возрасте 18-45 лет; n = 28). Однако, в рамках популяционного фармакокинетического анализа у больных шизофренией, после коррекции по ассоциированному с возрастом снижению клиренса креатинина, очевидного влияния возраста не отмечалось.
Подростки
Системное воздействие палиперидона у пациентов-подростков (15 лет и старше) было сопоставимо с таковым у взрослых. У подростков с массой тела < 51 кг, наблюдалось воздействие на 23% выше, чем у подростков с массой тела ≥ 51 кг. Возраст сам по себе не влияет на экспозицию палиперидона.
Раса
В рамках популяционного анализа фармакокинетики после приема препарата Инвега® не было выявлено доказательств влияния расы на параметры фармакокинетики палиперидона.
Пол
Кажущийся клиренс палиперидона после приема препарата Инвега® был приблизительно на 19% ниже у женщин, нежели у мужчин. Это различие преимущественно было обусловлено различиями в жировой массе тела и клиренса креатинина между представителями различного пола.
Курение
Согласно результатов исследований in vitro с использованием ферментов печени человека, палиперидон не является субстратом CYP1A2; поэтому курение не должно оказывать влияния на фармакокинетику палиперидона. В рамках популяционного анализа фармакокинетики было установлено незначительное снижение экспозиции палиперидона у курящих пациентов по сравнению с некурящими. Маловероятно, что это различие будет иметь клиническое значение.
Таблетки Инвега® производятся с использованием технологии осмотического высвобождения лекарственной субстанции (OROS® — Osmotic controlled Release Oral delivery System), при которой осмотическое давление обеспечивает высвобождение палиперидона с контролируемой скоростью. Система, внешне напоминающая капсуловидную таблетку, состоит из осмотически активного трехслойного ядра, окруженного промежуточной оболочкой и полупроницаемой мембраной. Трехслойное ядро состоит из двух лекарственных слоев, содержащих лекарственную субстанцию и вспомогательные вещества, а также из выталкивающего слоя, содержащего осмотически активные компоненты. На куполе лекарственных слоев имеются два выпускных отверстия, сделанные с помощью лазера. В желудочно-кишечном тракте цветная оболочка быстро растворяется и мембрана пропитывается водой. Мембрана контролирует уровень поступления воды, а это, в свою очередь, контролирует уровень высвобождения лекарственного вещества. Гидрофильные полимеры ядра таблетки впитывают воду и набухают, превращаясь в гель, содержащий палиперидон, который затем выталкивается через отверстия в куполе. Оболочка таблетки, а также нерастворимые компоненты ядра таблетки, выводятся из организма со стулом. Пациенты не должны волноваться, если заметят в стуле что-то похожее на таблетку.
Фармакодинамика
Палиперидон — это антагонист дофаминовых D2-рецепторов центрального действия, а также антагонист серотониновых 5-НТ2-рецепторов, альфа1- и альфа2-адренергических рецепторов и Н1-гистаминовых рецепторов. Палиперидон не обладает аффинитетом к холинергическим, мускариновым, а также бета1- и бета2-адренергическим рецепторам. Фармакологическая активность (+) и (-)-энантиомеров палиперидона одинакова в качественном и количественном отношениях.
Антипсихотическое действие обусловлено блокадой D2-дофаминергических рецепторов мезолимбической и мезокортикальной систем. Палиперидон вызывает меньшее подавление моторной активности и в меньшей степени индуцирует каталепсию, чем классические антипсихотики (нейролептики).
Сбалансированный центральный антагонизм к серотонину и дофамину может уменьшать склонность к экстрапирамидным побочным действиям и расширять терапевтическое воздействие препарата с охватом негативных и продуктивных симптомов шизофрении.
Палиперидон влияет на структуру сна: уменьшает латентный период до засыпания, уменьшает число пробуждений после засыпания, увеличивает общую продолжительность и время периода сна, повышает индекс качества сна. Палиперидон оказывает противорвотное действие, может вызывать увеличение концентрации пролактина в крови.
Показания к применению
— для лечении шизофрении у взрослых и подростков в возрасте от 15 лет и старше
— для лечения психотической или маниакальной симптоматики шизоаффективного расстройства у взрослых.
Влияние препарата на депрессивную симптоматику продемонстрировано не было.
Способ применения и дозы
Инвега® предназначена для приема внутрь независимо от приема пищи. Таблетки Инвега® следует проглатывать целиком, запивая жидкостью, таблетку нельзя разжевывать, делить или разламывать. Лекарственный препарат содержит неабсорбируемую оболочку, предназначенную для высвобождения препарата с контролируемой скоростью. Оболочка таблетки вместе с нерастворимыми компонентами выводится из организма; пациентам не следует беспокоиться, если они обнаружат в стуле что-то напоминающее таблетку.
Необходимо стандартизировать время приема препарата относительно времени приема пищи. Пациент должен быть проинструктирован о том, чтобы всегда принимать таблетку Инвега® натощак или всегда принимать ее во время завтрака, и не чередовать данные варианты приема препарата (т.е. натощак или после еды).
Шизофрения
Взрослые (возраст ≥ 18 лет)
Рекомендуемая доза Инвеги® для лечения шизофрении у взрослых составляет 6 мг один раз в день утром. Титрования дозы в начале лечения не требуется. Для некоторых пациентов подходят более низкие или более высокие дозы в диапазоне от 3 до 12 мг один раз в день. Коррекция дозы, если требуется, должна проводиться только после повторного клинического обследования. При необходимости повышения дозы рекомендуется увеличивать дозировку на 3 мг/день с интервалами не менее 5 дней.
Шизоаффективное расстройство
Взрослые (возраст ≥ 18 лет)
Рекомендуемая доза препарата Инвега® для лечения шизоаффективного расстройства у взрослых составляет 6 мг один раз в день утром. Титрования дозы в начале лечения не требуется. Для некоторых пациентов подходят более высокие дозы в диапазоне от 6 до 12 мг один раз в день. Коррекция дозы, если требуется, должна проводиться только после повторного клинического обследования. При необходимости повышения дозы рекомендуется увеличивать дозировку на 3 мг/день с интервалами не менее 4 дней.
Пациенты с нарушением функции печени
Пациентам с легким или умеренным нарушением функции печени коррекции дозы не требуется. Применение препарата Инвега® у пациентов с тяжелыми нарушениями функции печени не изучалось, следует соблюдать осторожность при применении препарата у таких пациентов.
Пациенты с нарушением функции почек
Для пациентов с легким нарушением функции почек (клиренс креатинина ≥ 50 — < 80 мл/мин) рекомендуемая начальная доза составляет 3 мг один раз в день. Дозу можно увеличить до 6 мг в день на основании клинического ответа и переносимости.
Для пациентов с умеренным и тяжелым нарушением функции почек (клиренс креатинина ≥ 10 — < 50 мл/мин) рекомендуемая доза препарата Инвега® составляет 3 мг один раз в день. Поскольку Инвега® не исследовалась на пациентах с клиренсом креатинина < 10 мл/мин, ее использование у таких пациентов не рекомендуется.
Пациенты пожилого возраста
Для пожилых людей с нормальной функцией почек (≥ 80 мл/мин) рекомендации по дозировкам такие же, что и для взрослых с нормальной функцией почек. Однако, поскольку у пациентов пожилого возраста функция почек может быть снижена, может понадобиться коррекция дозы в зависимости от состояния почек. Препарат Инвега® должен использоваться с осторожностью у пациентов пожилого возраста, страдающих деменцией с наличием факторов риска инсульта. Безопасность и эффективность применения препарата Инвега® у лиц > 65 лет, страдающих шизоаффективным расстройством, не исследовалась.
Применение у детей
Шизофрения: рекомендуемая начальная доза препарата Инвега® для лечения шизофрении у подростков 15 лет и старше составляет 3 мг один раз в день, принятая утром.
Подростки весом <51 кг: максимальная рекомендуемая суточная доза препарата Инвега® составляет 6 мг.
Подростки весом >51 кг: максимальная рекомендуемая суточная доза препарата Инвега® составляет 12 мг.
Коррекция дозы, при наличии показаний, должна осуществляться только после переоценки клинического состояния на основе индивидуальных потребностей пациента. При наличии показания для увеличения дозы, рекомендуется производить увеличение дозы с шагом 3 мг/сутки, и как правило с интервалом 5 дней или более. Эффективность и безопасность препарата Инвега® в лечении шизофрении у подростков в возрасте от 12 до 14 лет не установлена. Соответствующая информация по применению препарата Инвега® у детей младше 12 лет отсутствует.
Шизоаффективное расстройство: безопасность и эффективность применения препарата Инвега® в лечении шизоаффективных расстройств у пациентов в возрасте от 12 до 17 лет не изучалась или не установлена. Данные о соответствующем применении препарата Инвега® у детей младше 12 лет отсутствуют.
Зависимость дозирования препарата Инвега® от пола, расы или курения отсутствует.
Побочные действия
Взрослые
Резюме профиля безопасности
Наиболее частыми побочными действиями, которые наблюдались в клинических исследованиях были: головная боль, бессонница, седация/сонливость, паркинсонизм, акатизия, тахикардия, тремор, дистония, инфекции верхних дыхательных путей, головокружение, увеличение массы тела, тошнота, ажитация, запор, рвота, утомляемость, депрессия, диспепсия, диарея, сухость во рту, зубная боль, скелетно-мышечная боль, гипертония, астения, боль в спине, удлинение интервала QT на электрокардиограмме и кашель.
Следующие побочные действия имели дозозависимую выраженность: головная боль, седация/сонливость, паркинсонизм, акатизия, тахикардия, дистония, головокружение, тремор, инфекции верхних дыхательных путей, диспепсия и скелетно-мышечная боль. В исследованиях шизоаффективных расстройств, большая часть пациентов испытывала побочные действия в группе, которая получала комбинированную терапию препарата Инвега® с антидепрессантами или стабилизаторами настроения, по сравнению с пациентами, получавшими монотерапию препаратом Инвега®.
Табличный перечень побочных действий
Ниже перечислены все побочные действия, которые были отмечены в клинических исследованиях и в процессе постмаркетингового применения палиперидона по категориям частоты, оцененным на основе клинических исследований с препаратом Инвега® у взрослых. Применялись следующие условия и категории частоты встречаемости: очень часто (≥ 1/10), часто (≥ 1/100 до < 1/10), нечасто (≥ 1/1000 до < 1/100), редко (≥ 1/10 000 до < 1/1000), очень редко (< 1/10 000) и частота неизвестна (невозможно определить по результатам клинических исследований). В рамках каждой категории частоты побочные действия перечислены в порядке снижения степени серьезности.
|
Класс систем и органов |
Нежелательная лекарственная реакция |
||||
|
Частота |
|||||
|
Очень часто |
Часто |
Нечасто |
Редко |
Частота не известна |
|
|
Инфекции и инвазии |
бронхит, инфекции верхних дыхательных путей, синусит, инфекции мочевыводя-щих путей, грипп |
пневмония, инфекции дыхательных путей, синусит, инфекции уха, тонзилит |
инфекции глаз, онихомикоз, целлюлит, акродерматит |
||
|
Нарушения со стороны кроветвор-ной и лимфа-тической системы |
снижение количества белых кровяных телец, тромбоцито-пения, анемия, снижение гематокрита |
агранулоцитозс нейтропения, увеличение количества эозинофилов |
|||
|
Нарушения со стороны иммунной системы |
анафилактичес-кие реакции, гиперчувст-вительность |
||||
|
Нарушения со стороны эндокринной системы |
гиперпролак-тинемияa |
неадекватная выработка антидиуретического гормонас, присутствие глюкозы в моче |
|||
|
Нарушения метаболизма и обмена веществ |
увеличение массы тела, повышение аппетита, снижение массы тела, снижение аппетита |
сахарный диабетd, гиперглике-мия, увеличение окружности талии, анорексия, увеличение триглицери-дов в крови |
водная интоксикация, диабетический кетоацидозс, гипогликемия, полидипсия, увеличение холестерина в крови |
гиперин-сулинемия |
|
|
Психические нарушения |
бессонницас |
мания, ажитация, депрессия, тревога |
нарушение сна, спутанность сознания, снижение либидо, аноргазмия, нервозность, ночные кошмары |
аффективная уплощенностьс |
|
|
Нарушения со стороны нервной системы |
паркинсо-низмb, акатизияb, седация/ сонливость, головная боль |
дистонияb, головокруже-ние, дискинезияb, треморb |
поздняя дискинезия, судорогие, обморок, психомотор-ная гиперак-тивность, постуральное головокруже-ние, нарушение внимания, дизартрия, дисгевзия, гипестезия, парестезия |
злокачествен-ный нейролеп-тический синдром, церебральная ишемия, отсутствие реакии на раздражителис, потеря сознания,сни-жение уровня сознанияс, диабетическая комас, нарушение равновесия, нарушение координации, покачивающие движения головыс |
|
|
Нарушения со стороны органа зрения |
нечеткость зрения |
светобоязнь, конъюнкти-вит, сухость глаз |
глаукома, нарушение движения глазного яблокас, круговые движения глазного яблокас, увеличение слезоточивости, гиперемия глаз |
||
|
Нарушения со стороны слухового аппарата и внутреннего уха |
вертиго, шум в ушах, боль в ухе |
||||
|
Кардиологи-ческие нарушения |
атриовентри-кулярная блокада, нарушение проводимости, удлинение интервала QT на электрокар-диограмме, брадикардия, тахикардия |
синусовая аритмия, нарушения на электрокар-диограмме, учащенное сердцебиение |
фибрилляция предсердий, синдром постуральной ортостатичес-кой тахикардиис |
||
|
Нарушения со стороны сосудистой системы |
ортостатичес-кая гипотензия, гипертензия |
гипотензия |
эмболия легочной артерии, тромбоз вен, ишемия, гиперемия |
||
|
Респиратор-ные, тора-кальные и медиасти-нальные нарушения |
фаринголарин-геальная боль, кашель, заложенность носа |
одышка, свистящее дыхание, носовое кровотечение |
синдром апноэ во сне, гипервентиля-ция легких, аспирационная пневмония, заложенность дыхательных путей, дисфония |
застой в легких |
|
|
Нарушения со стороны пищевари-тельной системы |
боль в животе, дискомфорт в животе, рвота, тошнота, запор, диарея, диспепсия, сухость во рту, зубная боль |
отек языка, гастроэнтерит, дисфагия, метеоризм |
панкреатитс, непроходимость кишечника, илеус, недержание кала, фекаломас, хейлит |
||
|
Нарушения со стороны гепато-билиарной системы |
повышение содержания трансаминаз |
увеличение количества гаммаглута-милтрансфе-раз, увеличение количества печеночных ферментов |
желтуха |
||
|
Нарушения со стороны кожи и подкожной клетчатки |
зуд, сыпь |
крапивница, алопеция, экзема, акне |
ангионевроти-ческий отек, лекарственная сыпьс, гиперкератоз, сухость кожи, эритема, изменение цвета кожи, себорейный дерматит, перхоть |
||
|
Нарушения со стороны скелетно-мышечной системы и соединительной ткани |
скелетно-мышечная боль, боль в спине, артралгия |
увеличение креатин фосфокиназы в крови, мышечные спазмы, тугоподвиж-ность суставов, отечность суставов, мышечная слабость, боль в шее |
рабдомиолизс, нарушение осанкис |
||
|
Нарушения со стороны почек и мочевыводя-щей системы |
недержание мочи, поллакиурия, задержка мочи, дизурия |
||||
|
Осложнения беременнос-ти, послеро-дового и перинаталь-ного периода |
синдром отмены препарата у новорожденныхс |
||||
|
Нарушения со стороны репродуктив-ной системы и молочной железы |
аменорея |
эректильная дисфункция, нарушение эякуляции, нарушение менструально-го циклае, галакторея, сексуальная дисфункция, болезненность молочных желез, дискомфорт молочных желез |
приапизмс, задержка менструального циклас, гинекомастия, нагрубание молочных желез, увеличение грудис, выделения из сосков, вагинальные выделения |
||
|
Общие нарушения |
пирексия, астения, утомляемость |
отек лица, отеке, озноб, увеличение температуры тела, нарушение походки, жажда, боль в груди, дискомфорт в груди, недомогание |
гипотермияс, снижение температуры телас, синдром отмены препаратас, уплотненияс |
||
|
Травмы, отравления и процедурные осложнения |
слабость |
a Смотрите информацию, описанную ниже в пункте «Гипергликемия».
b Смотрите информацию, описанную ниже в пункте «Экстрапирамидные расстройства».
с Не наблюдались в клинических исследованиях с препаратом Инвега®, но обнаруживались при пост-маркетинговом применении палиперидона
d В плацебо-контролируемых пилотных исследованиях, сахарный диабет наблюдался у 0,05% пациентов в группе Инвега® по сравнению с 0% в группе плацебо. Общее количество сообщений о сахарном диабете, полученных из всех клинических испытаний при терапии препаратом Инвега®, составило 0,14%.
е Бессонница включает: нарушение засыпания, интрасомническое расстройство; Судороги включают: большой судорожный припадок; Отеки включают: генерализованнный отек, периферический отек, точечный отек. Нарушения менструального цикла включают: нерегулярные менструации, олигоменорею
Нежелательные реакции, наблюдавшиеся при применении рисперидона
Палиперидон является активным метаболитом рисперидона, поэтому, профили неблагоприятных реакций этих веществ (включая как пероральные и так и инъекционные формы) сопоставимы друг с другом. В дополнение к указанным выше побочных реакциям, следующие побочных реакции, отмеченные с использованием рисперидона, могут проявляться и при применении препарата Инвега®.
Расстройства нервной системы: цереброваскулярные нарушения
Нарушения со стороны глаз: синдром дряблой радужки (интраоперационный)
Респираторные, торакальные и медиастинальные нарушения: хрипы
Описание отдельных нежелательных реакций
Экстрапирамидные нарушения
В клинических исследованиях использования препарата при шизофрении не наблюдались различия касательно экстрапирамидных нарушений между группой, применявшей плацебо и группой, применявшей препарат Инвега® в дозах 3 мг и 6 мг. Дозозависимость экстрапирамидных нарушений наблюдалась при использовании препарата Инвега® в двух более высоких дозах (9 мг и 12 мг). В исследованиях использования препарата при шизоаффективном расстройстве частота экстрапирамидных нарушений была выше, по сравнению с группой плацебо, при использовании препарата во всех дозах, при этом очевидной дозозависимости не наблюдалось.
В объединенный анализ экстрапирамидных нарушений были включены следующие термины: паркинсонизм (включает гиперсекрецию слюны, ригидность опорно-двигательного аппарата, паркинсонизм, слюнотечение, ригидность по типу «зубчатого колеса», брадикинезию, гипокинезию, маскообразное лицо, мышечное напряжение, акинезию, ригидность затылочных мышц, ригидность мышц, паркинсоническую походку и нарушение глабеллярного рефлекса, паркинсонический тремор рук), акатизия (включает акатизию, беспокойство, гиперкинезию и синдром беспокойных ног), дискинезия (дискинезия, подергивание мышц, хореоатетоз, атетоз и миоклонус), дистония (включает дистонию, гипертонию, кривошею, непроизвольные мышечные сокращения, контрактуры мышц, блефароспазм, круговые движения глазного яблока, паралич языка, лицевой спазм, ларингоспазм, миотонию, опистотонус, спазм ротоглотки, изгиб туловища в сторону большего сокращения мышц, спазм языка, тризм) и тремор. Следует отметить, что выше приведен более широкий спектр симптомов, которые не всегда имеют экстрапирамидное происхождение.
Увеличение массы тела
В клинических исследованиях использования препарата при шизофрении доли пациентов, у которых отмечалось увеличение массы тела на ≥ 7%, были сравнимы на фоне терапии препаратом Инвега® (в дозах 3 мг и 6 мг) и плацебо; однако на фоне терапии препаратом Инвега® в дозах 9 мг и 12 мг частота увеличения массы тела была выше, нежели в группе плацебо.
В клинических исследованиях использования препарата при шизоаффективном расстройстве у большей доли пациентов, получавших препарат Инвега® (5%) отмечалось увеличение массы тела на ≥ 7% по сравнению с пациентами, получавшими плацебо (1%). В исследовании, в котором имелось две группы терапии активным препаратом в различных дозах, частота увеличения массы тела на ≥ 7% составляла 3% в группе терапии препаратом в низкой дозе (3-6 мг) и 7% в группе терапии препаратом в высокой дозе (9-12 мг) (по сравнению с 1% в группе плацебо).
Гиперпролактинемия
В клинических исследованиях использования препарата при шизофрении повышение концентрации пролактина в сыворотке крови наблюдалось на фоне терапии препаратом Инвега® у 67% пациентов. Нежелательные явления, которые могут соответствовать повышению концентрации пролактина (в частности, аменорея, галакторея, гинекомастия) отмечались, в общей сложности, у 2% пациентов. Максимальное среднее повышение концентрации пролактина в сыворотке крови обычно наблюдалось на 15-ый день терапии, однако до конца исследования показатель продолжал превышать исходный уровень.
Класс-специфические эффекты
На фоне терапии нейролептиками могут развиваться удлинение интервала QT, желудочковые аритмии (фибрилляция желудочков, желудочковая тахикардия), внезапная смерть, остановка сердца и двунаправленная желудочковая тахикардия. Кроме того, при использовании нейролептиков описаны случаи развития венозных тромбоэмболий, в том числе тромбоэмболии легочной артерии и тромбоза глубоких вен (частота данных нежелательных явлений не известна).
Палиперидон является активным метаболитом рисперидона. Поэтому сведения о безопасности последнего могут иметь отношение и к палиперидону.
Применение в пожилом возрасте
В исследовании, в которое были включены пациенты пожилого возраста, страдавшие шизофренией, безопасность препарата была аналогичной таковой при его использовании у больных более молодого возраста. Использование препарата Инвега® у лиц пожилого возраста, страдавших деменцией, не исследовалось. В клинических исследованиях некоторых других атипичных нейролептиков было констатировано о повышении риска смерти и инсульта.
Педиатрическая популяция
Краткое описание профиля безопасности
В одном краткосрочном и двух долгосрочных исследованиях использования таблеток палиперидона пролонгированного высвобождения для лечения шизофрении у подростков 12 лет и старше, общий профиль безопасности был сравним с таковым у взрослых. В общем пуле подростковых пациентов (12 лет и старше, N = 545), подвергшихся лечению препаратом Инвега®, частота и типы нежелательных эффектов были аналогичны таковым у взрослых, за исключением следующих нежелательных явлений, которые чаще наблюдались у подростков, принимавших лечение препаратом Инвега®, нежели у взрослых, принимавших лечение препаратом Инвега® (и чаще, чем в группе плацебо): у подростков проявлялись очень часто (≥ 1/10) заторможенность/сонливость, паркинсонизм, увеличение веса, инфекции верхних дыхательных путей, акатизия и тремор; и часто (≥ 1/100, <1/10) у подростков проявлялись боль в животе, галакторея, гинекомастия, угревая сыпь, дизартрия, гастроэнтерит, носовое кровотечение, инфекции уха, увеличение триглицеридов в крови и головокружение.
Экстрапирамидные симптомы (EPS)
В краткосрочном плацебо-контролируемом исследовании у подростков, с приемом фиксированной дозы, заболеваемость EPS была выше, в группах принимавших препарат Инвега® для всех доз по сравнению с плацебо, с тенденцией повышения частоты проявления EPS в группах, принимавших более высокие дозы. Во всех исследованиях, проведенных у подростков со всеми дозами препарата Инвега®, EPS чаще наблюдалось у подростков, нежели у взрослых.
Увеличение массы тела
В краткосрочном плацебо-контролируемом исследовании у подростков с приемом фиксированной дозы, более высокий процент увеличения массы тела (≥ 7%) наблюдался в группе, принимавшей препарат Инвега® (от 6 до 19% в зависимости от дозы) по сравнению с группой пациентов, принимавшей плацебо (2%). Четкой взаимосвязи с принимаемой дозой не обнаружено. В долгосрочном 2-годичном исследовании, у испытуемых, которые подверглись терапии препаратом Инвега® во время обоих, двойного слепого и открытого, исследований наблюдался умеренный набор веса (4,9 кг).
У подростков следует оценивать увеличение массы тела по сравнению с ожидаемым при нормальном росте.
Пролактин
В 2-годичном открытом исследовании лечения шизофрении у подростков препаратом Инвега®, случаи повышения уровня сывороточного пролактина наблюдались у 48% подростков женского пола и 60% мужского пола. Побочные реакции, которые позволяют предположить о повышении уровня пролактина (например, аменорея, галакторея, нарушения менструального цикла, гинекомастия) были зарегистрированы в целом у 9,3% испытуемых.
Противопоказания
— гиперчувствительность к активному веществу препарата, рисперидону или любому из вспомогательных веществ
— беременность и период лактации
— детский и подростковый период до 15 лет (шизофрения)
— детский и подростковый период до 18 лет (шизоаффективное расстройство)
Лекарственные взаимодействия
Следует соблюдать осторожность при одновременном применении препарата Инвега® с препаратами, удлиняющими интервал QT, например, антиаритмическими средствами IA класса (например, хинидином и дизопирамидом) и III класса (например, амиодароном и соталолом), некоторыми антигистаминными средствами, рядом других нейролептиков и некоторыми противомалярийными препаратами (например, мефлохином).
Влияние препарата Инвега® на другие препараты
В высоких концентрациях палиперидон является слабым ингибитором Р-гликопротеина. Клиническая значимость неизвестна.
Так как палиперидон действует преимущественно на ЦНС, его необходимо с осторожностью использовать в комбинациях с другими препаратами центрального действия и с алкоголем. Инвега® может нейтрализовать действие леводопы и других агонистов допамина. Если такое комбинирование расценивается как необходимое, в особенности при терминальных стадиях болезни Паркинсона, необходимо использовать минимальные эффективные дозы всех комбинируемых препаратов.
Вследствие способности препарата Инвега® вызывать ортостатическую гипотензию возможно возникновение аддитивного эффекта при использовании препарата одновременно с другими препаратами, вызывающими ортостатическую гипотензию (включая другие антипсихотические средства, трициклические антидепрессанты).
Рекомендуется соблюдать осторожность при комбинировании палиперидона с другими лекарственными средствами, которые, как известно, снижают судорожный порог (например, фенотиазинами или бутирофенонами, клозапином, трициклическими антидепрессантами или селективными ингибиторами обратного захвата серотонина, трамадолом, мефлохином и т.д.).
Исследований лекарственного взаимодействия между препаратом Инвега® и препаратами лития не проводилось, однако вероятность фармакокинетических взаимодействий между данными средствами представляется маловероятной.
Комбинирование препарата Инвега® (в дозе 12 мг, 1 раз в сутки) с фиксированной комбинацией вальпроата натрия и вальпроевой кислоты в виде таблеток пролонгированного высвобождения (в дозе 500 мг ‑ 2000 мг, 1 раз в сутки) не изменяло параметры фармакокинетики вальпроата в равновесном состоянии. Однако при таком комбинировании препарата Инвега® отмечалось увеличение значений экспозиции палиперидона (см. ниже).
Способность других препаратов влиять на препарат Инвега®
Палиперидон не является субстратом изоферментов CYP1А2, CYP2А6, CYP2С9, CYP2С19 и CYP3А5. Поэтому вероятность его взаимодействия с ингибиторами или индукторами указанных ферментов низкая. Нет доказательств того, что изоферменты CYP2D6 и CYP3А4 играют значимую роль в метаболизме палиперидона. Применение препарата Инвега® одновременно с пароксетином не влияет на фармакокинетику палиперидона.
Применение препарата Инвега® одновременно с 200 мг карбамазепина два раза в сутки вызывает уменьшение Сmax и AUC палиперидона примерно на 37%, так как, в результате индукции карбамазепином почечного Р-гликопротеина, клиренс палиперидона увеличивается на 35%. Небольшое снижение экскреции активного вещества в неизмененном виде с мочой позволяет предположить, что карбамазепин оказывает лишь незначительное влияние на метаболизм CYP или биодоступность палиперидона. Большее снижение плазменных концентраций палиперидона может наблюдаться при применении более высоких доз карбамазепина. При одновременном назначении с карбамазепином следует пересмотреть и, при необходимости, увеличить дозу препарата Инвега®. И наоборот, при отмене карбамазепина дозу препарата Инвега® следует пересмотреть и, при необходимости, снизить.
Полная индукция достигается в течение 2-3 недель, и после отмены индуктора действие заканчивается в течение аналогичного периода времени. Другие лекарственные средства или растительные препараты, являющиеся индукторами, например, рифампицин и St. Joh’s wort (Hypericum perforatum – зверобой продырявленный) могут оказывать подобные эффекты на палиперидон.
Лекарственные средства, оказывающие влияние на длительность транзита по кишечнику, например, метоклопрамид, могут оказывать влияние на абсорбцию палиперидона.
При одновременном назначении препарата Инвега® в дозировке 12 мг 1 раз в день и таблеток пролонгированного высвобождения натрия дивалпроекса (2 таблетки по 500 мг 1 раз в день) наблюдалось увеличение Cmax и AUC палиперидона на 50%. При одновременном назначении препарата Инвега® с вальпроатом, следует рассмотреть возможность снижения дозы препарата Инвега® на основании клинической оценки пациента.
Одновременное использование палиперидона и рисперидона
Не рекомендуется совместное применение препарата Инвега® и перорального рисперидона, поскольку палиперидон является активным метаболитом рисперидона и при их совместном применении возможно повышение уровней палиперидона в крови.
Педиатрическая популяция
Исследования лекарственного взаимодействия проводились только у взрослых пациентов.
Особые указания
Пациенты с шизоаффективным расстройством, получающие палиперидон, должны тщательно контролироваться на предмет потенциальной трансформации маниакальной симптоматики в депрессивную.
Злокачественный нейролептический синдром
При использовании палиперидона были получены сообщения о проявлении злокачественного нейролептического синдрома (ЗНС), характеризующегося развитием гипертермии, ригидности мышц, автономной нестабильности, изменением состояния сознания и повышением активности креатинфосфокиназы в сыворотке крови. Дополнительными клиническими проявлениями могут являться миоглобинурия (рабдомиолиз) и острая почечная недостаточность. При возникновении у пациента объективных или субъективных симптомов ЗНС необходимо немедленно отменить все антипсихотические препараты, включая препарат Инвега®.
Поздняя дискинезия
Препараты, обладающие свойствами антагонистов дофаминовых рецепторов, могут вызывать позднюю дискинезию, которая характеризуется ритмическими непроизвольными движениями, преимущественно языка и/или мимической мускулатуры. При возникновении у пациента объективных или субъективных симптомов, указывающих на позднюю дискинезию, нужно рассмотреть целесообразность отмены всех антипсихотических препаратов, включая препарат Инвега®.
Удлинение интервала QT
Как и для других антипсихотических средств, следует соблюдать осторожность при назначении препарата Инвега® пациентам с сердечными аритмиями в анамнезе, врожденным удлинением интервала QT и совместном применении с препаратами, удлиняющими интервал QT.
Гипергликемия и сахарный диабет
При лечении препаратом Инвега® наблюдалось проявление гипергликемии, сахарного диабета и обострение уже имеющегося сахарного диабета. В некоторых случаях, регистрировались случаи первоначального увеличения массы тела, которое могло стать предрасполагающим фактором. Были получены сообщения об очень редких случаях кетоацидоза и редких случаях диабетической комы, в связи с применением палиперидона. Рекомендуется проводить надлежащий клинический мониторинг в соответствии с используемыми руководствами по применению нейролептиков. Пациенты, принимающие лечение любым из атипичных нейролептиков, включая препарат Инвега®, должны наблюдаться на предмет появления симптомов гипергликемии (таких как, полидипсия, полиурия, полифагия и слабость), и пациенты с сахарным диабетом должны регулярно наблюдаться на предмет ухудшения контроля уровня глюкозы.
Увеличение массы тела
При лечении атипичными антипсихотиками наблюдалось значительное увеличение массы тела. Необходимо проводить контроль массы тела пациентов.
Гиперпролактинемия
Исследования культуры ткани показывают, что рост клеток опухолей молочной железы человека может стимулироваться пролактином. Хотя клинические и эпидемиологические исследования не показали пока четкой взаимосвязи с примененением антипсихотических препаратов, рекомендуется соблюдать осторожность у пациентов с соответствующим анамнезом. Палиперидон следует использовать с осторожностью у больных с возможными пролактин-зависимыми опухолями.
Ортостатическая гипотензия
Инвега® обладает альфа-блокирующей активностью, и поэтому может вызывать у некоторых пациентов ортостатическую гипотензию. Препарат Инвега® необходимо с осторожностью применять у пациентов с сердечно-сосудистыми заболеваниями (например, сердечная недостаточность, инфаркт или ишемия миокарда, нарушения проводимости сердечной мышцы), цереброваскулярными заболеваниями, а также с состояниями, способствующими артериальной гипотензии (например, обезвоживание, гиповолемия и терапия антигипертензивными препаратами).
Судороги
Как и другие антипсихотики, препарат Инвега® следует с осторожностью применять у пациентов, имеющих в анамнезе судорожные припадки или другие заболевания, снижающие порог судорожной готовности.
Риск обструкции желудочно-кишечного тракта
Поскольку таблетки Инвега® не изменяют в значительной мере свою форму при прохождении по желудочно-кишечному тракту, препарат Инвега® не следует назначать больным с выраженным сужением пищеварительного канала (патологическим или ятрогенным), а также пациентам с дисфагией или больным, испытывающим существенные затруднения при проглатывании таблеток. Учитывая лекарственную форму с контролируемым высвобождением, препарат Инвега® должны принимать только пациенты, которые способны проглатывать таблетку целиком.
Пожилые пациенты, страдающие деменцией
Терапия препаратом Инвега® не изучалась в популяции пожилых пациентов, страдающих деменцией.
Опыт применения рисперидона расценивается как применимый также и для палиперидона.
Общая летальность
В рамках мета-анализа 17 контролируемых клинических исследований у пациентов пожилого возраста, страдавших деменцией, получавших другие атипичные нейролептики, в том числе рисперидон, арипипразол, оланзапин и кветиапин, было констатировано повышение летальности по сравнению с плацебо. У пациентов, получавших рисперидон, летальность составляла 4% по сравнению с 3,1% в группе плацебо.
Цереброваскулярные нежелательные реакции
В рамках рандомизированных, плацебо-контролируемых клинических исследований у больных деменцией применение некоторых атипичных нейролептиков, в том числе рисперидона, арипипразола и оланзапина, ассоциировалось с повышением риска цереброваскулярных нежелательных реакций приблизительно в 3 раза. Механизм данного повышения риска не известен. Препарат Инвега® должен использоваться с осторожностью у лиц пожилого возраста, страдающих деменцией и имеющих факторы риска инсульта.
Регуляция температуры тела
Антипсихотическим препаратам приписывается такой нежелательный эффект как нарушение способности организма регулировать температуру. Необходимо соблюдать осторожность при назначении препарат Инвега® пациентам с состояниями, которые могут способствовать повышению внутренней температуры тела, к которым относятся интенсивная физическая нагрузка, обезвоживание организма, воздействие высоких внешних температур или одновременное использование препаратов с антихолинергической активностью.
Противорвотный эффект
В доклинических исследованиях с палиперидоном наблюдалось проявление у него противорвотного эффекта. Этот эффект, в случае его возникновения у людей, может маскировать объективные и субъективные симптомы передозировки определенных препаратов, а также такие состояния, как непроходимость кишечника, синдром Рейе и опухоли головного мозга.
Интраоперационный синдром дряблой радужки
Интраоперационный синдром дряблой радужки (IFIS) был отмечен при хирургических операциях по удалению катаракты у пациентов, получавших лекарственные средства с эффектом антагонистов альфа1а-адренорецепторов, включая препарат Инвега®.
IFIS может увеличивать риск осложнений со стороны глаз в течение и после операции. Информация о текущем и предшествующем использовании лекарственных препаратов с эффектом антагонистов альфа1а-адренорецепторов должна быть предоставлена офтальмохирургу до начала операции. Потенциальные преимущества прекращения альфа1-блокирующей терапии перед операцией по удалению катаракты не были определены, и их следует оценивать с учётом риска прекращения терапии нейролептиками.
Болезнь Паркинсона и деменция с тельцами Леви
При назначении антипсихотических препаратов, включая препарат Инвега®, пациентам, страдающим болезнью Паркинсона или деменцией с тельцами Леви (ДТЛ), необходимо тщательно взвешивать потенциальные пользу и риск терапии, поскольку для пациентов с такой патологией характерен высокий риск развития злокачественного нейролептического синдрома, а также повышенная чувствительность к антипсихотическим препаратам. Повышенная восприимчивость к антипсихотическим препаратам может проявляться нарушениями сознания, оглушением, неустойчивостью с частыми падениями, а также экстрапирамидной симптоматикой.
Приапизм
Препараты, обладающие альфа-адреноблокирующими эффектами, могут вызывать приапизм. В постмаркетинговых исследованиях палиперидона были получены сообщения о развитии приапизма. Пациенты должны быть проинформированы о необходимости обращения за экстренной медицинской помощью в случае развития приапизма, не разрешающегося в течение 3-4 часов.
Суицидальные попытки
Возможность суицидальных попыток характерна для психических заболеваний, поэтому терапия пациентов с высоким риском должна проводиться под тщательным наблюдением. В этих случаях препарат Инвега® должен выписываться в минимальном количестве таблеток для уменьшения риска передозировки.
Лейкопения, нейтропения, агранулоцитоз
Лейкопения, нейтропения и агранулоцитоз отмечались при применении антипсихотических средств, в том числе при применении препарата Инвега®. Агранулоцитоз отмечался очень редко в течение постмаркетинговых наблюдений. Пациентам, с клинически значимым уменьшением количества лейкоцитов в анамнезе или препарат-зависимой лейкопенией/нейтропенией рекомендуется проведение полного анализа крови в течение первых месяцев терапии, прекращение лечения препаратом Инвега® должно быть рассмотрено при первом клинически значимом уменьшении количества лейкоцитов при отсутствии других возможных причин. Пациентам с клинически значимой нейтропенией рекомендуется наблюдаться на предмет повышения температуры или возникновения симптомов инфекции и начинать лечение немедленно, при возникновении таких симптомов. Пациенты с тяжелой формой нейтропении (абсолютное количество нейтрофилов менее 1 х 109/л) должны прекратить применение препарата Инвега® до тех пор пока количество лейкоцитов не нормализуется.
Венозные тромбоэмболии
При применении антипсихотических препаратов были отмечены случаи венозной тромбоэмболии. Поскольку пациенты, принимающие антипсихотические препараты, часто имеют риск развития венозной тромбоэмболии, все возможные факторы риска должны быть выявлены до и во время лечения препаратом Инвега® и должны быть предприняты соответствующие предупреждающие меры.
Условия, приводящие к сокращению времени транзита препарата в ЖКТ
Условия, приводящие к сокращению времени транзита препарата в ЖКТ, например, болезни, связанные с хронической диареей, могут привести к снижению всасывания палиперидона.
Нарушение функции почек
Концентрация палиперидона в плазме крови возрастала у пациентов, страдающих нарушением функции почек, что в некоторых случаях может потребовать коррекции дозы препарата. Данные об использовании препарата у пациентов, имеющих значения клиренса креатинина ниже 10 мл/минуту, отсутствуют. Палиперидон не должен использоваться у пациентов с клиренсом креатинина ниже 10 мл/минуту.
Нарушение функции печени
Данные об использовании препарата у пациентов, страдающих тяжелой печеночной недостаточностью (класса С по Чайлду-Пью) отсутствуют. Следует соблюдать осторожность при применении препарата у данной категории пациентов.
Подростки и дети
Следует тщательно контролировать седативное действие препарата Инвега® в этой группе пациентов. Изменение времени приема препарата Инвега® может снизить воздействие седативного эффекта на пациента.
Из-за возможных эффектов длительной гиперпролактинемии на рост и половое созревание у подростков, следует рассматривать необходимость регулярной клинической оценки эндокринологического статуса, в том числе измерение роста, веса, полового созревания, мониторинг менструального функционирования, и других потенциальных пролактин-связанных эффектов.
Во время лечения препаратом Инвега® следует проводить регулярное обследование на предмет экстрапирамидных симптомов и других двигательных расстройств.
Содержание лактозы (имеет отношение только к таблеткам по 3 мг)
Пациенты, страдающие редкими врожденными нарушениями метаболизма, в частности непереносимостью галактозы, врожденной недостаточностью лактазы или синдромом мальабсорбции глюкозы и галактозы, не должны принимать этот препарат.
Беременность и лактация
В настоящее время нет данных о безопасности применения препарата Инвега® у беременных женщин и внутриутробного развития плода. Препарат не следует назначать беременным женщинам. Влияние препарата Инвега® на родовую деятельность женщин не известно. В случае если женщина принимала антипсихотические препараты (включая препарат Инвега®) в третьем триместре беременности, у новорожденных существует риск возникновения экстрапирамидных расстройств и/или синдрома отмены различной степени тяжести. Эти симптомы могут включать ажитацию, гипертонию, гипотонию, тремор, сонливость, респираторные нарушения и нарушение вскармливания.
Инвега® проникает в грудное молоко, в связи с этим препарат не следует назначать в период лактации.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Инвега® может нарушать деятельность, требующую быстрой психической реакции, и влиять на зрение, поэтому пациентам следует воздерживаться от управления транспортным средством и работы с потенциально опасными механизмами до тех пор, пока не будет установлена их индивидуальная чувствительность к препарату Инвега®.
Передозировка
Симптомы: в целом, объективные и субъективные симптомы передозировки палиперидона представляют собой усиленные фармакологические эффекты этого лекарственного средства, т. е. сонливость и седацию, тахикардию и артериальную гипотензию, удлинение интервала QT и экстрапирамидные симптомы. Двунаправленная тахикардия и фибрилляция желудочков наблюдалась при передозировке пероральным палиперидоном. При острой передозировке необходимо учитывать возможность токсического действия нескольких препаратов.
Лечение: при оценке терапевтических потребностей пациента и эффективности купирования передозировки необходимо помнить о том, что Инвега® является препаратом с пролонгированным высвобождением лекарственной субстанции. Специфического антидота палиперидона не существует. Необходимо осуществлять общепринятые поддерживающие меры. Следует обеспечить и поддерживать хорошую проходимость дыхательных путей, а также адекватную оксигенацию и вентиляцию. Необходимо сразу же организовать мониторинг сердечно-сосудистой деятельности (ЭКГ-мониторинг с целью выявления возможных аритмий). Артериальную гипотензию и коллаптоидные состояния купируют внутривенным введением плазмозамещающих растворов и/или симпатомиметических средств. В определенных ситуациях показано промывание желудка (после интубации, если пациент находится в бессознательном состоянии), введение активированного угля и слабительных средств. При возникновении тяжелых экстрапирамидных симптомов необходимо вводить антихолинергические препараты. Наблюдение за состоянием пациента и мониторинг основных физиологических функций необходимо продолжать до полного устранения последствий передозировки.
Форма выпуска и упаковка
По 7 таблеток в контурной ячейковой упаковке из алюминия и поливинилхлорида, ламинированного полихлоротрифторэтиленом. По 4 контурных ячейковых упаковок вместе с инструкцией по медицинскому применению на государственном и русском языках в картонной пачке. Дополнительно может быть контроль первого вскрытия в виде наклеек (по одной с 2-х сторон картонной пачки).
Условия хранения
Хранить при температуре не выше 30°С. Хранить в оригинальной упаковке для защиты от влаги. Хранить в недоступном для детей месте!
Срок хранения
2 года
Не использовать по истечении срока годности препарата.
Условия отпуска из аптек
По рецепту
Производитель
Янссен Силаг Мануфэкчуринг ЛЛС, Пуэрто-Рико
Упаковщик
Янссен-Силаг С.п.А., Италия
Владелец Регистрационного удостоверения
ООО Джонсон & Джонсон, Россия
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара)
филиал ООО «Джонсон & Джонсон» в Республике Казахстан
050040, г. Алматы, ул. Тимирязева, 42, павильон № 23 «А»
Тел.: +7 (727) 356 88 11
е-mail: DrugSafetyKZ@its.jnj.com
| 291898521477976984_ru.doc | 215.5 кб |
| 571114991477978151_kz.doc | 229.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Состав
В 1 таблетке палиперидона 3, 6, 9 или 12 мг. Макрогол, натрия хлорид, повидон, гиэтеллоза, кислота стеариновая, бутилгидрокситолуол, железа оксид желтый и красный, макрогол, ацетат целлюлозы, краситель, воск карнаубский, как вспомогательные компоненты.
Форма выпуска
Таблетки в оболочке пролонгированного действия 3 мг, 6 мг, 9 мг и 12 мг.
Фармакологическое действие
Нейролептическое.
Фармакодинамика и фармакокинетика
Фармакодинамика
Антагонист дофаминовых D2-рецепторов и серотониновых 5-НТ2. Антипсихотическое действие связано с блокадой D2-дофаминовых рецепторов. По сравнению с классическими нейролептиками меньше подавляет двигательную активность и провоцируют каталепсию.
Устраняет негативные и продуктивные симптомы шизофрении, при этом почти не вызывает экстрапирамидных побочных реакций. Оказывает влияние на сон: уменьшает период до засыпания, число пробуждений, увеличивает продолжительность и качество сна. Вызывает увеличение уровня пролактина в крови. Оказывает умеренное противорвотное действие.
Фармакокинетика
При приеме одной дозы концентрация действующего вещества в крови возрастает и достигает максимума через сутки. Равновесные концентрации достигаются через 4–5 дней регулярного приема. Палиперидон — активный метаболит рисперидона. Его особенности высвобождения обеспечивают меньшие колебания концентраций палиперидона.
Быстро распределяется в тканях, на 74% связывается с белками крови. Через неделю после приема одной таблетки 59% выделяется с мочой. Не подвергается метаболизму в печени, поэтому выделяется в неизмененном виде. Исследованиями in vitro показано, что изоферменты цитохрома Р450 играют определенную роль в метаболизме, но не значимую. Период полувыведения — 23 часа.
Поскольку активное вещество не подвергается метаболизму в печени, то снижать дозу у больных с умеренными нарушениями функции печени не надо. Однако доза должна быть снижена при тяжелых нарушениях функции почек. Фармакокинетика палиперидона у подростков сравнима с таковой у взрослых.
Показания к применению
- профилактика обострений и лечение шизофрении у взрослых пациентов;
- лечение шизофрении у подростков;
- шизоаффективные расстройства.
Противопоказания
- повышенная чувствительность;
- беременность (только по жизненным показаниям);
- период кормления грудью.
С осторожностью назначается препарат при судорожных состояниях, дисфагии, старческой деменции (возможны цереброваскулярные побочные эффекты), болезни Паркинсона в связи с риском экстрапирамидных расстройств.
Побочные действия
Часто встречающиеся побочные реакции:
- назофарингит;
- бессонница, мания;
- увеличение веса;
- головная боль;
- мышечная боль;
- тошнота, дискомфорт в животе, диарея или запор, повышенный аппетит;
- акатизия, дизартрия;
- паркинсонизм, повышение тонуса мышц;
- сонливость;
- слюнотечение.
Нечасто встречающиеся побочные реакции:
- цистит;
- инфекции уха, бронхит, синусит, тонзиллит;
- анафилактическая реакция;
- анемия, нейтропения, лейкопения;
- гиперпролактинемия;
- анорексия, гипогликемия и гипергликемия;
- сахарный диабет;
- нарушения сна, «кошмарные» сновидения;
- судороги, нарушение внимания, парестезии, психомоторная гиперактивность;
- конъюнктивит, сухость глаз, слезотечение;
- боль и звон в ушах;
- брадикардия, АВ блокада, увеличение интервала QT, повышение или снижение АД;
- метеоризм, недержание кала, гастроэнтерит;
- артралгия, опухание сустава и скованность;
- дизурия, недержание мочи;
- снижение либидо, выделения из сосков, гинекомастия,
- сексуальная дисфункция, изменения менструального цикла;
- периферические отеки, жажда, лихорадка, гипотермия.
Инвега, инструкция по применению (Способ и дозировка)
Препарат принимают внутрь утром, независимо от приема пищи. Дозировка Инвега зависит от тяжести заболевания и возраста больных.
При шизофрении взрослым назначают Инвега 6 мг раз в сутки. Если требуется повышение дозы рекомендуется увеличивать ее на 3 мг раз в 5 дней. У некоторых больных эффект наступает при более низких или высоких дозах — в диапазоне 3–12 мг в день. Подросткам рекомендуют 3 мг в сутки. Однако могут потребоваться и более высокие дозы, увеличение которых проводят раз в 5 суток.
При шизоаффективных расстройствах рекомендуемая доза составляет 6 мг в сутки, в утренние часы. Также возможно увеличение дозы до 12 мг в сутки, которое проводится постепенно.
При умеренном нарушении функции печени нет необходимости снижать дозу. При тяжелых — доза не более 3 мг в сутки. У пожилых пациентов доза зависит от функции почек. Безопасность препарата при лечении шизофрении у детей до 12 лет не изучалась. При переводе пациентов с палиперидона на прочие нейролептики нужно следить за состоянием больного.
Передозировка
Симптомы передозировки: сонливость и чрезмерная седация, артериальная гипотензия, тахикардия, экстрапирамидные нарушения и фибрилляция желудочков. Положение усугубляется, поскольку это препарат с пролонгированным высвобождением активного вещества. Лечение симптоматическое с поддержанием адекватной оксигенации, вентиляции и функции ССС. Тяжелые экстрапирамидные симптомы купируются м-холиноблокаторами. Специфического антидота нет.
Взаимодействие
Соблюдать осторожность при назначении с ЛС, удлиняющими интервал QT. Палиперидон не вызывает клинически значимых взаимодействиях с ЛС, которые метаболизируются системой цитохрома Р450. В исследованиях in vitro показано, что палиперидон не вызывает угнетения или индукции изоферментов этого цитохрома.
Препарат следует с осторожностью применять в комбинациях с прочими лекарственными средствами центрального действия. Нельзя совместно назначать с препаратами, которые вызывают ортостатическую гипотензию. Нейтрализует действие леводопы. Взаимодействие данного препарата и лития мало вероятно.
Одновременное назначение с вальпроатом натрия — концентрация обоих препаратов не изменялась. Значимого взаимодействия с пароксетином также не отмечено. Применение с рисперидоном не изучалось, а с карбамазепином вызывало уменьшение концентрации палиперидона в крови на 37%, в связи с чем нужно корректировать дозу последнего. Применение с триметопримом не влияло на фармакокинетические характеристики палиперидона.
Условия продажи
По рецепту.
Условия хранения
Температура до 25°С.
Срок годности
2 года.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Ксеплион, Рисперидон, Сперидан, Рисполепт.
Отзывы об Инвега
Данное лекарственное средство устраняет продуктивную симптоматику (бред, галлюцинации, ажититацию) при шизофрении. По наблюдению психиатров препарат более эффективен при шизофрении, сопровождающейся апатоабулическим синдромом (безразличие, безучастие, отрешенность от всего, паталогическое безволие, нежелание выполнять какие-либо действия). Прием препарата дает ресоциализирующий эффект — пропадает апатия ко всему происходящему и появляется потенция к действию. В своих отзывах пациенты отмечают эффективность препарата и наличие побочных эффектов.
- «... Два месяца принимал по на 12 мг. Негативные симптомы прошли — стал общительным, появился интерес к жизни. Очень повысился пролактин и меня перевели на Рисполепт».
- «… Общее состояние на Инвеге гораздо лучше, чем на других. Появилось стремление к творчеству, которое пропало 14 лет назад и созидательная бодрость».
- «… Принимаю по 12 мг — состояние нормализовалось, но, чтобы закрепить эффект, сказали еще 1,5 месяца полтора пить в этой дозировке, а потом снизить до 9 мг».
- «… Из побочек самое неприятное у меня — гормональные нарушения. Очень прибавляется вес, совсем пропали месячные, выделения из молочных желез и грудь растет».
- «… Принимаю лекарство Инвега, переношу хорошо. Врач сказал, что таблетку нельзя делить, так как ее оболочка обеспечивает постепенное выделение и длительное действие действующего вещества».
- «… При увеличении дозы появляются гриппоподобные симптомы: ломота в суставах, боли в мышцах, заложенность носа, жажда, учащенное дыхание — такое состояние, как при температуре за 40».
Данный препарат является более безопасным по сравнению с рисперидоном, но разрешен к применению только у взрослых и подростков.
Цена Инвега, где купить
Купить Инвега можно в любой аптеке. Стоимость 28 таблеток составляет 7068-8080 руб.
- Интернет-аптеки РоссииРоссия
Аптека Диалог
-
Инвега таблетки пролонгированного действия 6мг №28Janssen-Cilag
показать еще
Инвега (Палиперидон) относится к группе атипичных нейролептиков. Используют медикамент для терапии шизофрении и шизоаффективного расстройства.
Лекарство является измененной молекулой ее предшественника рисперидона, в отличие от которого Инвега имеет меньше побочных действий, а также лучшее качество и устойчивость терапии.
В печени рисперидон превращается именно в активное вещество палиперидон, молекулы которого связываются с серотонинэргическими 5 – НТ и дофаминэргическими Д – 2 рецепторами структур мозга, оказывая антипсихотический эффект. Если у пациента в анамнезе имеется печеночная недостаточность, то возможны осложнения и побочные реакции.
Лекарство выпускается в таблетках дозировкой 3, 6, 9 и 12 мг.
Фармакологический профиль
Молекула палиперидона имеет одну дополнительную гидроксильную группу в сравнении с рисперидоном. Из – за этого печень не способна к метаболизму лекарства, большая часть медикамента выделяется почками.
Благодаря этому эффекту Инвега практически не взаимодействует с лекарствами, метаболизирующимися в печени. Препарат безопасно назначать больным, которые имеют легкой или средней тяжести нарушение в работе печени.
Дополнительным положительным моментом является то, что Инвега дает более быстрый терапевтический эффект, а также отсутствует необходимость в постепенном нарастании дозировки.
При производстве лекарства используют принцип осмотического выделения действующего вещества. Осмотическое давление способствует выделению медикаментозного средства с определенной скоростью.
Капсула имеет ядро, состоящее из трех уровней. Оно окружено полупроницаемой мембраной и оболочкой. В двух слоях ядра содержатся основной компонент лекарства и дополнительные вещества.
В третьем, выталкивающем слое, расположены осмотические структуры. На слоях, содержащих лекарство, расположены 2 отверстия. Через них действующее вещество постепенно в течение суток высвобождается.
В желудке и кишечнике оболочка препарата растворяется. Мембрана пропитывается водой, которая затем проникает в ядро. Его гидрофильные полимеры набухают и образуется гель, который содержит лекарство. В последующем гель выдавливается сквозь эти отверстия.
Нерастворимые составляющие капсулы выводятся с калом. Поэтому в каловых массах можно заметить выделяющуюся таблетку. Это нормально.
Стабильный уровень препарата в крови образуется приблизительно через 5 дней от начала лечения и начиная с этого момента оказывается устойчивый терапевтический эффект.
Показания и противопоказания к применению
Инвегу используют в следующих целях:
- для длительного лечения различных форм шизофрении и купирования обострений этой болезни;
- успешно применяют для лечения шизоаффективных состояний.
- при терапии биполярного расстройства.
Противопоказания к применению следующие:
- непереносимость действующего компонента медикамента или любого другого вещества, входящего в его состав;
- острое психомоторное возбуждение с тревогой, аффективным расстройством, бредом.
Правила приема и дозировки
Препарат принимается в утренние часы. Время приема не связано с употреблением пищи. Проглатывать необходимо целую капсулу, нельзя нарушать целостность таблетки!
Когда подбирают дозу, обязательно учитывают вес человека. Для людей с массой до 50 кг дозировка лекарства обычно не выше 6 мг/сутки. Для больных весом 50 – 70 кг средняя доза препарата 9 мг.
Для людей со средним весом, которые ранее не принимали антипсихотики, или если они использовали эту группу препаратов во время лечения обострения шизофрении (длительностью не больше 2 мес.), лечение нужно начинать с 6 мг/день.
Больным с массой выше 85 кг, а также людям, имевшим в прошлом терапевтический результат только от приема высоких доз антипсихотиков, начинать прием нужно с 9 мг.
Иногда, у больных весом больше 70 кг «рабочая» доза составляет 12 мг.
Эффективная концентрация палиперидона в крови развивается через 4 — 5 дней от начала приема препарата. Тогда — же появляется и наилучший антипсихотический эффект. Потому думать о наращивании дозировки нужно не раньше, чем через 5 дней от старта терапии.
Практически всегда индивидуально подобранная дозировка препарата не нуждается в последующем увеличении. Медикамент эффективен для терапии шизофрении во время обострения и как поддерживающее лечение.
При правильной терапии полное анти продуктивное действие антипсихотического лекарства проявляется к 4 – 6 неделе от начала приема, а анти дефицитарное действие к 8 – 12 месяцу постоянного лечения.
То есть, при хорошей переносимости препарата, даже после выхода из зоны обострения, дозу можно не снижать.
Причиной для уменьшения дозировки является возникновение и сохранение дольше 7 дней побочных проявлений, таких как:
- головокружение;
- сонливость;
- легкие диспепсические нарушения.
При возникновении непереносимости или в случае тяжелых осложнений лекарство сразу отменяют. Но такие ситуации довольно редки.
Вопрос о возможной замене средства, если нет серьезных побочных явлений, нужно ставить не раньше, чем через 3 – 4 нед. от старта терапии.
Клинический эффект
Палиперидон значительно уменьшает, как позитивные проявления шизофрении (бред, расстройства мышления, галлюцинации), так и негативные симптомы (уплощение аффекта, эмоциональная закрытость, нарушение спонтанности).
Особое значение имеет уменьшение негативной симптоматики — этого, как правило, не удается достичь при лечении типичными антипсихотическими препаратами. Они обычно устраняют только позитивную симптоматику. Отмечается улучшение ночного сна при отсутствии сонливости днем.
Не продуцирует бессонницу, тревогу. При использовании медикамента нет проявлений ажитации.
У препарата больше выражен седативный эффект. Однако заторможенность и вялость, характерные для седативных антипсихотиков, отсутствует.
Случаи передозировки
При превышении дозы наблюдается усиление фармакологических свойств препарата.
Часто наблюдается синдром удлиненного интервала QТ с развитием опасной для жизни аритмии.
Развивается злокачественный нейролептический синдром, который является причиной острых отравлений и летальных случаев.
Он возникает приблизительно у 0,1% больных, которые находятся на стационарном лечении и принимают нейролептики.
Данный синдром был впервые описан 40 лет назад. В то время смертность при его возникновении составляла более 10%. Новые возможности лечения этого состояния привели к существенному уменьшению смертности в последние годы. Но все-таки это состояние и сейчас считается очень тяжелым и опасным.
Нейролептический синдром проявляется четырьмя клиническими признаками:
- повышение мышечного тонуса;
- гипертермия;
- психические расстройства;
- вегетативная «буря».
Осознанная передозировка с целью суицида
Еще одна причина острых отравлений — не медицинское использование препарата больными с целью суицида.
Самоубийство — серьезная опасность для больных шизофренией. Среди таких пациентов высока смертность от несчастных случаев, физических болезней и суицида, в сравнении с обычными людьми, а также пациентами, страдающими другими психическими расстройствами.
Предугадать вероятность самоубийства у лиц с шизофренией достаточно сложно. Это может случиться как во время стационарного лечения, так и в амбулаторных условиях.
Нерегулярный прием препарата или же полный отказ от него приводит к обострению болезни. Это повышает возможность суицида с использованием этого же лекарства.
По данным статистики 20% стационарных и 40 — 70% амбулаторных больных шизофренией негативно относятся к назначенному лечению. Что рано или поздно приводит к возврату заболевания.
Лечение передозировки симптоматическое. Антидота нет.
При тяжелых симптомах лечение происходит в условиях реанимационного отделения. Проводится:
- интубация для обеспечения функции дыхания;
- оксигенация;
- промывание желудка, кишечника;
- дезинтоксикационная терапия;
- контроль ЭКГ, лечение нарушения сердечного ритма;
- терапия коллапса, гипотензии;
- вводятся м- холиноблокаторы при экстрапирамидных нарушениях.
Значительная передозировка палиперидоном с большой вероятностью может закончиться летальным исходом.
Побочные реакции
Инвега гораздо реже, чем ее предшественник рисперидон вызывает сонливость, диспепсию, головокружения.
Сухость во рту, тремор, головные боли, повышение давления, ортостатическое падение давления, увеличение интервала QT — возникают с частотой меньше 5%. Гораздо чаще встречается тахикардия.
Экстрапирамидные эффекты от приема препарата (акатизия, гиперсаливация, ригидность, гипокинезия, острая дистония) зависят от дозы.
При использовании до 6 мг лекарства побочные проявления возникают с той же частотой, как и при приеме плацебо (до 13%).
При приеме 9 – 12 мг/сутки около 26% пациентов имеют побочные действия. Выраженность экстрапирамидных симптомов небольшая.
Возможность их возникновения увеличивается у больных:
- с тяжелой мозговой недостаточностью;
- у людей, которые ранее длительно принимали типичные нейролептики.
Наиболее ярко экстрапирамидные расстройства выражены в первые три дня лечения. Они уменьшаются за 1-3 месяца, а за тем полностью проходят.
Другие побочные проявления:
- ухудшение памяти, снижение скорости мышления и реакции на внешние раздражители и т.д.;
- цереброваскулярный дефицит.
Усиливается риск:
- ухудшения обмена углеводов;
- расширения интервала QT на кардиограмме, что проявляется тяжелой аритмией, приводящей к смерти.
Увеличение веса пациентов происходит в течении 2 месяцев лечения, в среднем на 700 гр. Значимая прибавка веса (больше 7% от исходного) возникает редко и связана с дозировкой препарата. Для сдерживания прибавки в весе не нужно назначать повышенные дозы.
Людям, склонным к ожирению, дополнительно назначают диету и физнагрузки.
Повышение содержания пролактина в крови определяется у 67% больных к концу 2й недели лечения палиперидоном. Затем этот показатель остается на одном уровне. Возможны проявления гиперпролактинемии:
- выделения из сосков;
- прекращение менструаций;
- гинекомастия;
- сексуальная дисфункция и пр.
Но возникают они всего лишь у 2% пациентов, которые используют препарат. Это выгодно отличает его от рисперидона и других классических нейролептиков.
Особые указания
Таблетки Инвега практически не изменяют свою форму при прохождении желудка и кишечника. Поэтому их нельзя принимать:
- больным со значимым сужением каких — либо отделов ЖКТ;
- пациентам с нарушением функции проглатывания.
У таких людей изредка возможно нарушение проходимости желудка или кишечника, связанное с приемом недеформируемых лекарств.
Сочетание с алкоголем
Необходимо соблюдать осторожность во время лечения при употреблении алкоголя, потому как препарат действует напрямую на головной мозг. Лучше отказаться от приема спиртных напитков.
Назначения при нарушенной работе почек и печени
Дозу лекарства уменьшают при умеренных и тяжелых нарушениях работы почек. При умеренном и средней тяжести снижении функции печени дозировку менять не нужно.
Взаимодействие с иными препаратами
Перед началом лечения и через неделю после старта терапии необходимо зарегистрировать кардиограмму, чтобы исключить расширение интервала QT.
Медикамент не рекомендовано применять для терапии психозов на фоне деменции из — за опасности цереброваскулярных осложнений.
Из – за возможного ухудшения мозговой деятельности, обменных нарушений и расширения интервала QT не рекомендовано комбинировать Инвегу с:
- трициклическими антидепрессантами;
- Кветиапином;
- в — блокерами.
Беременность и лактация
Палиперидон не назначают женщинам при кормлении грудью и беременным.
В исключительных случаях препарат назначают беременным, если польза для матери больше вреда для плода.
Прием детьми
Назначают для лечения шизофрении с 12 лет. У подростков стартовая доза – 3 мг утром. Некоторым можно увеличить дозу до 6 – 12 мг.
Практический опыт применения
Мнение практикующих врачей и отзывы пациентов, которые принимали лекарство Инвега на продолжении длительного времени.
Из психиатрической практики
Врач назначил Инвегу пациенту 25 лет, находившемуся на госпитализации 3-й раз. При приеме классических нейролептиков продуктивная симптоматика не купировалась.
У пациента оставалось выраженное безразличие. Препарат назначен по 6 мг/день. Через 2 недели пациент начал изменяться. У него проснулись эмоции, начал общаться, включаться в трудовые процессы, пропала «апатия ко всему происходящему», появился потенциал к действию.
Иной случай…
Трое больных, длительно принимавших Галоперидол переведены на Палиперидон. У пациентов при смене препарата улучшились мыслительные процессы, выросла социальная активность.
У всех троих на протяжении 3 месяцев началось обострение, что потребовало госпитализации. Доза лекарства была увеличена до 12 мг. Сроки выхода их курса терапии такие же как на Галоперидоле.
Точка зрения самих пациентов
{banner_banstat10}
Пью Инвегу, все хорошо. Несколько месяцев принимал по 9 мг – помогало. Дозу сейчас повысили до 12 мг. Побочных действий нет.
Леня, 39
2 месяца пил по 12 мг лекарства. Прошли негативные симптомы. Появился интерес к жизни, стал общительным. Очень увеличился пролактин, перевели на Рисполепт.
Николай, 40
Из побочных действий самое неприятное – гормональные нарушения. Очень прибавляется вес, пропали месячные, появились выделения из молочных желез, растет грудь.
Нина, 29
Принимаю по 12 мг – состояние улучшилось. Чтобы закрепить результат, назначили еще 1,5 мес. пить такую дозу, а потом уменьшить до 9 мг.
Коля, 33
Стоимость и аналоги
Цена одной упаковки лекарства Инвега на 28 таблеток лежит в районе 6634 – 10198 руб в зависимости от аптеки.
Хранить препарат следует в недоступном месте для детей. Температура 15 – 30 градусов Цельсия. Срок годности – 24 мес. Отпускают в аптеках, по рецепту.
Молекулярных аналогов препарата Инвега, содержащих палиперидон в составе, сейчас не существует.
На рынке присутствует только оригинальный препарат производства фирмы Янсен – Силаг, США в двух формах:
- таблетки для ежедневного приема 3, 6, 9 и 12 мг;
- Ксеплион — суспензия В — М 50, 100, 150 мг, шприц №1.
Описание
Название: Ксеплион суспензия для инъекций 100мг/1мл шприц с иглами №1(Палиперидон)
МНН: палиперидон
Производитель: ЯНССЕН ФАРМАЦЕВТИКА Н.В./БЕЛЬГИЯ
Страна: БЕЛЬГИЯ
Форма выпуска: суспензий для внутримышечного введения пролонгированного действия
Предложение для юридических лиц
Интернет-аптека «Мирофарм» осуществляет продажу оптом со склада в Москве сертифицированных лекарств и медикаментов, медицинских товаров, диагностических средств, медицинской техники, лечебной косметики, средств по уходу за больными. Оптовые цены действуют для бюджетных и коммерческих медицинских учреждений (больницы, поликлиники, медицинские центры).
Подробнее…
🏥 Купить Ксеплион суспензия для инъекций 100мг/1мл шприц с иглами №1(Палиперидон) в наших аптеках в Москве
💊 Ксеплион суспензия для инъекций 100мг/1мл шприц с иглами №1(Палиперидон) в интернет-аптеке «Мирофарм»
🚚 Доставка в аптеку Ксеплион суспензия для инъекций 100мг/1мл шприц с иглами №1(Палиперидон) в Москве от 1-го дня
Регистрационный номер
– ЛСР-009014/10
Торговое название препарата
– Ксеплион
Международное непатентованное название:
– палиперидон
Лекарственная форма Ксеплиона:
– суспензия для внутримышечного введения пролонгированного действия
Состав
Каждый предварительно заполненный шприц содержит:
Активное вещество: 100 мг палиперидона в 1 мл суспензии (эквивалентно 156 мг палиперидона пальмитата).
Вспомогательные вещества: полисорбат 20 – 12 мг, макрогол 4000 (полиэтиленгликоль 4000) – 30 мг, лимонной кислоты моногидрат – 5 мг, натрия гидрофосфат – 5 мг, натрия дигидрофосфата моногидрат – 2,5 мг, натрия гидроксид – 2,84 мг, вода для инъекций – до 1 мл.
Описание Ксеплиона
Белая или почти белая суспензия, свободная от посторонних включений
Фармакотерапевтическая группа:
– антипсихотическое средство (нейролептик).
Код АТХ
– N05AX
Фармакологические свойства Ксеплион
Фармакодинамика
Механизм действия Ксеплиона
Палиперидона пальмитат гидролизуется до палиперидона. Последний является центральнодействующим активным антагонистом преимущественно серотониновых 5-HT2A-рецепторов, а также дофаминовых D2-рецепторов, адренергических ?1— и ?2— рецепторов и Н1-гистаминовых рецепторов. Палиперидон не связывается с холинергическими м-рецепторами и с адренергическими ?1— и ?2— рецепторами. Фармакологическая активность (+) и (-) энантиомеров палиперидона количественно и качественно одинакова.
Предполагается, что терапевтическая эффективность препарата Ксеплион при шизофрении обусловлена комбинированной блокадой D2 и 5-HT2A -рецепторов.
Фармакокинетика
Всасывание и распределение
Из-за исключительно низкой растворимости в воде палиперидона пальмитат после внутримышечного введения медленно растворяется и всасывается в системный кровоток. После однократного внутримышечного введения концентрация палиперидона в плазме крови медленно увеличивается, достигая максимума через 13-14 дней (медиана) после введения в дельтовидную мышцу и 13-17 дней после введения в ягодичную мышцу.
Показания к применению Ксеплион:
Лечение шизофрении и профилактика рецидивов шизофрении.
Противопоказания:
Гиперчувствительность к палиперидону или любому компоненту препарата. Поскольку палиперидон является активным метаболитом рисперидона, Ксеплион противопоказан больным с известной гиперчувствительностью к рисперидону.
C осторожностью
Следует с осторожностью применять Ксеплион в следующих случаях (см. более подробную информацию в разделе «Особые указания»):
— У больных с сердечно-сосудистыми заболеваниями (например, сердечной недостаточностью, инфарктом или ишемией миокарда, нарушением сердечной проводимости), нарушениями мозгового кровообращения или состояниями, предрасполагающими к снижению артериального давления (например, обезвоживание, уменьшение объема циркулирующей крови, применение гипотензивных препаратов).
Срок годности Ксеплион
2 года. Не применять после истечения срока годности.
Условия хранения Ксеплион
При температуре не выше 30 °С. Хранить в недоступном для детей месте.
Условия отпуска из аптек:
По рецепту
Производитель
Производство, упаковка и выпускающий контроль:
Янссен Фармацевтика Н.В., Беерсе, Турнхоутсевег, 30, В-2340, Бельгия
Держатель регистрационного удостоверения:
ООО «Джонсон & Джонсон», Россия, 121614, Москва, ул. Крылатская, 17/2