Состав
В 1 мл препарата Небидо содержится 250 мг ундеканоата тестостерона.
Дополнительные вещества: касторовое масло, бензилбензоат.
Форма выпуска
Бледно-желтый прозрачный раствор маслянистой консистенции:
- 4 мл раствора в стеклянной ампуле, одна ампула в картонной пачке;
- 4 мл раствора в темном стеклянном флаконе, один флакон в картонной пачке.
Фармакологическое действие
Андрогенное действие.
Фармакодинамика и фармакокинетика
Фармакодинамика
Ундеканоат тестостерона является эфиром естественного тестостерона.
Тестостерон является половым гормоном мужчин, обладающим всеми видами биологической активности, нужной для поддержания и формирования андрогенных функций. Образуется в яичках и в коре надпочечников. Обеспечивает формирование мужских характеристик во время развития плода и в детстве; в подростковом периоде – развитие вторичных и первичных половых признаков. В остальное время служит для поддержания андрогенозависимых функций и мужского фенотипа.
Недостаточный биосинтез тестостерона приводит к гипогонадизму, проявляющемуся эректильной дисфункцией, утомляемостью, ослаблением полового влечения, депрессивными настроениями, обратным развитием вторичных половых признаков, остеопорозом.
Характер воздействия тестостерона в зависимости от органа-мишени может быть андрогенным или белково-анаболическим. Действие тестостерона в ряде органов проявляется после трансформации тестостерона в эстрадиол.
У мужчин с гипогонадизмом, использование андрогенов понижает количество жировой ткани, повышает нежировой вес тела, останавливает регрессию костной ткани. Андрогены способны усиливать половую функцию и оказывать позитивное психотропное влияние.
Фармакокинетика
После внутримышечного введения ундеканоата тестостерона он медленно высвобождается из депо и полностью расщепляется эстеразами сыворотки на ундекановую кислоту и тестостерон. Повышение концентраций свободного тестостерона может фиксироваться уже на следующий день.
Время наступления максимальной концентрации — 10-14 дней. Связывание с белками в сыворотке мужчины достигает 98%. Время полувыведения тестостерона – около 90 дней, что приближается к его скорости высвобождения из депо.
Метаболизируется и выводится тем же способом, что и естественный тестостерон. Подвергается значительной трансформации в печени и в иных тканях. Выводится с мочой в виде конъюгатов и через кишечник.
Показания к применению
Дефицит тестостерона при гипогонадизме (первичном и вторичном) у мужчин.
Противопоказания
- Андрогенозависимая злокачественная опухоль молочной железы у лиц мужского пола.
- Андрогенозависимая карцинома простаты.
- Опухоли печени, в том числе в анамнезе.
- Гиперкальциемия на фоне злокачественных опухолей.
- Гиперчувствительность к составляющим препарата.
- Небидо не используют у женщин.
- Следует с осторожностью использовать препарат у лиц с синдромом апноэ.
Побочные действия
- Наиболее часто встречаются акне и боль в области введения.
- Реакции со стороны крови: полицитемия, увеличение гематокрита, эритроцитоз, увеличение уровня гемоглобина.
- Реакции со стороны иммунитета: возможно развитие реакций гиперчувствительности.
- Реакции со стороны метаболизма: повышение массы тела, усиление аппетита, гиперхолестеринемия, повышение концентрации гликозилированного гемоглобина, увеличение уровня триглицеридов в плазме.
- Реакции со стороны психики: агрессивность, депрессия, беспокойство, бессонница, раздражительность.
- Реакции со стороны нервной деятельности: мигрень, головная боль, тремор.
- Реакции со стороны кровообращения: повышение давления, гипертензия, приливы, головокружение.
- Реакции со стороны дыхания: храп, бронхит, кашель, синусит, одышка, дисфония.
- Реакции со стороны пищеварения: тошнота, диарея, изменения показателей печени.
- Реакции со стороны кожи: алопеция, акне, эритема, папулезная сыпь, сыпь, сухость кожи, зуд.
- Реакции со стороны опорно-двигательной системы: боли в конечностях, артралгия, мышечные спазмы, миалгия, мышечное напряжение, увеличение активности креатинфосфокиназы, ригидность.
- Реакции со стороны мочеполовой сферы: задержка мочи, уменьшение количества выделяемой мочи, никтурия, дизурия, повышение содержания простат специфического антигена, аденома предстательной железы, патологические результаты исследования предстательной железы, интраэпителиальная неоплазия простаты, уплотнение простаты, увеличение или снижение либидо, простатит, боли в яичках или в молочной железе, повышение содержания эстрадиола, гинекомастия, повышение содержания тестостерона в крови.
- Местные реакции: дискомфорт, боли, зуд, гематома, отек, раздражение в области введения.
- Общие реакции: гипергидроз, утомляемость, астения, потливость.
Микроэмболия масляными растворами легочной артерии может в очень редких случаях вызывать одышку, кашель, недомогание, боль в груди, гипергидроз, парестезии, головокружение, обморок. Эти реакции имеют обратимый характер.
Терапия высокими дозами тестостерона вызывает обратимое понижение сперматогенеза и уменьшение яичек, а также отеки.
Инструкция по применению (Способ и дозировка)
Инструкция на Небидо рекомендует производить одну инъекцию препарата в дозе 1 грамм (1 ампула) раз в 3-4 месяца. При указанной частоте инъекций достигается поддержание адекватного уровня тестостерона и не наблюдается кумуляции вещества.
Небидо вводят строго внутримышечно непосредственно после открытия ампулы. Введение следует производить как можно медленнее. Необходимо следить, чтобы препарат не оказался в кровеносном сосуде.
Также следует определить содержание тестостерона в крови перед началом терапии. Первый перерыв между инъекциями обычно сокращается, но составляет не менее, чем 6 недель.
В конце каждого перерыва между инъекциями советуется измерять содержание тестостерона в крови. Данные значения можно корригировать изменением величины интервала между введениями.
Передозировка
В подобных случаях никаких специальных мероприятий не требуется кроме прекращения понижения дозировки или прекращения лечения.
Взаимодействие
Андрогены могут вызывать увеличение содержания оксифенбутазона в сыворотке.
Прием с препаратами, активирующими микросомальные ферменты (барбитураты), вызывает увеличение клиренса тестостерона.
Тестостерон способен повышать эффекты пероральных антикоагулянтов.
Под влиянием андрогенов вероятно усиление гипогликемического действия инсулина.
Условия продажи
Отпуск из аптек осуществляется только по рецепту.
Условия хранения
Беречь от детей. Хранить при комнатной температуре.
Срок годности
5 лет.
Особые указания
У лиц, находящихся на продолжительной терапии андрогенами, советуется периодически осуществлять контроль уровня гемоглобина и гематокрита.
При использовании андрогенов для лечения лиц пожилого возраста возможно повышение риска появления гиперплазии простаты. Также андрогены могут способствовать развитию уже имеющейся карциномы простаты.
На фоне использования тестостерона в крайне редких случаях выявлялись злокачественные и доброкачественные опухоли печени, способные приводить к внутрибрюшному кровотечению. Если во время лечения препаратом увеличивается печень, появляются сильные боли вверху живота или симптомы внутрибрюшного кровотечения, то следует исключить онкологическое заболевание печени.
Синдром апноэ во сне на фоне приема препарата может усилиться.
Андрогены не следует использовать для усиления роста мышц у здоровых лиц и для увеличения физических способностей.
Заместительное лечение тестостероном может временно понижать сперматогенез.
Препарат не изменяет способность к управлению мобильными механизмами.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Аналоги Небидо: Тестостерона Пропионат, Андриол, Андрогель, Андриол ТК, Сустанон 250, Омнадрен 250.
Детям
Небидо не предназначен лечения для детей и подростков. Его использование у данной категории лиц наряду с маскулинизацией способно вызывать стимуляцию роста и развития костной ткани, преждевременное закрытия зон роста в костях, что в конечном итоге приводит к понижению роста всего организма.
Отзывы о Небидо
Мужчины, использующие препарат для заместительной терапии, оставляют очень хорошие отзывы о Небидо. Препарат помогает им не только нормализовать свою жизнь, но и вернуть уверенность в себе, а также половую активность.
Цена Небидо, где купить
Цена Небидо в России составляет около 4000 рублей. Купить Небидо в Москве обойдется минимум в 4070 рублей.
На Украине цена данного средства приближается к 2800 гривнам.
Обобщенные научные материалы по действующему веществу препарата Небидо® (раствор для внутримышечного введения, 250 мг/мл)
Дата последней актуализации: 28.11.2020
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Владелец РУ
- Условия хранения
- Срок годности
- Источники информации
- Фармакологическая группа
- Предупреждения
- Характеристика
- Фармакология
- Показания к применению
- Нозологическая классификация (МКБ-10)
- Противопоказания
- Ограничения к применению
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Владелец РУ
Байер АГ
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
5 лет.
Не применять по истечении срока годности, указанного на упаковке.
Источники информации
Обобщенные материалы www.drugs.com и www.rxlist.com, 2020 г.
Фармакологическая группа
Предупреждения
Злоупотребление и зависимость
Имеются сообщения о злоупотреблении мужчинами, принимающими более высокие дозы легально полученного тестостерона, чем предписанные, и продолжающих прием тестостерона, несмотря на побочные эффекты или вопреки рекомендациям врача.
Продолжительное злоупотребление тестостероном и другими анаболическими стероидами может приводить к развитию зависимости (см. Меры предосторожности).
Легочная масляная микроэмболия
Введение тестостерона ундеканоата может привести к развитию серьезных, в т.ч. опасных для жизни реакций легочной масляной микроэмболии, а также анафилактоидных реакций (см. «Побочные действия» и «Меры предосторожности»). Симптомы включают кашель, позыв к кашлю, одышку, гипергидроз, сжатие в горле, боль в груди, головокружение и обморок. В некоторых случаях может потребоваться неотложная помощь и/или госпитализация.
В/м инъекция должна проводиться глубоко в ягодичные мышцы, избегая внутрисосудистого попадания.
Характеристика
Тестостерона ундеканоат представляет собой кристаллическое вещество от белого до почти белого цвета. Молекулярная масса 456,7.
Фармакология
Фармакодинамика
Основной эндогенный андроген, ответственный за рост и развитие мужских половых органов и поддержание вторичных половых признаков. Эти эффекты включают рост и созревание простаты, семенных пузырьков, полового члена и мошонки; развитие мужского типа распределения волос, например на лице, лобке, груди и подмышечных впадинах; увеличение гортани, утолщение голосовых связок и изменения мускулатуры тела и распределения жира.
Андрогены также вызывают задержку азота, натрия, калия и фосфора и снижение экскреции кальция с мочой. Андрогены увеличивают анаболизм белков и снижают катаболизм белков. Баланс азота улучшается только при достаточном потреблении калорий и белка.
Во многих тканях активность тестостерона, по-видимому, зависит от восстановления до дигидротестостерона, который связывается с белками рецептора в цитозоле. Комплекс стероид-рецептор транспортируется в ядро, где он инициирует события транскрипции и клеточные изменения, связанные с действием андрогенов.
Андрогены ответственны за всплеск роста в подростковом возрасте и за возможное прекращение линейного роста, вызванное слиянием эпифизарных центров роста. У детей экзогенные андрогены ускоряют линейную скорость роста, но могут вызывать непропорциональное ускорение созревания костей. Использование в течение длительного времени может привести к слиянию эпифизарных центров роста и прекращению процесса роста. Андрогены стимулируют выработку красных кровяных телец за счет увеличения выработки фактора эритропоэтической стимуляции.
Во время экзогенного введения андрогенов высвобождение эндогенного тестостерона подавляется за счет ингибирования ЛГ по принципу обратной связи. При больших дозах экзогенных андрогенов может также подавляться сперматогенез за счет ингибирования ФСГ по принципу обратной связи. Отсутствуют убедительные доказательства эффективности андрогенов при переломах, хирургических вмешательствах, выздоровлении и функциональном маточном кровотечении.
В результате недостаточной секреции тестостерона возникает клинический синдром — мужской гипогонадизм, который имеет две основные этиологии. Первичный гипогонадизм вызывается дефектами гонад, такими как синдром Клайнфельтера или аплазия клеток Лейдига, тогда как вторичный гипогонадизм — это неспособность гипоталамуса (или гипофиза ) вырабатывать достаточное количество ЛГРГ (или гоандотропинов — ФСГ и ЛГ).
Фармакокинетика
Абсорбция и распределение
Эфиры тестостерона менее полярны, чем свободный тестостерон. При в/м введении масляных растворов эфиры тестостерона абсорбируются из липидной фазы и в результате расщепления боковой цепи тканевыми эстеразами высвобождается тестостерон.
Тестостерон в плазме крови связывается со специфическим ГСПГ (до 98%), оставшаяся часть — с альбумином или находится в свободном состоянии.
Время достижения пикового уровня при в/м введении составляет для тестостерона ундеканоата 7 дней (медиана; диапазон от 4 до 42 дней).
Продолжительность действия составляет для тестостерона ундеканоата 18 нед.
Метаболизм
Тестостерон метаболизируется в печени до различных 17-кетостероидов двумя разными путями. Основными активными метаболитами тестостерона являются эстрадиол и дигидротестостерон.
Выведение
Около 90% дозы тестостерона, введенной в/м, выводится с мочой в виде конъюгатов с глюкуроновой, серной кислотами и других метаболитов. Около 6% дозы выводится с калом, преимущественно в неконъюгированной форме.
Показания к применению
Гипогонадизм, первичный (врожденный или приобретенный) — лечение недостаточности яичек, вызванной крипторхизмом, двусторонним перекрутом, орхитом, синдромом исчезновения яичка, орхиэктомией, синдромом Клайнфельтера, химиотерапией или токсическим повреждением от алкоголя или тяжелых металлов.
Гипогонадизм, гипогонадотропный (врожденный или приобретенный) — дефицит гонадотропина или ЛГРГ или гипофизарно-гипоталамическое повреждение опухолями, травмами или радиацией.
Задержка полового созревания у лиц мужского пола.
Тестостерон следует использовать только у пациентов, которым требуется заместительная терапия тестостероном, и если преимущества применения перевешивают серьезный риск развития легочной масляной микроэмболии и анафилаксии.
Противопоказания
Повышенная чувствительность к тестостерону и его эфирам, рак молочной железы у мужчин, рак предстательной железы (известный или подозреваемый).
Ограничения к применению
Безопасность и эффективность применения тестостерона у мужчин с возрастным гипогонадизмом (гипогонадизм с поздним началом) не установлены. Тем не менее рекомендуется предлагать терапию тестостероном пациентам с симптомами дефицита тестостерона, имеющим постоянно и однозначно низкие концентрации тестостерона по утрам.
Безопасность и эффективность тестостерона у лиц мужского пола в возрасте до 18 лет не установлены.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и кормлении грудью, а также женщинам, которые в состоянии забеременеть.
Тестостерон может причинить вред плоду при введении беременной женщине и вызвать серьезные побочные реакции у грудных детей. Воздействие андрогенов на плод или грудного ребенка может привести к различной степени вирилизации.
Побочные действия
Тестостерона ундеканоат оценивался в 84-недельном клиническом исследовании с использованием схемы дозирования 750 мг в начале лечения, через 4 нед и каждые 10 нед после этого у 153 мужчин с гипогонадизмом. Наиболее частыми побочными реакциями (>2%) были акне (5,2%), боль в месте инъекции (4,6%), повышение уровня ПСА (4,6%), гипогонадизм (2,6%) и повышение уровня эстрадиола (2,6%) (см. таблицу).
Таблица
Побочные реакции, отмечавшиеся как минимум у 1% пациентов в 84-недельном клиническом исследовании
| Предпочтительный термин MedDRA | Количество пациентов (%) |
| Угревая сыпь | 8 (5,2) |
| Боль в месте инъекции | 7 (4,6) |
| Повышенный уровень ПСА1 | 7 (4,6) |
| Увеличение уровня эстрадиола | 4 (2,6) |
| Гипогонадизм | 4 (2,6) |
| Усталость | 3 (2) |
| Раздражительность | 3 (2) |
| Повышенный уровень Hb | 3 (2) |
| Бессонница | 3 (2) |
| Перепады настроения | 3 (2) |
| Агрессивность | 2 (1,3) |
| Расстройство эякуляции | 2 (1,3) |
| Эритема в месте инъекции | 2 (1,3) |
| Повышенный гематокрит | 2 (1,3) |
| Гипергидроз | 2 (1,3) |
| Рак предстательной железы | 2 (1,3) |
| Уплотнение простаты | 2 (1,3) |
| Увеличение массы тела | 2 (1,3) |
1 Повышение уровня ПСА, определяемое как концентрация сывороточного ПСА >4 нг/мл.
В 84-недельном клиническом исследовании семь пациентов (4,6%) прекратили лечение из-за побочных реакций. Побочные реакции, приведшие к прекращению приема, включали повышение гематокрита, повышение уровня эстрадиола, повышение уровня ПСА, рак предстательной железы, перепады настроения, дисплазию предстательной железы, угри и ТГВ. В ходе 84-недельного клинического исследования средний уровень ПСА в сыворотке крови увеличился с исходного уровня (1±0,8) до (1,5±1,3) нг/мл в конце исследования. Четырнадцать пациентов (10,9%), у которых исходный уровень ПСА был <4 нг/мл, имели постбазовый уровень сывороточного ПСА >4 нг/мл в течение 84-недельного периода лечения.
В общей сложности 725 мужчин с гипогонадизмом получали тестостерона ундеканоат в/м в 7 контролируемых клинических испытаниях. В этих клинических испытаниях доза и частота применения тестостерона ундеканоата варьировались от 750 до 1000 мг и от каждых 9 нед до каждых 14 нед. Некоторые из этих клинических испытаний включали дополнительные дозы после начала терапии (например, ударные дозы). В дополнение к побочным реакциям, указанным в таблице, по крайней мере 3% пациентов в этих испытаниях сообщили о следующих побочных эффектах, независимо от оценки исследователем связи с исследуемым препаратом: синусит, простатит, артралгия, назофарингит, инфекция верхних дыхательных путей, бронхит, боль в спине, гипертония, диарея и головная боль.
Легочная масляная микроэмболия (ЛММЭ) и анафилаксия в контролируемых клинических исследованиях
Нежелательные явления, связанные с ЛММЭ и анафилаксией, были зарегистрированы у небольшого числа пациентов в контролируемых клинических исследованиях. В 84-недельном клиническом испытании у 1 пациента случился легкий приступ кашля, продолжавшийся 10 мин после третьей инъекции, который ретроспективно был отнесен на счет ЛММЭ. В другом клиническом испытании при применении тестостерона ундеканоата (1000 мг) в/м у пациента мужского пола с гипогонадизмом возникли позывы к кашлю и респираторный дистресс через 1 мин после десятой инъекции, что также было ретроспективно приписано ЛММЭ.
В ходе обзора, который включал рассмотрение всех случаев, соответствующих определенным критериям, было признано, что имели место 9 событий ЛММЭ у 8 пациентов и 2 события анафилаксии у 3556 пациентов, получавших тестостерона ундеканоат в/м в 18-ти клинических испытаниях.
Постмаркетинговый опыт
Сообщения о следующих побочных реакциях были получены во время пострегистрационного применения. Ввиду того что такие сообщения поступают в добровольном порядке от неопределенного круга лиц, не всегда возможно надежно оценить их частоту или установить причинную связь с воздействием тестостерона.
ЛММЭ и анафилаксия
Сообщалось о серьезных случаях развития ЛММЭ, включая кашель, позывы к кашлю, одышку, гипергидроз, сжатие в горле, боль в груди, головокружение и синкопальные состояния во время или сразу после в/м инъекции тестостерона ундеканоата в дозе 1000 мг. Большинство из этих событий длилось несколько минут и разрешалось поддерживающими мерами, однако некоторые из них длились до нескольких часов, а некоторым требовалась неотложная помощь и/или госпитализация. В дополнение к серьезным реакциям ЛММЭ, при в/м применении тестостерона ундеканоата отмечались эпизоды анафилаксии, в т.ч. опасные для жизни. Серьезные реакции развития ЛММЭ и анафилаксия возникали после любой инъекции ундеканоата тестостерона во время курса терапии, в т.ч. после первой дозы.
Другие побочные реакции
Следующие побочные реакции отмечались во время постмаркетинговых клинических исследований и пострегистрационного в/м применения тестостерона ундеканоата. В большинстве случаев применяемая доза составляла 1000 мг.
Со стороны крови и лимфатической системы: полицитемия, тромбоцитопения.
Сердечные заболевания: стенокардия, остановка сердца, сердечная недостаточность, ИБС, окклюзия коронарной артерии, инфаркт миокарда, тахикардия.
Нарушения слуха и со стороны внутреннего уха: внезапная потеря слуха, шум в ушах.
Эндокринные нарушения: гиперпаратиреоз, гипогликемия.
Со стороны ЖКТ: боли в верхней части живота, диарея, рвота.
Общие расстройства и реакции в месте применения: боль в груди, периферический отек, дискомфорт, гематома, раздражение, боль, реакция в месте инъекции, недомогание, парестезия, процедурная боль.
Со стороны иммунной системы: анафилактическая реакция, анафилактический шок, астма, аллергический дерматит, реакции гиперчувствительности, лейкоцитокластический васкулит.
Инфекции и инвазии: абсцесс в месте инъекции, инфекция простаты.
Отклонения результатов лабораторных исследований: увеличение уровня АЛТ, АСТ, билирубина, глюкозы в крови, повышение АД, увеличение уровня пролактина в крови, снижение или увеличение уровня тестостерона в крови, увеличение уровня триглицеридов, ГГТ в крови, повышение гематокрита, ВГД, отклонения в тестах функции печени, повышенный уровень ПСА.
Нарушения обмена веществ и питания: сахарный диабет, задержка жидкости, гиперлипидемия, гипертриглицеридемия.
Со стороны скелетно-мышечной системы и соединительной ткани: боль в груди, скелетно-мышечная боль, миалгия, остеопения, остеопороз, СКВ.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): рак предстательной железы, интраэпителиальная неоплазия предстательной железы.
Со стороны нервной системы: инсульт, цереброваскулярная недостаточность, обратимая ишемическая неврологическая недостаточность, транзиторная ишемическая атака.
Психические расстройства: агрессивность, беспокойство, депрессия, бессонница, раздражительность, неалкогольный психоз Корсакова, мужское оргазмическое расстройство, нервозность, беспокойство, нарушение сна.
Со стороны почек и мочеполовой системы: мочевой камень, дизурия, гематурия, нефролитиаз, поллакиурия, почечная колика, почечная боль, расстройство мочевыводящих путей.
Со стороны репродуктивной системы и молочных желез: азооспермия, ДГРЖ, огрубление молочной железы, боль в молочной железе, эректильная дисфункция, гинекомастия, снижение или повышение либидо, затвердение предстательной железы, простатит, сперматоцеле, боль в яичках.
Со стороны органов дыхания, грудной клетки и средостения: астма, ХОБЛ, кашель, дисфония, одышка, гипервентиляция, обструктивное нарушение дыхательных путей, отек глотки, боль в глотке, легочная микроэмболия, легочная эмболия, респираторный дистресс, ринит, синдром апноэ во сне, храп.
Со стороны кожи и подкожных тканей: акне, алопеция, ангионевротический отек, аллергический дерматит, эритема, гипергидроз, зуд, сыпь.
Сосудистые нарушения: инфаркт головного мозга, инсульт, сердечно-сосудистой коллапс, ТГВ, тромбоз, приливы, гипертония, обморок, тромбоэмболия, венозная недостаточность.
Взаимодействие
Инсулин. У пациентов, принимающих андрогены, могут наблюдаться изменения чувствительности к инсулину или гликемического контроля. У пациентов с диабетом метаболические эффекты андрогенов могут снижать уровень глюкозы в крови и, следовательно, могут потребовать снижения дозы антидиабетических ЛС.
Пероральные антикоагулянты. Изменения антикоагулянтной активности могут наблюдаться при применении андрогенов, поэтому у пациентов, принимающих варфарин, рекомендуется более частый мониторинг МНО и ПВ, особенно в начале и при прекращении терапии андрогенами. Может потребоваться снижение дозы антагониста витамина К.
Кортикостероиды. Одновременное применение тестостерона с кортикостероидами может привести к увеличению задержки жидкости и требует тщательного наблюдения, особенно у пациентов с заболеваниями сердца, почек или печени.
Оксифенбутазон. Одновременное применение оксифенбутазона и андрогенов может привести к повышению уровня оксифенбутазона в сыворотке крови.
Аймалин. Андрогены могут усиливать неблагоприятное/токсическое действие аймалина. В частности, может увеличиваться риск развития холестаза.
Ингибиторы С1. Андрогены могут усиливать тромбогенный эффект ингибиторов C1.
Циклоспорин (системный). Андрогены могут повышать концентрацию циклоспорина в сыворотке крови и усиливать его гепатотоксический эффект. Рекомендуется избегать одновременного приема андрогенов и циклоспорина. Если одновременное применение неизбежно, необходимо контролировать концентрацию циклоспорина в сыворотке крови, а также признаки и симптомы гепатотоксичности. Может потребоваться снижение дозы циклоспорина.
Дегидроэпиандростерон может усиливать неблагоприятное/токсическое действие тестостерона. Следует избегать совместного применения.
Передозировка
Симптомы: имеется одно сообщение об острой передозировке с использованием одобренного инъекционного тестостерона; пациент имел уровень тестостерона в сыворотке крови до 11400 нг/дл с нарушением мозгового кровообращения.
Лечение: прекращение применения тестостерона и проведение соответствующей симптоматической и поддерживающей терапии.
Способ применения и дозы
В/м. Режим дозирования и схемы применения зависят от заболевания и возраста пациента.
Меры предосторожности
Злоупотребление и зависимость. Злоупотреблением является преднамеренное, даже однократное, нетерапевтическое применение ЛС благодаря его психологическим и физиологическим эффектам. Злоупотребление и неправильное использование тестостерона наблюдается у взрослых мужчин и женщин, а также у подростков. Имеются сообщения о злоупотреблении мужчинами, принимающими более высокие дозы легально полученного тестостерона, чем предписанные, и продолжающих прием тестостерона, несмотря на побочные эффекты или вопреки рекомендациям врача.
Сообщалось о серьезных побочных реакциях у лиц, злоупотребляющих анаболическими андрогенными стероидами, включая остановку сердца, инфаркт миокарда, гипертрофическую кардиомиопатию, застойную сердечную недостаточность, нарушение мозгового кровообращения, гепатотоксичность и серьезные психиатрические проявления, в т.ч. большую депрессию, манию, паранойю, психоз, бред, галлюцинации, неприязнь и агрессия.
Сообщалось также о следующих побочных реакциях у мужчин: транзиторные ишемические атаки, судороги, гипомания, раздражительность, дислипидемии, атрофия яичек, недостаточная фертильность и бесплодие. Сообщалось о следующих дополнительных побочных реакциях у женщин: гирсутизм, вирилизация, огрубление голоса, увеличение клитора, атрофия груди, облысение по мужскому типу и нарушения менструального цикла.
Сообщалось о следующих побочных реакциях у подростков мужского и женского пола: преждевременное закрытие костных эпифизов с прекращением роста и преждевременное половое созревание.
Ввиду того что такие сообщения поступают в добровольном порядке от неопределенного круга лиц и могут включать злоупотребление другими веществами, не всегда возможно надежно оценить их частоту или установить причинную связь с воздействием тестостерона.
Продолжительное злоупотребление тестостероном и другими анаболическими стероидами может приводить к зависимости. Физическая зависимость характеризуется симптомами отмены после резкого прекращения приема или значительного снижения дозы ЛС. У людей, принимающих сверхтерапевтические дозы тестостерона, могут наблюдаться симптомы отмены, продолжающиеся в течение недель или месяцев, которые включают подавленное настроение, большую депрессию, усталость, тягу, беспокойство, раздражительность, анорексию, бессонницу, снижение либидо и гипогонадотропный гипогонадизм. Лекарственная зависимость у лиц, использующих утвержденные дозы тестостерона по утвержденным показаниям, не документирована.
Повышение АД. Повышение АД наблюдалось при применении тестостерона. Следует проверять АД до начала терапии, примерно через 3–6 нед после ее начала, а затем периодически. Некоторым пациентам может потребоваться начало или корректировка антигипертензивной терапии.
Рак молочной железы. Длительное (>10 лет) применение тестостерона при мужском гипогонадизме может повысить риск развития рака молочной железы.
Сердечно-сосудистые события. Имеющиеся исследования не позволяют сделать окончательных выводов в отношении риска развития серьезных неблагоприятных сердечно-сосудистых событий, таких как нефатальный инфаркт миокарда, инсульт или смерть от сердечно-сосудистых заболеваний после приема тестостерона. Некоторые исследования предполагают повышенный риск развития сердечно-сосудистых событий среди групп мужчин, которым назначена терапия тестостероном, хотя общие данные не демонстрируют повышенного или пониженного риска сердечно-сосудистых заболеваний. Согласно FDA, терапию тестостероном следует назначать только мужчинам с низким уровнем тестостерона, вызванным определенными заболеваниями (например, заболеваниями яичек, гипофиза, мозга) и подтвержденным лабораторными тестами. В заявлении, опубликованном Американской ассоциацией клинических эндокринологов (AACE) и Американским колледжем эндокринологии (ACE), рекомендуется, чтобы после тщательного диагностического обследования при заместительной терапии тестостероном руководствовались признаками и симптомами и концентрацией тестостерона, а не первопричиной. Рекомендуется избегать терапии тестостероном у мужчин, перенесших инфаркт миокарда или инсульт в течение последних 6 мес. Перед началом терапии следует оценивать факторы риска развития сердечно-сосудистых заболеваний, и внимательно следить за сердечно-сосудистыми событиями во время терапии.
Дислипидемия. Применение тестостерона может изменять липидный профиль сыворотки крови. Следует соблюдать осторожность при наличии инфаркта миокарда или ИБС в анамнезе.
Гинекомастия. Применение тестостерона может вызывать гинекомастию, которая может сохраняться у пациентов, леченных от гипогонадизма.
Воздействие на печень. Длительное применение высоких доз андрогенов было связано с серьезными поражениями печени (пелиоз печени, новообразования печени, холестатический гепатит, желтуха). Длительное в/м введение тестостерона может вызвать развитие аденомы печени. Если развиваются признаки или симптомы нарушения функции печени (например, желтуха), терапию следует прекратить.
Гиперкальциемия. Андрогены могут вызывать гиперкальциемию у пациентов с длительной иммобилизацией или раком.
Полицитемия. Возможно повышение гематокрита, что потребует корректировки дозы или отмены. Необходимо прекратить лечение у пациентов с гематокритом >48 или >50%, если они живут на больших высотах. Терапию следует прекратить, если гематокрит превышает 54%; возможно возобновление терапии с применением более низкой дозы.
Приапизм. Возможно развитие приапизма или чрезмерной сексуальной стимуляци. В этих случаях терапию необходимо приостановить, при возобновлении лечения следует использовать более низкую дозу.
Рак простаты. Может увеличиться риск развития рака простаты. Следует отказаться от терапии до проведения урологического обследования у пациентов с пальпируемым узлом простаты или уплотнениями, ПСА >4 или ПСА >3 нг/мл у мужчин с высоким риском развития рака простаты.
Венозная тромбоэмболия. При применении тестостерона сообщалось о случаях развития венозной тромбоэмболии, включая ТГВ и ТЭЛА. Необходимо обследовать пациентов с симптомами боли, отека, тепла и эритемы в нижних конечностях на предмет ТГВ и пациентов с острой одышкой на предмет ТЭЛА. При подозрении на венозную тромбоэмболию терапию следует прекратить. Не рекомендуется использование тестостерона у мужчин с гипогонадизмом и тромбофилией.
ЛММЭ. При инъекции масляных растворов тестостерона были зарегистрированы серьезные, в т.ч. опасные для жизни, случаи развития ЛММЭ и анафилаксии. Реакции включали анафилаксию, боль в груди, позыв к кашлю, головокружение, одышку, сжатие в горле и обморок. Эти реакции могут возникнуть после любой инъекции во время курса терапии, включая первую дозу. Пациенты должны находиться под наблюдением в течение 30 мин после инъекции. Чтобы свести к минимуму риск развития побочных реакций, тестостерона ундеканоат следует вводить глубоко в ягодичную мышцу.
ДГПЖ. Андрогены могут ухудшить течение ДГПЖ, их использование у пациентов с тяжелыми симптомами со стороны нижних мочевыводящих путей не рекомендуется. Терапию следует прекратить, если у пациентов с ДГПЖ развивается обструкция уретры (при возобновлении лечения используется меньшая доза).
Депрессия. Следует соблюдать осторожность при применении тестостерона у пациентов с депрессией, тестостерон может повысить риск развития депрессии и суицидальных мыслей. Необходимо производить оценку состояния пациентов с впервые возникшей или усиливающейся депрессией, тревогой, изменениями настроения или суицидальными идеями или поведением.
Заболевания, усугубляемые задержкой жидкости. Следует соблюдать осторожность у пациентов с заболеваниями, которые могут усугубляться задержкой жидкости, включая сердечную недостаточность; тестостерон может вызвать задержку жидкости. Лечение синдромов андрогенной недостаточности не рекомендуется мужчинам с неконтролируемой или плохо контролируемой сердечной недостаточностью.
Печеночная и почечная недостаточность. Тестостерон может вызвать задержку жидкости. Следует соблюдать осторожность при применении тестостерона у пациентов с печеночной и почечной недостаточностью.
Апноэ во сне. Тестостерон может усилить апноэ во сне у некоторых пациентов мужского пола, особенно у пациентов с факторами риска (например, ожирение или хроническое заболевание легких). Необходимо отказаться от начала лечения пациентов с нелеченым синдромом обструктивного апноэ во сне.
Фертильность. Большие дозы тестостерона могут подавлять сперматогенез, влияние на фертильность может быть необратимым. Лечение гипогонадотропного гипогонадизма тестостероном не рекомендуется мужчинам, желающим зачать ребенка в течение 6–12 мес.
Особые группы пациентов
Пожилой возраст. Гериатрические пациенты могут подвергаться большему риску развития ДГПЖ, рака простаты, задержки жидкости и повышения уровня трансаминаз. Заместительная терапия тестостероном у пациентов старше 65 лет обычно не рекомендуется и должна рассматриваться только в каждом конкретном случае, если присутствуют состояния или симптомы, указывающие на низкий уровень тестостерона, наряду с постоянно и однозначно низкими концентрациями тестостерона в крови по утрам.
Параметры мониторинга
До начала лечения. Подтверждение гипогонадизма измерением общего уровня тестостерона в сыворотке по крайней мере 2 раза утром после ночного голодания. Функциональные пробы печени, липидная панель, Hb и гематокрит (воздержаться от начала лечения у пациентов с гематокритом >48% или >50% у мужчин, живущих на больших высотах). Исследование ПСА и простаты у мужчин от 55 до 69 лет или ≥40 лет и с повышенным риском развития рака предстательной железы (воздержаться от лечения до урологического обследования у пациентов с пальпируемым узлом простаты или уплотнением простаты, или если уровень ПСА >4 нг/мл или ПСА >3 нг/мл у мужчин с высоким риском развития рака простаты; контроль АД.
Во время лечения. Контроль АД (от 3 до 6 нед после начала приема или корректировки дозировки и периодически после этого); функциональные тесты печени; липидный профиль, Hb и гематокрит (через 3–6 мес, через 12 мес, затем ежегодно, прекратить терапию, если гематокрит превышает 54%). Контроль содержания кальция в моче и сыворотке. Уровень глюкозы в сыворотке (может снижаться под действием тестостерона, контроль состояния пациентов с диабетом). Оценивать реакцию мужчин на лечение и побочные эффекты через 3–12 мес после начала лечения, а затем ежегодно; внимательное наблюдение за сердечно-сосудистыми событиями во время терапии.
Мужчины с гипогонадизмом, остеопорозом или переломом с малой травмой — наблюдение через 1–2 года лечения. Контроль ПСА и простаты в период от 3 до 12 мес, затем в соответствии с текущими рекомендациях по скринингу рака предстательной железы.
Свободный тестостерон следует измерять у пациентов с состояниями, связанными с повышенным или пониженным уровнем ГСПГ, или у пациентов с концентрацией общего тестостерона в пограничной зоне около нижнего предела нормального диапазона (например, от 200 до 400 нг/дл).
Определение общего тестостерона в период от 3 до 6 мес после начала лечения, через 12 мес, затем каждые 6–12 мес.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
1 ампула (4 мл раствора) содержит: действующее вещество тестостерона ундеканоат — 1000 мг, вспомогательные вещества бензилбензоат — 2000 мг, касторовое масло очищенное для парентерального введения — 1180 мг.
Концентрация действующего вещества в растворе — 250 мг/мл.
Прозрачный желтоватый масляный раствор
Тестостерона ундеканоат является эфиром природного андрогена, тестостерона. Активная форма, тестостерон, образуется в результате расщепления боковой цепи.
Тестостерон является самым важным андрогеном в мужском организме и синтезируется, главным образом, в яичках и, в меньшей степени, в коре надпочечников.
Тестостерон отвечает за формирование мужских характеристик во время внутриутробного развития, в раннем детстве, а также в период полового созревания, а впоследствии за поддержание мужского фенотипа и андрогенозависимых функций (например, сперматогенез, половые железы). Недостаточная секреция тестостерона приводит к мужскому гипогонадизму, который характеризуется низкими концентрациями тестостерона в сыворотке. К симптомам, связанным с мужским гипогонадизмом, кроме прочего, относятся эректильная дисфункция, снижение полового влечения, утомляемость, депрессивные настроения, отсутствие, недоразвитость или регресс вторичных половых признаков, а также повышенный риск остеопороза. Экзогенные андрогены назначаются с целью повышения недостаточных уровней эндогенного тестостерона и уменьшения симптомов гипогонадизма.
В зависимости от органа-мишени характер действия тестостерона является, главным образом, андрогенным (например, предстательная железа, семенные пузырьки, придаток яичка) или белково-анаболическим (мышцы, кости, кроветворная система, почки, печень).
Действия тестостерона в некоторых органах проявляются после периферического превращения тестостерона в эстрадиол, который затем связывается с эстрогенными рецепторами в ядрах клеток-мишеней (например, гипофиза, жировой ткани, головного мозга, костей и тестикулярных лейдиговских клеток).
У мужчин, страдающих гипогонадизмом, использование андрогенов снижает массу жировой ткани тела, увеличивает нежировую массу тела, а также предотвращает потерю костной ткани.
Андрогены могут улучшить половую функцию, а также оказывать положительное психотропное влияние путем улучшения настроения.
Всасывание
Небидо® представляет собой внутримышечный препарат-депо, содержащий тестостерона ундеканоат. По этой причине эффект первого пассажа отсутствует. После внутримышечной инъекции масляного раствора тестостерона ундеканоата он постепенно высвобождается из депо и почти полностью расщепляется сывороточными эстеразами на тестостерон и ундекановую кислоту. Возрастание сывороточных концентраций тестостерона относительно исходных показателей может определяться уже на следующий день после инъекции.
Распределение
В ходе двух отдельных исследований средние максимальные концентрации тестостерона, составляющие 24 и 45 нмоль/л, определялись, соответственно, через 14 и 7 дней после однократной внутримышечной инъекции 1000 мг тестостерона ундеканоата мужчинам, страдающим гипогонадизмом. Постмаксимальные уровни тестостерона снижались, при этом период полувыведения составлял приблизительно 53 дня.
Около 98% циркулирующего тестостерона связывается в сыворотке крови с ГСПС (глобулин, связывающий половые стероиды) и альбумином. Биологически активной считается только свободная фракция тестостерона. После внутривенного введения тестостерона пожилым мужчинам кажущийся объем распределения определялся на уровне приблизительно 1,0 л/кг. Метаболизм
Тестостерон, образующийся из тестостерона ундеканоата в результате расщепления эфирной связи, метаболизируется и выводится из организма теми же путями, что и эндогенный тестостерон. Ундекановая кислота метаболизируется путем р-окисления так же, как и другие алифатические карбоновые кислоты.
Выведение
Тестостерон подвергается значительному метаболизму в печени и за ее пределами. После введения меченого тестостерона около 90% радиоактивности определяется в мочи в виде глюкуронидных и сульфатных кислотных конъюгатов, а 6% после прохождения кишечнопеченочной циркуляции обнаруживается в фекалиях. Определяемые в моче продукты включают андростерон и этиохоланолон.
Равновесная концентрация
После повторных внутримышечных инъекций 1000 мг тестостерона ундеканоата мужчинам, страдающим гипогонадизмом, при интервале между инъекциями в 10 недель, равновесная концентрация достигалась между 3-ей и 5-ой инъекциями. Средние максимальные и средние минимальные концентрации тестостерона в равновесном состоянии составляли около 42 и 17 нмоль/л, соответственно. Постмаксимальные уровни тестостерона в сыворотке снижались с периодом полувыведения, равным приблизительно 90 дням, что соответствует скорости высвобождения вещества из депо.
Недостаточность тестостерона при первичном и вторичном гипогонадизме у мужчин (тестостерон-заместительная терапия).
Небидо® не должен применяться при наличии андрогенозависимой карциномы предстательной или грудной желез у мужчин; гиперкальциемии, сопутствующей злокачественным опухолям; при опухолях печени в настоящее время или в анамнезе; при повышенной чувствительности к активной субстанции или к любому из вспомогательных компонентов препарата.
Небидо® не должен применяться у женщин.
С ОСТОРОЖНОСТЬЮ
У пациентов с синдромом апноэ препарат следует применять с осторожностью.
Инъекция Небидо® (в 1 ампуле содержится 1000 мг тестостерона ундеканоата) производится один раз в 10 — 14 недель. При такой частоте инъекций обеспечивается поддержание достаточного уровня тестостерона и не происходит кумуляция вещества.
Содержимое ампулы следует ввести внутримышечно назамедлительно после ее вскрытия. Инъекцию следует производить очень медленно. Небидо® можно вводить только строго внутримышечно. Необходимо тщательно следить за тем, чтобы вводимое вещество не попало в сосуд.
Начало лечения
Перед началом лечения следует определить величину содержания тестостерона в сыворотке крови. Первый интервал между инъекциями может быть сокращен, но он должен составлять не менее 6 недель. Равновесная концентрация при такой дозе достигается быстро.
Индивидуальная корректировка лечения
В конце интервала между инъекциями рекомендуется измерять концентрацию тестостерона в сыворотке крови. Если его концентрация ниже нормальных показателей, то это может свидетельствовать о необходимости сокращения интервала между инъекциями. При высоких концентрациях следует рассмотреть вопрос о целесообразности увеличения данного интервала.
Интервал между инъекциями должен оставаться в пределах рекомендуемого диапазона 10-14 недель.
Особые категории пациентов
Дети и подростки
Небидо® не предназначен для применения у детей и подростков, поскольку для него не проводились клинические исследования у мужчин в возрасте до 18 лет (см. раздел «Особые указания»).
Пациенты пожилого возраста
Имеющиеся ограниченные данные не указывают на необходимость корректировки дозы у пациентов пожилого возраста (см. раздел «Особые указания»).
Пациенты с нарушениями функции печени
Никаких официальных исследований у пациентов с нарушениями функции печени не проводилось. Использование Небидо® противопоказано у мужчин с опухолями печени в настоящее время или в анамнезе (см. раздел «Противопоказания»).
Пациенты с почечной недостаточностью
Никаких официальных исследований у пациентов с почечной недостаточностью не проводилось.
Наиболее часто при лечении Небидо® отмечались такие нежелательные эффекты, как акне и боль в месте введения.
В представленной ниже таблице приводятся нежелательные реакции (HP), которые встречались при применении Небидо®, сгруппированные по классам систем органов в соответствии с терминологий MEdDRA. Частота встречаемости HP определена по данным клинических исследований и классифицирована следующим образом: часто (от > 1/100 до < 1/10) и нечасто (от> 1/1000 до < 1/100).
Нежелательные реакции были зарегистрированы в ходе 6 клинических исследований (суммарно 422 пациента). Их связь с Небидо® считается, по крайней мере, возможной.
Таблица. Относительная частота встречаемости пациентов с HP по классификации MedRA, определенная на основе совокупных данных шести клинических исследований, N-422 (100%)
Микроэмболия легочной артерии масляными растворами может в редких случаях приводить к появлению ряда признаков и симптомов, таких как кашель, одышка, недомогание, гипергидроз, боль в груди, головокружение, парестезии или обморок. Эти реакции могут развиваться во время инъекции или непосредственно после нее и носят обратимый характер. В ходе клинических исследований, а также в постмаркетинговый период регистрировались редко встречающиеся (> 1/10000 и < 1/1000 инъекций) случаи жировой микроэмболии легочной артерии (см. раздел «Особые указания»).
Имеются сообщения об анафилактических реакциях после инъекций Небидо®.
Наряду с вышеперечисленными нежелательными реакциями на фоне лечения тестостеронсодержащими препаратами сообщалось о нервозности, агрессии, апноэ во сне, различных кожных реакциях (включая себорею), учащении эрекций, а также о единичных случаях развития желтухи.
Терапия препаратами с высоким содержанием тестостерона обычно вызывает обратимое прекращение или снижение сперматогенеза, что приводит к уменьшению размера яичек. Тестостерон-заместительная терапия гипогонадизма в редких случаях может вызывать персистирующие болезненные эрекции (приапизм).
Длительная или высокодозированная терапия тестостероном иногда может приводить к учащению случаев задержки жидкости в организме и отекам.
Хотя в ходе клинических исследований Небидо® об этих нежелательных реакциях не сообщалось, нельзя исключить возможность их появления на фоне лечения Небидо®.
Препараты, влияющие на тестостерон
Барбитураты и другие индукторы ферментов
Возможно взаимодействие с препаратами, индуцирующими микросомальные ферменты (например, барбитураты), что может привести к возрастанию клиренса тестостерона.
Влияние андрогенов на другие препараты Оксифенбутазон
Сообщалось о возрастании концентрации оксифенбутазона в сыворотке крови.
Пероральные антикоагулянты
Тестостерон и его производные могут повышать активность пероральных антикоагулянтов, что может привести к необходимости корректировки дозы. Независимо от данного факта, в качестве общего правила следует всегда соблюдать ограничения, касающиеся внутримышечных инъекций пациентам с приобретенными или наследственными нарушениями свертываемости крови. У пациентов, получающих антикоагулянты перорально, требуется проведение тщательного контроля, особенно в начале или в конце терапии андрогенами. Рекомендуется проведение усиленного контроля за протромбиновым временем и определение международного нормализационного индекса INR.
Гипогликемические препараты
Андрогены могут усиливать гипогликемический эффект инсулина. Может появиться необходимость снизить дозу гипогликемического препарата.
Поскольку исследований совместимости не проводилось, не следует смешивать данный препарат с другими лекарственными средствами.
Другие взаимодействия
Сопутствующее применение тестостерона и АКТГ или кортикостероидов может усилить образование отеков; следовательно, данные вещества следует применять с осторожностью, особенно у пациентов с заболеваниями сердца или печени, а также у пациентов, склонных к отекам.
Влияние на результаты лабораторных исследований: Андрогены могут снижать уровень глобулина сыворотки, связывающего тироксин, что приводит к снижению общего уровня Т4 в сыворотке и усилению захвата ТЗ и Т4 ионной смолой. Однако уровни свободного тиреоидного гормона остаются неизменными, клинического подтверждения дисфункции щитовидной железы не наблюдается.
Небидо® следует применять только при проявлениях гипогонадизма (гипер- и гипогонадотропного) и лишь в том случае, если до начала лечения были исключены все прочие причины, которые могли вызывать данные симптомы. Должны присутствовать явные клинические признаки недостаточности тестостерона (регрессия вторичных половых признаков, изменение строения тела, астения, снижение либидо, эректильная дисфункция и т.д.), которая должна быть подтверждена в ходе двух отдельных измерений уровня тестостерона в крови.
Опыт применения Небидо® у пациентов пожилого возраста старше 65 лет ограничен. В настоящий момент не существует единого мнения по поводу контрольных значений уровня тестостерона в зависимости от возраста. Однако следует принимать во внимание, что с возрастом происходит физиологическое снижение уровня тестостерона в сыворотке крови.
Медицинское обследование
При использовании андрогенов для лечения пожилых пациентов может повышаться риск развития гиперплазии предстательной железы. Несмотря на отсутствие данных о том, что андрогены могут вызывать карциному предстательной железы, они могут способствовать росту уже имеющейся карциномы. Поэтому, перед началом терапии тестостероном все пациенты должны пройти тщательное обследование, чтобы исключить риск наличия рака предстательной железы. Тщательный и регулярный контроль предстательной и грудных желез должен проводиться по меньшей мере один раз в год в соответствие с рекомендованными методами (пальцевое ректальное исследование, оценка ПСА (Простатический специфический антиген) в сыворотке) у пациентов, получающих терапию тестостероном, и два раза в год у пациентов пожилого возраста и пациентов, входящих в группу риска (при наличии клинических или семейных факторов). Следует принимать во внимание региональные рекомендации по контролю безопасности при заместительной терапии тестостероном.
Помимо лабораторных анализов концентрации тестостерона у пациентов, получающих длительную терапию андрогенами, должны периодически проверяться следующие лабораторные параметры: гемоглобин, гематокрит и функциональные пробы печени.
Ввиду вариабельности лабораторных результатов все измерения уровня тестостерона должны проводиться в одной и той же лаборатории.
Опухоли
Небидо® следует применять с осторожностью у пациентов, больных раком, с риском возникновения гиперкальциемии (и связанной с ней гиперкальциурии) из-за метастазов в кости. У этих пациентов рекомендуется проведение регулярного контроля концентрации кальция в сыворотке.
Сообщается о случаях доброкачественных и злокачественных опухолей печени у пациентов, принимавших гормональные вещества, например, производные андрогена. В случае возникновения у мужчин, принимающих Небидо®, жалоб на сильную боль в верхнем отделе живота, увеличение печени или признаков внутрибрюшинного кровотечения следует включить опухоль печени в число возможных вариантов при проведении дифференциальной диагностики. Другие заболевания
У пациентов, страдающих тяжелой сердечной, печеночной или почечной недостаточностью или ишемической болезнью сердца, лечение с применением тестостерона может вызывать тяжелые осложнения, характеризующиеся отеком при наличии или отсутствии застойной сердечной недостаточности. В подобных случаях следует немедленно прекратить лечение. Исследования для подтверждения эффективности и безопасности данного лекарственного продукта у пациентов с почечной или печеночной недостаточностью не проводились. Следовательно, следует соблюдать осторожность при проведении заместительной терапии тестостероном у данных пациентов.
Следует соблюдать меры предосторожности у пациентов, предрасположенных к отекам, поскольку лечение с применением андрогенов может привести к повышенной задержке натрия. Как правило, всегда следует соблюдать ограничения по применению внутримышечных инъекций у пациентов с приобретенными или наследственными нарушениями свертывания крови.
Небидо® следует применять с осторожностью у пациентов, страдающих эпилепсией и мигренями, поскольку может наступить обострение данных заболеваний.
Улучшение чувствительности к инсулину может наблюдаться у пациентов, получающих андрогены, у которых в результате заместительной терапии достигается нормальная концентрация тестостерона в плазме.
Определенные клинические признаки, как раздражительность, нервозность, увеличение массы тела, пролонгированные или частые эрекции, могут указывать на чрезмерное воздействие андрогенами, что требует коррекции дозировки.
Существующий синдром апноэ во сне может усилиться.
Андрогены не используются для усиления развития мышц у здоровых субъектов, равно как и для повышения физической способности.
Спортсмены, получающие заместительную терапию тестостероном при первичном или вторичном мужском гипогонадизме, должны быть поставлены в известность о том, что данный лекарственный продукт содержит действующее вещество, которое может дать положительную реакцию при проведении антидопинговых проб.
Клинические исследования Небидо® с участием детей или подростков младше 18 лет до настоящего времени не проводились.
Использование тестостерона для лечения детей наряду с маскулинизацией может вызывать ускорение роста и созревания костной ткани, а также преждевременное замыкание зоны роста эпифиза, что в результате приведет к снижению конечного роста. Возможно появление обыкновенных угрей.
Как и все масляные растворы, Небидо® следует вводить внутримышечно и очень медленно, для того чтобы избежать микроэмболии легочной артерии масляным раствором препарата и которая может проявляться такими симптомами как кашель, одышка, недомогание, гипергидроз, боль за грудиной, головокружение, парестезии или обморок. Эти реакции могут развиваться во время инъекции или непосредственно после нее и носят обратимый характер. Лечение, как правило, поддерживающее, например, введение дополнительного кислорода.
Имеются сообщения об анафилактических реакциях после инъекций Небидо®.
Если во время терапии по рекомендованному режиму дозирования симптомы чрезмерного воздействия андрогенами сохраняются или возникают повторно, Небидо следует окончательно отменить.
Фертильность
Заместительная терапия тестостероном может обратимо снижать сперматогенез (см. раздел «Побочное действие»).
Данные о безопасности, полученные из доклинических исследований
Использование Небидо® может приводить к вирилизации плода женского пола на некоторых стадиях развития. Однако результаты исследований на предмет эмбриотоксических и, в частности, тератогенных эффектов, не указывают на вероятность дополнительного ухудшения развития органов.
Влияние на способность управлять транспортными средствами и движущимися механизмами
Небидо® не оказывает влияния на способность управлять автомобилем и движущимися механизмами, требующими повышенного внимания.
Раствор для внутримышечного введения 250 мг/мл.
По 4 мл препарата в ампуле из стекла гидролитического типа I янтарного цвета.
По 1 ампуле с инструкцией по применению в картонную пачку с вклеенным ампульным держателем из картона.
При температуре не выше 25°С.
Хранить в недоступном для детей месте!
5 лет.
Не применять после истечения срока годности, указанного на упаковке.
Небидо® (Nebido®) инструкция по применению
📜 Инструкция по применению Небидо®
💊 Состав препарата Небидо®
✅ Применение препарата Небидо®
📅 Условия хранения Небидо®
⏳ Срок годности Небидо®
Описание лекарственного препарата
Небидо®
(Nebido®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2014
года, дата обновления: 2022.04.20
Владелец регистрационного удостоверения:
Контакты для обращений:
БАЙЕР АГ
(Германия)
Код ATX:
G03BA03
(Тестостерон)
Лекарственные формы
| Небидо® |
Р-р д/в/м введения 250 мг/1 мл: фл. 4 мл 1 шт. рег. №: ЛС-001028 |
|
|
Р-р д/в/м введения 250 мг/1 мл: амп. 4 мл 1 шт. рег. №: ЛС-001028 |
Форма выпуска, упаковка и состав
препарата Небидо®
Раствор для в/м введения прозрачный, масляный, с желтоватым оттенком.
Вспомогательные вещества: бензилбензоат — 2 г, масло касторовое очищенное (для парентерального введения) — 1.18 г.
4 мл — ампулы из янтарного стекла типа I (1) — пачки картонные с вклеенным держателем.
4 мл — флаконы темного стекла типа I (1) — пачки картонные с вклеенным держателем.
Фармако-терапевтическая группа:
Андроген
Фармакологическое действие
Андроген. Тестостерона ундеканоат является эфиром природного андрогена, тестостерона. Активная форма, тестостерон, образуется в результате расщепления боковой цепи.
Тестостерон — мужской половой гормон, обладающий всем спектром биологической активности, необходимой для формирования и поддержания андрогенных функций. Синтезируется, главным образом, в яичках и, в меньшей степени, в коре надпочечников. Обеспечивает формирование мужских характеристик во время внутриутробного развития, в раннем детстве; в период полового созревания — развитие мужских половых органов и вторичных половых признаков. Впоследствии тестостерон обеспечивает поддержание мужского фенотипа и андрогенозависимых функций (например, сперматогенез, половые железы).
Недостаточная секреция тестостерона приводит к мужскому гипогонадизму, который характеризуется низкими концентрациями тестостерона в сыворотке. К симптомам, связанным с мужским гипогонадизмом, кроме прочего, относятся эректильная дисфункция, снижение полового влечения, утомляемость, депрессивные настроения, отсутствие, недоразвитость или регресс вторичных половых признаков, а также повышенный риск остеопороза. Экзогенные андрогены назначаются с целью повышения недостаточных уровней эндогенного тестостерона и уменьшения симптомов гипогонадизма.
В зависимости от органа-мишени характер действия тестостерона является, главным образом, андрогенным (например, предстательная железа, семенные пузырьки, придаток яичка) или белково-анаболическим (мышцы, кости, кроветворная система, почки, печень).
Действие тестостерона в некоторых органах проявляется после периферического превращения тестостерона в эстрадиол, который затем связывается с эстрогенными рецепторами в ядрах клеток-мишеней (например, гипофиза, жировой ткани, головного мозга, костей и в тестикулярных клетках Лейдига).
У мужчин, страдающих гипогонадизмом, применение андрогенов снижает массу жировой ткани тела, увеличивает нежировую массу тела, а также предотвращает потерю костной ткани. Андрогены могут улучшить половую функцию, а также оказывать положительное психотропное влияние, улучшая настроение.
Фармакокинетика
Всасывание
После в/м инъекции масляного раствора тестостерон ундеканоат постепенно высвобождается из депо и почти полностью расщепляется сывороточными эстеразами на тестостерон и ундекановую кислоту. Повышение сывороточных концентраций тестостерона относительно исходных показателей может определяться уже на следующий день после инъекции.
Распределение
В ходе двух отдельных исследований средние Cmax тестостерона, составляющие 24 нмоль/л и 45 нмоль/л, определялись соответственно через 14 и 7 дней после однократной в/м инъекции тестостерона ундеканоата в дозе 1 г мужчинам с гипогонадизмом. В сыворотке мужчины связывание с белками (ГСПС и альбумином) составляет около 98%. Биологически активной считается только свободная фракция тестостерона. После в/в инфузии тестостерона пожилым мужчинам Vd составлял около 1 л/кг.
После повторных в/м инъекций тестостерона ундеканоата в дозе 1 г мужчинам с гипогонадизмом при интервале между инъекциями в 10 недель Css достигалась между 3 и 5 инъекциями. Средние значения максимальных Css и минимальных Css тестостерона составляли около 42 и 17 нмоль/л соответственно. T1/2 тестостерона составляет около 90 дней, что соответствует скорости высвобождения вещества из депо.
Метаболизм
Тестостерон, образующийся из тестостерона ундеканоата в результате расщепления эфирной связи, метаболизируется и выводится из организма теми же путями, что и эндогенный тестостерон. Ундекановая кислота метаболизируется путем β-окисления так же, как и другие алифатические карбоновые кислоты.
Выведение
Тестостерон подвергается значительному метаболизму в печени и за ее пределами. После введения меченого тестостерона около 90% радиоактивности определяется в моче в виде глюкуронидных и сульфатных кислотных конъюгатов, а 6% после прохождения кишечно-печеночной циркуляции обнаруживается в кале. Определяемые в моче продукты включают андростерон и этиохоланолон.
Показания препарата
Небидо®
- недостаточность тестостерона при первичном и вторичном гипогонадизме у мужчин (тестостерон-заместительная терапия).
Режим дозирования
Инъекция Небидо® в дозе 1 г тестостерона ундеканоата (1 ампула) производится 1 раз в 10-14 недель. При такой частоте инъекций обеспечивается поддержание достаточного уровня тестостерона, и не происходит кумуляции вещества.
Препарат вводят в/м сразу после вскрытия ампулы. Инъекции следует производить очень медленно. Небидо® можно вводить только строго в/м. Необходимо тщательно следить за тем, чтобы препарат не попал в кровеносный сосуд.
Перед началом лечения следует определить величину содержания тестостерона в сыворотке. Первый интервал между инъекциями может быть сокращен, но должен составлять не менее 6 недель. Css при такой дозе достигается быстро.
В конце интервала между инъекциями рекомендуется измерять концентрацию тестостерона в сыворотке. Если его уровень ниже нормальных показателей, то данный факт может свидетельствовать о необходимости сокращения интервала между инъекциями. При высоких концентрациях следует рассмотреть вопрос о целесообразности увеличения данного интервала. Интервал между инъекциями должен оставаться в пределах рекомендуемого диапазона в 10-14 недель.
Поскольку клинические исследования не проводились у мужчин в возрасте до 18 лет Небидо® не предназначен для детей и подростков.
Имеющиеся ограниченные данные не указывают на необходимость коррекции дозы у пациентов пожилого возраста.
Исследований применения препарата у пациентов с нарушениями функции печени не проводилось.
Исследований применения препарата у пациентов с почечной недостаточностью не проводилось.
Побочное действие
Наиболее часто: акне, боль в месте введения.
В представленной ниже таблице приводятся нежелательные реакции, сгруппированные по классам систем органов в соответствии с терминологий MedRA. Частота встречаемости определена по данным клинических исследований и классифицирована следующим образом: часто (от ≥1/100 до < 1/10) и нечасто (от ≥1/1000 до < 1/100).
Нежелательные реакции были зарегистрированы в ходе 6 клинических исследований (суммарно — 422 пациента). Связь указанных нежелательных реакций с применением Небидо® считается, по крайней мере, возможной.
Таблица. Относительная частота встречаемости пациентов с нежелательными реакциями по классификации MedRA, определенная на основе совокупных данных 6 клинических исследований, n=422 (100%)
Микроэмболия легочной артерии масляными растворами может в редких случаях приводить к появлению ряда признаков и симптомов, таких как кашель, одышка, недомогание, гипергидроз, боль в груди, головокружение, парестезии или обморок. Эти реакции могут развиваться во время инъекции или непосредственно после нее и носят обратимый характер. В ходе клинических исследований, а также в постмаркетинговый период регистрировались редкие случаи (≥1/10 000 и <1/1000 инъекций) жировой микроэмболии легочной артерии.
После инъекций Небидо® имеются сообщения об анафилактических реакциях.
Наряду с вышеперечисленными нежелательными реакциями на фоне лечения тестостерон-содержащими препаратами сообщалось о нервозности, агрессии, апноэ во сне, различных кожных реакциях (включая себорею), учащении эрекций, а также о единичных случаях развития желтухи.
Терапия препаратами с высоким содержанием тестостерона обычно вызывает обратимое прекращение или снижение сперматогенеза, что приводит к уменьшению размера яичек.
Тестостерон-заместительная терапия гипогонадизма в редких случаях может вызывать персистирующие болезненные эрекции (приапизм).
Длительная или высокодозированная терапия тестостероном иногда может приводить к учащению случаев задержки жидкости в организме и отекам.
Противопоказания к применению
- андрогенозависимая карцинома предстательной железы;
- андрогенозависимая карцинома молочной железы у мужчин;
- гиперкальциемия, сопутствующая злокачественным опухолям;
- опухоли печени в настоящее время или в анамнезе;
- повышенная чувствительность к активной субстанции или любому из вспомогательных компонентов препарата.
Небидо® не применяют у женщин.
С осторожностью следует применять препарат у пациентов с синдромом апноэ.
Применение при беременности и кормлении грудью
Небидо® не применяют у женщин.
Применение при нарушениях функции печени
Противопоказан при опухолях печени в настоящее время или в анамнезе.
Исследований применения препарата у пациентов с нарушениями функции печени не проводилось.
Применение при нарушениях функции почек
Исследований применения препарата у пациентов с почечной недостаточностью не проводилось.
Применение у детей
Клинические испытания Небидо с участием детей или подростков младше 18 лет до настоящего времени не проводились.
Использование тестостерона для лечения детей наряду с маскулинизацией может вызывать ускорение роста и созревания костной ткани, а также преждевременное замыкание зоны роста эпифиза, что в результате приведет к снижению конечного роста. Возможно появление обыкновенных угрей
Применение у пожилых пациентов
При применении андрогенов для лечения пациентов пожилого возраста может повышаться риск развития гиперплазии предстательной железы. Несмотря на отсутствие данных о том, что андрогены могут вызывать карциному предстательной железы, они могут способствовать росту уже имеющейся карциномы. Поэтому перед началом лечения препаратами, содержащими тестостерон, следует исключить рак предстательной железы.
Особые указания
При применении андрогенов для лечения пациентов пожилого возраста может повышаться риск развития гиперплазии предстательной железы. Несмотря на отсутствие данных о том, что андрогены могут вызывать карциному предстательной железы, они могут способствовать росту уже имеющейся карциномы. Поэтому перед началом лечения препаратами, содержащими тестостерон, следует исключить рак предстательной железы.
В качестве профилактики рекомендуется проводить регулярные обследования предстательной железы.
У пациентов, находящихся на длительной терапии андрогенами, рекомендуется периодически контролировать гемоглобин и гематокрит с целью выявления случаев полицитемии.
На фоне применения половых стероидов, к которым относится и тестостерон, в редких случаях наблюдались доброкачественные и, еще реже, злокачественные опухоли печени, которые могут привести к внутрибрюшному кровотечению. Если на фоне лечения препаратом Небидо® развиваются сильные боли в верхней части живота, увеличена печень, или присутствуют признаки внутрибрюшного кровотечения, то при дифференциальной диагностике следует учесть вероятность наличия опухоли печени.
Необходимо соблюдать осторожность в отношении пациентов, склонных к отекам, поскольку терапия андрогенами может приводить к задержке выведения ионов натрия.
Существующий синдром апноэ во сне может усилиться.
Андрогены не применяют для усиления развития мышц у здоровых субъектов, равно как и для повышения физической способности.
Заместительная терапия тестостероном может обратимо снижать сперматогенез.
Как и все масляные растворы, Небидо® следует вводить в/м и очень медленно, чтобы избежать микроэмболии легочной артерии масляным раствором препарата, которая может проявляться такими симптомами как кашель, одышка, недомогание, гипергидроз, боль за грудиной, головокружение, парестезии или обморок. Эти реакции могут развиваться во время инъекции или непосредственно после нее и носят обратимый характер. Лечение, как правило, поддерживающее, например, введение дополнительного кислорода.
Использование в педиатрии
Препарат Небидо® не предназначен для применения у детей и подростков, поскольку клинические исследования препарата с участием детей и подростков в возрасте до 18 лет не проводились.
Применение тестостерона для лечения детей наряду с маскулинизацией может вызывать ускорение роста и созревания костной ткани, а также преждевременное замыкание зоны роста эпифиза, что в результате приведет к снижению конечного роста. Возможно появление обыкновенных угрей.
Влияние на способность к управлению транспортными средствами и механизмами
Небидо® не оказывает влияния на способность к управлению автомобилем и работе с механизмами, требующими повышенного внимания.
Данные по безопасности, полученные из доклинических исследований
Применение Небидо® может приводить к вирилизации плода женского пола на некоторых стадиях развития. Однако результаты исследований на предмет эмбриотоксических и, в частности, тератогенных эффектов, не указывают на вероятность дополнительного ухудшения развития органов.
Передозировка
В случае передозировки специальных терапевтических мероприятий не требуется, за исключением временного прекращения терапии или снижения дозы.
Лекарственное взаимодействие
Препараты, влияющие на тестостерон
Возможно взаимодействие с препаратами, индуцирующими микросомальные ферменты (например, барбитураты), что может привести к возрастанию клиренса тестостерона.
Влияние андрогенов на другие препараты
Андрогены способны вызывать увеличение концентрации оксифенбутазона в сыворотке.
Тестостерон и его производные способны повышать активность пероральных антикоагулянтов, что может привести к необходимости коррекции дозы. Независимо от данного факта, в качестве общего правила следует всегда соблюдать ограничения, касающиеся в/м инъекций пациентам с приобретенными или наследственными нарушениями свертываемости крови.
Под влиянием андрогенов возможно усиление гипогликемических эффектов инсулина. Может потребоваться уменьшение дозы гипогликемического препарата.
Поскольку исследований совместимости не проводилось, не следует смешивать данный препарат с другими лекарственными средствами.
Условия хранения препарата Небидо®
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Небидо®
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
БАЙЕР АГ
(Германия)

|
|
Организация, принимающая |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
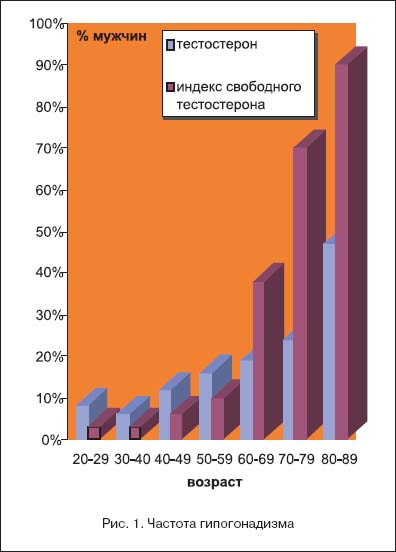
Необычайный интерес, проявляемый исследователями к проблеме возрастного андрогенного дефицита, связан прежде всего с его широкой распространенностью. Направление, изучающее синдром частичного возрастного андрогендефицита у мужчин, иначе называемый андропаузой, является стремительно развивающейся отраслью медицины. Известно, что от 40 до 50 лет примерно 7% мужчин страдает гипогонадизмом, от 60 до 80 лет – 20%, старше 80 лет – уже 35%. Согласно данным исследований, проведенных в США, гипогонадизмом страдают почти 5 млн. человек, а получают заместительную терапию лишь 5% из них [1]. В возрасте 80 лет средний уровень общего тестостерона составляет около 60% от его среднего уровня в возрасте 20 лет, а свободного – лишь 20%. Такая разница в уровнях фракций объясняется возрастанием у пожилых людей содержания глобулина, связывающего половые стероиды (примерно на 1,6% в год), что приводит к относительному увеличению связанной формы тестостерона. Однако несмотря на снижение уровня общего тестостерона с возрастом у мужчин, у большинства из них он не доходит до показателей истинного гипогонадизма (менее 12 нмоль/л). Кроме того, идет параллельное снижение количества эстрадиола, увеличивается уровень белков, связывающих гормоны, поэтому с каждым годом жизни проблемы усугубляются. Поэтому существующие мнения о необходимости заместительной гормональной терапии у мужчин нередко меняются, а порою и оспариваются. Тем не менее рекомендации, опубликованные Международным обществом по изучению проблем пожилых мужчин и касающиеся вопросов терапии андрогенного дефицита мужчин, успешно претворяются в практику [2].
К сожалению, отсутствие универсальных клинических маркеров затрудняет диагностику андрогендефицита. Наиболее достоверным биохимическим маркером является свободный тестостерон, однако его определение является чрезвычайно трудоемкой методикой. Как правило, его определяют расчетным методом на основании данных общего тестостерона и глобулина, связывающего половые стероиды, измеренного в нмоль/л. Клинические симптомы андрогенного дефицита могут маскироваться сопутствующей соматической патологией. Тем не менее его диагностика у пожилых мужчин должна осуществляться максимально широко.
Тестостерон, как известно – важнейший половой гормон, отвечающий за здоровье и активность мужчины на протяжении всей жизни. Вместе с дигидротестостероном, андростендионом и их метаболитами он создает тонус центральной нервной системы, подкорковых образований, поддерживая функциональную активность половых желез и обеспечивая копулятивную функцию. При его недостатке развиваются сердечно–сосудистые заболевания, ожирение, атеросклероз, инсулинорезистентность и сахарный диабет 2 типа, остеопения и остеопороз, анемия, сухость кожи, снижение мышечной массы и силы, эректильная дисфункция, а также вегетативные расстройства, к которым относятся колебания уровня артериального давления, кардиалгии, головокружения, повышенная потливость, внезапная гиперемия лица и шеи и пресловутые «приливы». Действия тестостерона в некоторых органах проявляются после периферического превращения тестостерона в эстрадиол, который затем связывается с эстрогенными рецепторами в ядрах клеток–мишеней (например, гипофиза, жировой ткани, головного мозга, костей и клеток Лейдига).
В основе снижения продукции тестостерона лежат уменьшение его синтеза клетками Лейдига вследствие ухудшения кровоснабжения тестикулярной ткани, а также уменьшение на их поверхности количества рецепторов к лютеинизирующему гормону, возникающие и прогрессирующие с возрастом [3]. С возрастом уменьшаются и размеры гипофиза, тем самым нарушается нейрорегуляторное звено синтеза тестостерона. МРТ головного мозга, выполненная у 153 мужчин в возрасте от 50 до 70 лет, показало прогрессивное уменьшение размеров гипофиза, начиная с 56 лет. Более чем у 80% пациентов с возрастной андрогенной недостаточностью отмечается хороший ответ при введении хорионического гонадотропина (ХГЧ), выражающийся в повышении эндогенного синтеза тестостерона клетками Лейдига [4].
Однако в литературе, касающейся спортивной медицины, есть данные, которые указывают на возможные ограничения применения препаратов ХГЧ. Продолжительность инъекций ХГЧ должна ограничиваться лишь очень малым количеством недель. Если ХГЧ принимается атлетами много недель да еще в очень высоких дозах, то возможно развитие гипофункции половых желез. По мнению Б. Филипс, прием ХГЧ должен ограничиться периодом в три недели, с паузой, по меньшей мере 6 месяцев. ХГЧ можно применять, например, в течение 2–3 недель в середине лечения и в течение 2–3 недель в конце. Следует помнить, что длительный прием ХГЧ подавляет выработку организмом гонадотропинов на длительное время, поэтому препараты следует применять лишь короткое время. Кроме того, при приеме ХГЧ возможно развитие побочных эффектов (чувство дурноты, увеличение массы тела, желудочно–кишечные расстройства).
Немалую роль в развитии андрогенной недостаточности играют роль и другие причины, поскольку показано, что у мужчин с сопутствующей соматической патологией уровень тестостерона в крови ниже, чем у здоровых мужчин того же возраста [5,6]. Помимо физиологических факторов, к гипогонадизму может приводить прием некоторых медикаментов (гипотензивные средства, снотворные, нейролептики, глюкокортикоиды, противоязвенные препараты, антиаллергены), которые часто назначают пожилым, усиливая связанное с возрастом снижение уровня свободного тестостерона.
Происходящие вследствие дефицита тестостерона у мужчин изменения по решению рабочего совещания Австрийского общества урологов (1994 г.) было предложено назвать «частичным андрогендефицитом пожилых мужчин», или синдромом PADAM (partial androgen deficiency in aging male). В последнее время отечественные авторы все больше склоняются к термину «возрастной гипогонадизм».
Последствия возрастного гипогонадизма подтверждаются рядом серьезных исследований. Работа, выполненная польскими учеными, в которой изучалась корреляция между уровнем свободного тестостерона в группе пациентов с подтвержденным на коронарографии атеросклеротическим поражением коронарных артерий и в группе здоровых мужчин, установила достоверно низкий уровень тестостерона у пациентов с андрогендефицитом [7]. При этом уровень триглицеридов и липопротеинов низкой плотности (ЛПНП) у пациентов с дефицитом тестостерона был статистически значимо выше, чем у здоровых, а показатели общего холестерина и холестерина липопротеинов высокой плотности (ЛПВП) практически не различались. Исследование W. Barud. с соавт [8] также выявило положительную корреляцию между уровнем тестостерона и холестерина ЛПВП. Следовательно, низкая концентрация тестостерона играет безусловную роль в патогенезе атеросклероза.
Не подлежит сомнению роль ожирения в развитии сердечно–сосудистой патологии. Причиной же дефицита андрогенов при ожирении является вырабатываемый белой жировой тканью лептин, стимулирующий секрецию гонадотропин–рилизинг гормона [9]. Резистентность центральных структур к лептину у больных ожирением приводит к нарушению ритма секреции гонадотропин–рилизинг–гормона, что может являться еще одной причиной развития гипогонадотропного гипогонадизма.
Возрастной дефицит андрогенов вносит свой вклад в развитие остеопении и остеопороза. С 40–летнего возраста у мужчин начинается физиологическая потеря костной массы. В начале происходит незначительная потеря – 0,3–0,5% в год. При развитии синдрома PADAM у мужчин потеря костной массы ускоряется до 2 и даже 3% в год (в зависимости от локализации костей), продолжаясь в таком темпе до 75–80 лет. Гистоморфометрическая гетерогенность гипогонального остеопороза у мужчин может отражать постепенный переход от остеокласт– до остеобластзависимых потерь массы кости с течением времени. Дефицит тестостерона может также уменьшать секрецию кальцитонина и нарушать синтез кальцитриола [10]. Несмотря на то, что более эффективно препятствуют росту маркеров метаболизма все же эстрогены, тестостерон оказывает самостоятельное действие на костную ткань, стимулируя периостальный рост кости, причем степень их влияния зависит от чувствительности андрогеновых рецепторов на остеокластах [11]. Андрогены ингибируют действие интерлейкина–6 [12].
Трудно переоценить роль гипогонадизма у пациентов с сахарным диабетом 2 типа. Результаты Массачусетского исследования по изучению старения мужчин, изучавшего распространенность нарушений половой функции в общей популяции и у больных сахарным диабетом, установили взаимосвязь между уровнями свободного тестостерона, глобулина, связывающего половые стероиды (ГСПС), и риском развития инсулинорезистентности и сахарного диабета 2 типа. Проспективное наблюдения за 1709 мужчинами в возрасте 40–70 лет в течение 7–10 лет выявило риск развития сахарного диабета типа 2, равный 1,58 при снижении уровня свободного тестостерона на 1 стандартное отклонение (3,9 нг/дл) и, соответственно, 1,89 для снижения ГСПС на 1 стандартное отклонение (15,8 нмоль/л) [13]. При наличии у обследованных сахарного диабета такое его осложнение, как эректильная дисфункция, отмечено у более чем 55% пациентов. Риск возникновения эректильной дисфункции при сахарном диабете типа 2 наблюдается в 3 раза чаще, чем в основной популяции [14]. Распространенность андрогендефицита у больных сахарным диабетом 2 типа составляет до 75% [15].
У мужчин любого возраста андрогены играют значительную роль в индукции поведения согласно принадлежности полу, управляют сексуальным поведением, а также влияют на эрекцию и либидо. Этот механизм связан с деятельностью исключительно андрогеновых рецепторов. Снижение уровня тестостерона приводит к снижению либидо и потенции. Нормальный уровень тестостерона способствует высвобождению дофамина в преоптической области как в фазе копуляции, так и в предшествующей стадии возбуждения. Этот механизм определяется выработкой под воздействием тестостерона оксида азота, влияющего на выброс дофамина [12].
В настоящее время считается доказанной отрицательная обратная связь между уровнем тестостерона и хроническими депрессиями. При лечении препаратами тестостерона пациентов с андрогенным дефицитом отмечены значительное улучшение настроения и исчезновение депрессивного синдрома [16].
Распространенность гипогонадизма достаточно высока. По данным разных авторов, она может достигать от 10 до 35% (рис. 1) [17]. Исследование, проведенное в США, в котором приняли участие 890 мужчин, продемонстрировало прогрессивное увеличение с возрастом частоты выявления низкого уровня общего тестостерона и индекса свободного тестостерона (соотношение тестостерон/глобулин, связывающий половые стероиды) [18].
Таким образом, не вызывает сомнений вопрос о возможности назначении пациентам с андрогендефицитом заместительной терапии препаратами тестостерона. При этом рассматриваются два вопроса: безопасность препарата и выбор его лекарственной формы. Широкое внедрение в практику заместительной гормональной терапии ограничено существующим мифом о негативном влиянии тестостерона на предстательную железу, особенно у пожилых мужчин. Не менее противоречивым остается мнение об отрицательном воздействии андрогенов на липидный спектр, хотя вышеуказанные исследования не подтверждают этого. Что же касается влияния заместительной андрогенной терапии на предстательную железу, то рядом работ показано, что четкой зависимости состояния простаты в пожилом возрасте от уровня тестостерона не установлено. Заместительная терапия тестостероном не способствует развитию доброкачественной гиперплазии и рака простаты, поскольку целью лечения является поддержание лишь физиологического уровня содержания гормона в крови[18].
Известно, что тестостерон подвергается метаболизму в печени и быстро разрушается в ней, следовательно, при его приеме внутрь требуются высокие дозы. Таким образом, в качестве лекарственной терапии используют модифицированные аналоги гормона и формы для его парентерального введения. Пути введения препарата следующие: пероральный, трансдермальный и инъекционный. Не умаляя значения отдельных лекарственных средств, отметим некоторые неудобства их применения. Пероральная форма представлена тестостерона ундеканоатом. Препарат имеет короткий период полувыведения, не создает гиперконцентраций, однако суммарно около 6 часов в сутки уровень тестостерона на фоне приема препарата не превышает 12 нмоль/л (при норме 12–33 нмоль/л). Кратность приема составляет 3 раза в сутки, что создает ряд неудобств для пациента. Последнее время широкое распространение получили пластыри и гели с тестостероном. Однако их применение также имеет ряд ограничений. Для большинства пациентов возникает дискомфорт из–за невозможности принять душ после нанесения препарата в течение нескольких часов (снижение концентрации препарата), что во многом изменяет их привычки. Наш опыт говорит о том, что четверть всех пациентов нарушают режим назначенного лечения, забывая о ежедневном нанесении геля, что приводит к нестабильности концентрации тестостерона в крови. Существующие буккальные формы тестостерона широкого применения в практике не нашли.
В нашем исследовании мы применяли инъекционную форму тестостерона ундеканоата, полученного при этерификации природного тестостерона в 17b–позиции. Этот препарат известен в нашей стране под названием «Небидо». Он был разработан для долговременного повышения сывороточной концентрации тестостерона у мужчин до физиологического уровня. Одна ампула содержит 1000 мг тестостерона ундеканоата в 4 мл масляного раствора (касторового масла). Показанием к применению явился лабораторно подтвержденный гипогонадизм (уровень общего тестостерона ниже 12 нмоль/л). Противопоказания при применении «Небидо» такие же, как и для любой другой формы тестостерона: андрогензависимая карцинома предстательной железы, злокачественное новообразование молочной железы у мужчин; гиперкальциемия как маркер злокачественного роста опухолей; существующая или имеющаяся в анамнезе опухоль печени; повышенная чувствительность к любому из компонентов препарата. Применялась следующая методика введения: вводилось по 1000 мг тестостерона ундеканоата за одну инъекцию, интервал между первой и второй инъекциями составил 6 недель. последующие интервалы между инъекциями – 12 недель. Содержимое одной ампулы препарата вводилось глубоко в ягодичную мышцу очень медленно в течение около 1 минуты. Соблюдение этого правил свело к минимуму неприятные ощущения, связанные с введением «Небидо». Исследование проводилось в течение 30 недель.
Всего в нашем исследовании приняли участие 42 пациента в возрасте от 59 до 72 лет (средний возраст 65,5±7,0 лет). 20 пациентов страдали сахарным диабетом от 6 до 15 лет, у 22 пациентов нарушений углеводного обмена не отмечалось. Все пациенты перед обследованием заполнили опросник выявления андрогенного дефицита, оценка снижения уровня андрогенов предварительно оценивалась по шкале Morley. Все больные имели нарушения половой функции и лабораторно подтвержденный гипогонадизм (содержание общего тестостерона ниже 12 нмоль/л). Всем пациентам был назначен препарат «Небидо» по вышеуказанной методике. Эффективность оценивалась через 5 дней, 6, 18 и 30 недель от начала терапии. Обе группы были сопоставимы по возрасту, индексу массы тела и наличию сопутствующей соматической патологии, а именно артериальной гипертензии и стабильной стенокардии (I–III функционального класса). Все пациенты с сахарным диабетом получали сходную терапию пероральными сахароснижающими препаратами, которая на протяжении исследования не менялась. У всех мужчин имелась эректильная дисфункция, тяжесть которой определялась по Международному индексу эректильной дисфункции (средний уровень составил 12 баллов, что соответствует ее средней степени тяжести (норма– 21–25 баллов). Всем пациентам была выполнена ультразвуковая диагностика пенильных артерий и определен уровень PSA (неоднократно в течение всего периода исследования). Уровень депрессивного состояния оценивался до и после исследования с использованием шкалы депрессии Бека (BDI).
У всех пациентов проводилось гормональное обследование с определением уровня общего тестостерона; свободный тестостерон определялся расчетным методом. Для исключения гипогонадотропного гипогонадизма у всех больных исследовали уровни общего тестостерона, лютеинизирующего, фолликулостимулирующего гормонов, пролактина и эстрадиола в сыворотке крови.
До начала терапии у всех пациентов, как результат андрогенного дефицита, выявлялись снижение полового влечения, различной степени нарушения половой функции, снижение работоспособности, слабость, сонливость, утомляемость, депрессивные реакции. Помимо этого, у всех пациентов отмечалось абдоминальное ожирение (индекс ОБ/ОТ составил более 1,2). Концентрация тестостерона в плазме оценивалась через 5, дней, 6, 18 и 30 недель от начала терапии.
Таким образом, уже через 5 дней от начала лечения концентрация общего тестостерона достигла нормальных значений (рис. 2). По нашим оценкам, перепадов в уровнях тестостерона в течение периода наблюдения не отмечалось. Удобная фармакокинетика препарата обеспечивала стабильную сывороточную концентрацию тестостерона у мужчин в пределах физиологической нормы. У пациентов с сахарным диабетом исходный средний уровень тестостерона крови был ниже, чем у пациентов без нарушений углеводного обмена, но через 30 недель от начала лечения оказался даже чуть выше, чем в группе больных без сахарного диабета.
Мы оценивали уровни гликированного гемоглобина, общего холестерина сыворотки крови, триглицеридов, ЛПНП, ЛПВП и индекс массы тела у пациентов на фоне лечения препаратом «Небидо». Оценка этих показателей проводилась через 6,18 и 30 недель от начала терапии. Их динамика приведена в таблице 1.
На фоне приема препарата «Небидо» не отмечалось супрафизиологических пиковых концентраций тестостерона в течение всего периода терапии. Как видно из представленных данных, у всех пациентов на фоне терапии «Небидо» отмечалось достоверное улучшение липидного профиля. Это выражалось в достоверном снижении содержания общего холестерина, ЛПНП и триглицеридов. Положительную динамику демонстрируют как уровень гликированного гемоглобина, так и индекса массы тела.
В таблице 2 приведены аналогичные результаты лечения «Небидо» у пациентов без сахарного диабета. Результаты незначительно отличаются от приведенных выше, однако позитивный эффект лечения прослеживается достаточно четко.
Уровень артериального давления у пациентов с артериальной гипертензией в ходе исследования достоверно не изменился.
Всем пациентам проводилась костная денситометрия, методом определения минеральной плотности костной ткани (МПКТ) явилась рентгеновская двухфотонная абсорбциометрия дистальных костей предплечья (аппарат DТХ 200 корпорации Osteometer) (Дания). При наличии клинических и лабораторных признаков андрогенного дефицита низкая МПКТ выявлена в 85% случаев у пациентов с сопутствующим сахарным диабетом и в 77,2% случаев без нарушений углеводного обмена. При первичном исследовании пациенты обеих групп имели плотность костной массы ниже среднереференсных показателей более чем на 1,0 SDS. Через 30 недель от начала лечения у 70,5% пациентов в группе с сахарным диабетом отмечалось увеличение плотности костной массы от исходных показателей на 0,25 SDS, в остальных случаях значимых изменений в костной ткани не было выявлено. У пациентов без сахарного диабета плотность костной массы увеличилась на такой же уровень в 38,8% случаев, в 61,2% случаев достоверно не изменилась.
Уровень артериального давления у пациентов с артериальной гипертензией в ходе исследования достоверно не изменился.
Состояние предстательной железы, включая УЗИ и определение концентрации PSA, проверялось в начале исследования, через 18 и 30 недель от начала терапии. В ходе клинических исследований ни у одного пациента не развился рак или доброкачественная гиперплазия предстательной железы. Средние значения PSA достоверно не увеличивались. Лишь у одного пациента уровень PSA достиг 4 мкг/л, однако лечения он не прекратил. Объем предстательной железы увеличивался незначительно, но оставался в физиологических пределах.
У всех пациентов отмечено улучшение сексуальной активности, повышение либидо, снижение общей массы тела и процента жировой ткани. Международный индекс эректильной дисфункции возрос и составил в среднем 17 баллов. Уровень депрессии по шкале Бека существенно снизился – в среднем с 21 балла до 11.
Таким образом, терапия «Небидо» обладает несомненным позитивным действием на липидный спектр, массу тела, компенсацию сахарного диабета 2 типа, сексуальную функцию и настроение. Его применение у пациентов с приобретенным андрогендефицитом эффективно, безопасно и существенно улучшает качество их жизни.
Для восстановления уровня тестостерона требуется лишь 4 инъекции в год, при этом отсутствует супрафизиологическое повышение уровня тестостерона после его введения.
Безусловный эффект, удобство и безопасность применения с точки зрения практического врача позволяют отдать «Небидо» предпочтение в терапии андрогенного дефицита.
Литература
1. Велиев Е.И. «Андрогендефицитные состояния у мужчин–взгляд уролога». Материалы Национального конгресса «Человек и лекарство», 2006,Москва.
2. Morales A, Lunenfeld B. Androgen replacement therapy in aging men with secondary hypogonadism. Draft recommendations for endorsement by ISSAM. Aging male 2001;4;151–62.
3. Snyder PJ, Lawrence DA. Treatment of male hypogonadism with testosterone enanthate.J Clin Endocrinol Metab. 1980 Dec;51(6):1335–9.
4. Калинченко С.Ю., Козлов Г.И., Гончаров Н.П., Новолодская Ю.В. Возрастные изменения гипоталамо–гипофизарно–тестикулярной оси у мужчин.Вторая научная конференция с международным участием посвященная 80–летию со дня рождения профессора Михаила Григорьевича Колпакова. Россия, Новосибирск, 15 – 17 октября 2002 года.
5. A multicenter trial comparing the luteinizing hormone releasing hormone analog Zoladex, with Zoladex plus flutamide in the treatment of advanced prostate cancer. Eur Urol. 1990;18 Suppl 3:28–9.
6. Верткин А.Л. и соавт.»Эректильная дисфункция: кардиологические аспекты».МЕДпресс–информ, 2005 г.144 стр.
7. Sieminska L et al. Serum free testosterone in men with coronary artery atherosclerosis. Med Sci Monit. 2003; 9(5): CR 214–218.
8. Barud W. et al. Association of obesity and insulin resistance with serum testosterone, sex hormone binding globulin and estradiol in older males. Pol Merkuriusz Lek. 2005 Mar;18(105):295–7.
9. Kim S.–C., Ahn S.–Y., Park S.–H. et al. // J. Korean Med. Sci. – 1995. – Vol. 10. – N 1.
10. Baillie S.P. Davison C.E., Johnson F.J., Francis R.M. Pathogenesis of vertebral crush fractures in men. Age Aging. 1992. N° 21. P. 139–141.
11. Pederson L.,KremerM. Judd J., Pascoe D., Spelsberg T.C., Riggs B.L, Oursler M J. Androgens regulate bone resorption activity of isolated osteoclasts in vitro. Proc Natl Acad Sci USA, 1999.
12. И.И.Дедов,С.Ю.калинченко. Возрастной андрогенный дефицит у мужчин. Москва, «Практическая медицина», 2006, 239 с.
13. Feldman H. A., Golstein I., Hatzichristou D. G. etal. Impotence and its medical and psychological correlates: results of the Massachusetts Male Aging Study // J. Urol. (Baltimore). 1994. Vol. 151. P. 54–61.
14. Hakim L S., Goldstein I. Diabetic sexual dysfunction //Endocrinol. Metab. Clin. N. Am. – 1996. – Vol. 25. –P. 379–400.
15. Калинченко С.Ю. Роль коррекции гипогонадизма в лечении сахарного диабета типа 2 у мужчин. Материалы Пятого Московского городского съезда эндокринологов 23–24 марта 2006 года.
16. BurrisAS., Banks SM, Carter C.S., Davidson JM., Sher–insRJ. A long–term, prospective study of the physiologic and behavioral effects of hormone replacement in untreated hypogonadal men. J Androl.Jul–Aug 1992; 13(4): 297–304.
17. Plymate S. Hypogonadism. Endocrinol Metab Clin North Am 1994; 23:749–772.
18. Yarman S.M.,Metter E.J.,Tobin J.D.F. et al. Longitudinal effects of aging on serum total and free testosterone levels in healthy men. J.Clin. Endocrinol.Metab,2001;86: 724–31.
19. Сегал А.С. Длительное назначение препаратов тестостерона: оценка безопасности. Симпозиум «Небидо – современные возможности в коррекции андрогендефицита у мужчин» Москва, 21 апреля 2006 года.
Проведен сравнительный анализ результатов двух независимых исследований применения тестостерона ундеканоата (препарата Небидо) у пациентов с гипогонадизмом – международного многоцентрового пострегистрационного исследования IPASS (участвовало 155 центров в 23 странах Европы (в том числе России), Азии, Латинской Америки и Австралии, n = 1493) и собственного исследования авторов (проведено в стационарах и амбулаторных учреждениях Москвы, n = 140). Показано, что при применении Небидо в режиме монотерапии по поводу эректильной дисфункции отмечена высокая терапевтическая эффективность препарата, что выразилось в положительной динамике как объективных (уровень свободного тестостерона крови), так и субъективных показателей (симптомы андрогенного дефицита по шкале Лайкерта, AMS, МИЭФ-5). На фоне терапии Небидо отмечено снижение массы тела у пациентов с избыточной массой тела и ожирением, уменьшение окружности талии, улучшение показателей липидного спектра крови (снижение уровня триглицеридов, общего холестерина, ЛПНП). У пациентов московского исследования (исходно имели метаболические нарушения) отмечено снижение уровня гликированного гемоглобина. Ни в одном случае на фоне терапии Небидо не было зарегистрировано развития рака предстательной железы.
С возрастом репродуктивная система мужчины претерпевает изменения, характеризующиеся недостаточностью андрогенов в сыворотке крови и сопровождающиеся симптомами гипогонадизма [1]. Патогенетическим лечением, направленным на восстановление нормального уровня тестостерона, является проведение заместительной терапии экзогенными андрогенами. В настоящее время синтезированы новые высокоэффективные и безопасные препараты тестостерона для проведения андрогензаместительной терапии у мужчин. Среди них заслуживает внимания препарат-депо с замедленным высвобождением действующего вещества – тестостерона ундеканоат (Небидо, компания BayerHealthCare Pharmaceuticals, Германия). Поскольку после инъекции Небидо уровень тестостерона в течение 12 недель поддерживается в физиологических пределах, без патологических повышений и снижений, такой режим терапии имеет значительное преимущество перед другими схемами лечения, предусматривающими в среднем 22 инъекции в год. Важными преимуществами для пациента являются быстрое наступление эффекта и длительность действия препарата, которая позволяет не зависеть от необходимости частого обращения к врачу.
Известно, что тестостерона ундеканоат, нормализуя уровень андрогенов, оказывает целый ряд позитивных воздействий на различные органы и системы: уровень артериального давления (АД), массу тела и его строение, показатели жирового и углеводного обмена, эректильную функцию. Так, например, исследование J. Svartberg и соавт., посвященное изучению взаимосвязи дефицита эндогенного тестостерона, артериальной гипертонии и массы миокарда левого желудочка, продемонстрировало статистически значимую обратную взаимосвязь уровня тестостерона, АД и массы левого желудочка [2], а применение тестостерона ундеканоата в комплексной терапии артериальной гипертонии позволило не только достоверно снизить цифры систолического АД (САД) и диастолического АД (ДАД), но и уменьшить дозу применявшихся ранее гипотензивных препаратов [3].
Как показано в ходе нескольких исследований, заместительная терапия препаратами тестостерона улучшает чувствительность к инсулину, снижает уровни гликированного гемоглобина (HbA1c), гликемии натощак и общего холестерина, а также уменьшает окружность талии [4]. Это подтверждается и результатами рандомизированного двойного слепого плацебоконтролируемого исследования, в котором приняли участие 50 мужчин с гипогонадизмом. Через 24 месяца у всех пациентов статистически достоверно снизились индекс инсулинорезистентности HOMA (Homeostasis Model Assessment of Insulin Resistance – математическая гомеостатическая модель для оценки резистентности к инсулину), масса висцерального жира, объем талии, улучшились показатели маркеров атеросклероза, снизился уровень гликемии [5].
Однако не все исследователи отмечают одинаковое воздействие терапии препаратами тестостерона на уровень липидов. Так, K.T. Khaw и соавт. зарегистрировали рост уровня холестерина при терапии препаратами тестостерона [6], M.H. Emmelot-Vonk и соавт. не выявили достоверного снижения уровня триглицеридов [7].
Представляют интерес данные открытого рандомизированного проспективного клинического исследования у 40 мужчин с гипогонадизмом, получавших 1000 мг тестостерона ундеканоата каждые 6–9 недель в течение 30 недель по сравнению с инъекциями тестостерона энантата 250 мг каждые 3 недели. Впоследствии исследование пролонгировалось еще на 114 недель. Его результаты не продемонстрировали изменений массы тела, но соотношение «окружность талии / окружность бедер» снизилось после проведенной терапии. Это свидетельствует о перераспределении жировой массы тела в пользу мышечной. Уровни холестерина сыворотки крови, холестерина липопротеинов низкой плотности (ЛПНП) и триглицеридов (ТГ) статистически значимо снизились в течение первых 30 недель. Уровни гемоглобина и гематокрита значительно увеличились за первые 30 недель в обеих группах, при этом показатели не превысили верхнюю границу нормы, затем наблюдался стабильный уровень гематокрита и гемоглобина. В обеих группах уровень простатспецифического антигена (ПСА) также несколько возрос после 30 недель терапии, но в дальнейшем колебался в пределах нормальных значений. Последующее применение Небидо в течение более 114 недель показало отличные характеристики его эффективности и безопасности [8].
Возможности применения заместительной гормональной терапии у пациентов с андрогенным дефицитом и эректильной дисфункцией (ЭД) на практике ограничиваются под влиянием мнения о потенциальном развитии рака предстательной железы на фоне лечения препаратами тестостерона, особенно у пожилых мужчин. Хотя факт негативного влияния андрогенов при уже имеющемся раке предстательной железы известен и не подлежит сомнению, доказательств отрицательного воздействия андрогенов на возникновение злокачественных новообразований предстательной железы не получено. Так, результаты ретроспективного исследования у 460 мужчин с раком предстательной железы подтвердили, что уровни тестостерона и глобулина, связывающего половые стероиды, не влияют на развитие рака предстательной железы [9]. Интересным представляется исследование, выполненное в США, в котором в течение 10 лет приняли участие 34 989 пациентов, получавших статины и имевших низкий уровень холестерина. По сравнению с контрольной группой пациенты с низким уровнем холестерина имели вдвое меньший риск развития рака предстательной железы и втрое меньший риск его метастазирования [10].
Заслуживает внимания наблюдение за 25 мужчинами, которые получали парентерально тестостерона ундеканоат 1000 мг каждые 12 недель в течение, по крайней мере, четырех лет. Это исследование было продолжением 30-недельного исследования, в котором эффекты тестостерона ундеканоата сравнивались с парентеральным введением тестостерона энантата. Концентрации тестостерона в плазме крови составили 11,9–15,9 нмоль/л (N (референсные значения) 10,0–30,0), уровни эстрадиола и глобулина, связывающего половые стероиды, оставались стабильными. Уровни общего холестерина, ТГ не изменились, но уровень ЛПНП снизился, а уровень липопротеинов высокой плотности (ЛПВП) первоначально уменьшился (в течение первых 30 недель), а через 3 года существенно возрос. Уровень лептина, минеральная плотность костной ткани, АД, функции печени, уровни гемоглобина и гематокрита оставались стабильными, не выходя за верхнюю границу нормы. За первые 12 месяцев исследования было отмечено увеличение объема предстательной железы с 19,7 ± 8,8 до 22,0 ± 8,4 мл (р < 0,05), но дальнейшего роста не наблюдалось. Несколько увеличился уровень ПСА – с 0,67 ± 0,38 до 0,75 ± 0,35 мкг/дл (р < 0,05) – без какой-либо динамики после 12 месяцев терапии. Таким образом, авторы пришли к заключению о том, что использование тестостерона ундеканоата – эффективный и безопасный метод лечения гипогонадизма у мужчин [11].
С целью изучения фармакокинетики и безопасности тестостерона ундеканоата в 2007 г. в США было выполнено 24-недельное открытое, многоцентровое скрининговое исследование 130 мужчин, имеющих дефицит андрогенов. Безопасность оценивалась по биохимическим маркерам и побочным эффектам. К 24-й неделе средние значения гематокрита и гемоглобина увеличились по сравнению с исходными показателями. Средний уровень ПСА также возрос по сравнению с исходным, однако случаев рака предстательной железы и гинекомастии не наблюдалось в течение всего исследования [12]. В данной статье мы сопоставили результаты двух независимых исследований – международного многоцентрового пострегистрационного мониторингового исследования IPASS (International, Multi-center Post Authorization Surveillance Study on the Use of Nebido® to Assess Tolerability and Treatment Outcomes in Daily Clinical Practice), проведенного в 155 центрах 23 стран Европы (включая Россию), Азии, Латинской Америки и Австралии [13], и собственного исследования, проведенного в стационарах и амбулаторных учреждениях г. Москвы [14].
Материалы и методы исследования IPASS и собственного исследования эффективности и безопасности Небидо у пациентов с гипогонадизмом
Конечными точками исследования IPASS явилась оценка эректильной функции, либидо, уровня жизненной силы/активности, настроения и способности к концентрации внимания. В исследование было включено 1493 пациента в возрасте 49,2 ± 13,9 года, получавших инъекции Небидо в течение 9–12 месяцев. Исследование, проведенное в Москве на базе ряда стационаров и поликлиник, включало 721 мужчину в возрасте 51,5 ± 11,9 года, у которых был выявлен андрогенный дефицит на фоне соматических заболеваний. Целью этого исследования, помимо оценки эффективности и безопасности лечения Небидо у 140 пациентов в течение 52 недель [15], было изучение распространенности андрогенного дефицита и особенностей течения гипогонадизма у пациентов с соматическими заболеваниями [16].
Диагноз гипогонадизма в обоих исследованиях устанавливался на основании международных стандартов, требующих наличия симптомов андрогенного дефицита и низкого уровня общего тестостерона в сыворотке. Оценка симптомов андрогенного дефицита проводилась с помощью перечней и пятибалльных шкал Лайкерта, а также шкалы старения мужчин AMS (Aging Males Symptoms) и Международного индекса эректильной функции-5 (МИЭФ-5). Оценка исходов лечения в исследованиях проводилась по следующим критериям:
- Изменение исходных лабораторных показателей в конце периода наблюдения.
- Изменение исходной субъективной оценки пациента до конца периода наблюдения.
- Изменение исходной тяжести симптомов или нарушений, связанных с низким уровнем тестостерона в конце периода наблюдения.
- Оценка параметров безопасности (особенно со стороны предстательной железы и гематокрита) (уровень гематокрита в нашей работе не исследовался).
- Оценка результатов лечения, по мнению пациентов, в конце периода наблюдения.
В исследование IPASS включались пациенты, страдающие первичным, вторичным или поздним гипогонадизмом, нуждающиеся в терапии тестостероном, а также мужчины, ранее получавшие другие формы андрогензаместительной терапии. Уровень свободной фракции тестостерона соответствовал диапазону 314 ± 214 пмоль/л. В наше исследование включались мужчины только с приобретенным гипогонадизмом. Уровень свободной фракции тестостерона составил 137,9; 95,0 – 181,0 (медиана (Ме); 25–75%) пмоль/л.
В исследовании IPASS средний вес исследуемых составил 86,8 ± 17,6 кг, окружность талии – 99,5 ± 15,25 см. Предшествующую терапию андрогенами получал 641 человек, из которых 37,4% – инъекции тестостерона, 44,9% – гели тестостерона и 17,5% – капсулы. Средний уровень общего тестостерона до лечения составлял 9,6 ± 7,5 нмоль/л. У пациентов имелись сопутствующие заболевания: сахарный диабет – у 14%, артериальная гипертония – у 26,1%, дислипидемия – у 22,2%, ЭД – у 64,7%. Наши пациенты имели следующие исходные характеристики: окружность талии – 116,1 ± 14,6 см, масса тела – 109,2 ± 22,6 кг. Предшествующая терапия андрогенами не проводилась. Средний уровень свободного тестостерона до лечения составлял 142,4 ± 15,3 пмоль/л. Из сопутствующих заболеваний отмечались сахарный диабет 2 типа – у 14,2%, сахарный диабет 1 типа – у 2,9%, артериальная гипертония – у 16,9%, дислипидемия – у 27,4%, ЭД – у 78,4%, ишемическая болезнь сердца (ИБС) – у 18,6%, хроническая обструктивная болезнь легких (ХОБЛ) – у 7,1% исследуемых. Сочетание заболеваний (2 и более различных нозологических форм) отмечалось у 59,6% пациентов.
Критериями исключения в обоих исследованиях были андрогензависимый рак предстательной железы или рак молочной железы у мужчин, активные опухоли печени или наличие их в анамнезе, гиперчувствительность к тестостерону, а также желаемое отцовство. Критериями исключения в нашей работе (дополнительно к вышеперечисленным) были заболевания, приводящие к снижению секреции тестостерона (гиперпролактинемия, гипотиреоз), выраженные нарушения функции почек и печени. Во время каждого из визитов в исследовании IPASS оценивались такие симптомы гипогонадизма, как приливы, избыточное потоотделение, нарушения сна и снижение физической силы. В конце каждого периода наблюдения пациент давал субъективную оценку удовлетворенности лечением, его общей переносимости и эффективности лечения в сравнении с ранее использовавшейся формой андрогенной терапии.
Частота досрочного выбывания из исследования IPASS составляла 17,5%, причем менее четверти пациентов выбывало по причине дискомфорта в месте инъекции, а большинство – по другим причинам, не связанным с нежелательными лекарственными реакциями. Различные нежелательные лекарственные реакции (все с частотой не более 4) явились причиной выбывания из исследования 31 мужчины (в основном дискомфорт в месте инъекции). В нашем исследовании досрочно выбывших не было, что связано с относительно небольшой выборкой по сравнению с исследованием IPASS.
Результаты исследований
В исследовании IPASS наблюдалось значимое улучшение общих уровней сексуального влечения / либидо: доля пациентов с очень низким / низким уровнем снизилась с 64% до 10% после 5 инъекций. Число пациентов с высоким / очень высоким уровнем либидо возросло с 10% до 61% после 5 инъекций (общий критерий χ2: р < 0,0001). Было отмечено благоприятное действие в отношении приливов: они отсутствовали у 49,8% мужчин на момент исходной оценки и у 79,1% мужчин на момент 5-й инъекции. Жалобы на избыточное потоотделение снижались аналогичным образом. Наблюдалось улучшение качества сна: доля пациентов с хорошим качеством сна увеличивалась с исходных 56% до 88% после 5 инъекций (общий критерий χ2: p < 0,0001).
Коррекция андрогенного дефицита в нашем исследовании с применением Небидо проводилась 50 пациентам с метаболическим синдромом. Из них 29 человек имели только артериальную гипертонию, 2 – ИБС, 4 – комбинацию артериальной гипертонии и ИБС, 6 – сочетание сахарного диабета 2 типа и артериальной гипертонии, 1 – сахарный диабет, артериальную гипертонию и ИБС, 8 пациентов – сочетание ХОБЛ и артериальной гипертонии. Средний индекс массы тела (ИМТ) составил 34,4 ± 6,2 кг/м². На фоне терапии тестостероном мы отметили у всех больных положительную динамику тяжести клинической симптоматики андрогенного дефицита. Так, через 52 недели терапии средний балл по анкете AMS составил 30,0 ± 9,4 против 41,2 ± 10,9 до начала терапии (р = 0,0002). Оценка лабораторных показателей андрогенного дефицита на фоне терапии тестостерона ундеканоатом также продемонстрировала положительную динамику по уровню свободного тестостерона крови и составила 634 ± 302 пмоль/л в исследовании IPASS, а в нашем – 290,3; 186,0–364,0 пмоль/л (Ме; 25–75%).
На момент исходной оценки 65% пациентов исследования IPASS имели жалобы на ЭД. Этот показатель упал до 19% после 5-й инъекции тестостерона ундеканоата (общий критерий χ2: p < 0,0001). Примерно 56% пациентов с ЭД любой степени, не получавших сопутствующей терапии ингибиторами фосфодиэстеразы 5-го типа (ФДЭ-5), отмечали снижение тяжести ЭД после лечения тестостерона ундеканоатом. Во время периода наблюдения 15–16% пациентов получали сопутствующее лечение ингибиторами ФДЭ-5, а на фоне лечения тестостерона ундеканоатом отмечалось улучшение ответа на ингибиторы ФДЭ-5 с 35% до 57% после 5 инъекций (общий критерий χ2: p < 0,0001). Доля пациентов с низким ответом на ингибиторы ФДЭ-5 или отсутствием ответа снизилась с 25,2% до 12,2% после 5 инъекций. Доля пациентов со значимым ответом на ингибиторы ФДЭ-5 увеличилась с 35,1% до 56,6% на момент 5-й инъекции.
Оценка выраженности ЭД проводилась исходно и через 52 недели от начала терапии. В нашем исследовании ЭД диагностирована у каждого третьего мужчины с артериальной гипертонией, у каждого второго – с ИБС и ХОБЛ и в 75% случаев – при сочетании этих заболеваний. Столь же высокой была частота ЭД у больных с сахарным диабетом 2 типа. Что касается тяжести ЭД, то в худшем положении находились пациенты с сахарным диабетом (тяжелая ЭД отмечена у 60% пациентов с сахарным диабетом 1 типа и у 54,1% – с сахарным диабетом 2 типа), сочетанием сахарного диабета 2 типа с ИБС (64,5%) и с артериальной гипертонией (48,8%), а также при комбинации сахарного диабета, артериальной гипертонии и ХОБЛ (68%). Тяжелые нарушения эректильной функции также отмечены у больных с алкогольной болезнью печени.
Как показал проведенный корреляционный анализ, тяжесть ЭД ассоциировалась также со стажем сердечно-сосудистого заболевания, а между уровнем тестостерона и тяжестью ЭД обнаружена умеренно сильная положительная корреляция (r = 0,67; p < 0,001). У всех пациентов наблюдалась положительная динамика тяжести ЭД. Так, через 52 недели от начала терапии средний балл по анкете МИЭФ составил в среднем 20,0 против 14,2 до начала терапии (р = 0,005). В нашем исследовании мы не наблюдали пациентов, не отреагировавших на терапию тестостероном без добавления к лечению ингибиторов ФДЭ-5.
В нашем исследовании коррекцию андрогенного дефицита с применением Небидо проводили изначально 50 пациентам. Из них 29 человек имели только артериальную гипертонию, 2 – ИБС, 4 – комбинацию артериальной гипертонии и ИБС, 6 – сочетание сахарного диабета 2 типа и артериальной гипертонии, 1 – сахарный диабет, артериальную гипертонию и ИБС и 8 – сочетание ХОБЛ и артериальной гипертонии. Средний ИМТ составил 34,4 ± 6,2 кг/м². На фоне терапии тестостероном у всех больных мы отметили положительную динамику тяжести клинической симптоматики андрогенного дефицита. Так, через 52 недели средний балл по анкете AMS составил 30,0 ± 9,4 против 41,2 ± 10,9 до начала терапии (р = 0,0002). Уровень свободного тестостерона c исходного 137,9; 95,0–181,0 (Ме; 25–75%) повысился до 290,3; 186,0–364,0 (р = 0,005).
В исследовании IPASS в подгруппе пациентов с исходно повышенным уровнем HbA1c (> 6,1%) (среднее 7,9%, n = 60) наблюдалось его снижение на 1,1% на протяжении всего периода лечения (критерий Стьюдента: p < 0,0001). В нашем исследовании влияние Небидо на течение сахарного диабета 2 типа оценивали у 20 пациентов (средний возраст 65,5 ± 7,0 лет), отобранных из основной группы. В начале исследования уровень НbА1с составил 9,3%, к концу – 6,9%, снизившись на 2,4% (р < 0,001). САД в исследовании IPASS на фоне терапии Небидо снизилось c 129,3 ± 14,6 до 127,2 ± 13,1 мм рт. ст. (p = 0,0002), ДАД – с 79,8 ± 9,8 до 78,7 ± 8,9 мм рт. ст. (р = 0,016). У наших пациентов с дефицитом андрогенов средний уровень САД и ДАД по данным суточного мониторирования был выше на 41,4 и 16,7 мм рт. ст. соответственно, по сравнению с группой с нормальным содержанием тестостерона (р = 0,002). Это подтверждается и результатами корреляционного анализа, в соответствии с которым между уровнями САД и ДАД и общего тестостерона имеется обратная сильная корреляция (r = -0,85, р = 0,00001 и r = -0,8, р = 0,002 соответственно).
В нашем исследовании мы оценивали влияние Небидо на уровень АД у 80 пациентов с артериальной гипертонией, разделенных методом пар на две одинаковые по численности подгруппы из пациентов, которым была назначена либо одна гипотензивная терапия, либо гипотензивная терапия в комбинации с Небидо. У пациентов, получавших только гипотензивную терапию (бисопролол и гидрохлоротиазид), мы наблюдали снижение САД с 167,4 ± 8,3 до 138,4 ± 4,2 мм рт. ст., ДАД – с 93,5 ± 4,7 до 84,2 ± 2,7 мм рт. ст. (p < 0,005). В подгруппе пациентов, получавших тестостерон и гипотензивную терапию, САД снизилось со 164,7 ± 7,3 до 128,6 ± 5,6 мм рт. ст., ДАД – с 91,6 ± 3,8 до 79,5 ± 3,8 мм рт. ст. (p < 0,005).
В исследовании IPASS уровень ТГ снизился со 160,0 ± 100,5 до 143,9 ± 87,2 (р < 0,0001), общего холестерина – с 197,0 ± 46,5 до 187,3 ± 44,3 (р < 0,0001), холестерина ЛПВП – повысился с 47,4 ± 18,3 до 48,3 ± 16,1 (р = 0,3), холестерина ЛПНП – снизился с 115,9 ± 40,6 до 110,9 ± 39,2 (p = 0,0017) мг/дл. В нашем исследовании влияние Небидо на уровень липидов оценивали у 40 пациентов. Уровень ТГ снизился с 2,2 ± 1,7 до 1,7 ± 0,9 ммоль/л (p < 0,001), общего холестерина – с 6,9 ± 1,2 до 5,8 ± 1,2 ммоль/л (p < 0,001), холестерина ЛПНП – с 3,0 ± 0,6 до 2,6 ± 0,6 ммоль/л (p < 0,001), холестерина ЛПВП – повысился с 0,9 до 1,0 ммоль/л (p > 0,05). Таким образом, в нашем исследовании отмечено снижение уровня холестерина в среднем на 1,1 ммоль/л, а также уровней ЛПНП и ТГ, при этом отмечено недостоверное повышение уровня ЛПВП.
В нашем исследовании мы наблюдали положительную динамику антропометрических данных у всех пациентов. Так, за 52 недели терапии масса тела у пациентов уменьшилась в среднем на 5,7 кг, окружность талии – на 5,8 см. Положительная динамика наблюдалась и по ИМТ: через 52 недели после начала лечения этот показатель снизился с 34,4 ± 6,2 до 33,1 ± 5,9 кг/м2 (р = 0,02). Снижение произошло в среднем на 1,3 кг/м² (р < 0,005). В исследовании IPASS наблюдалось небольшое снижение веса – c 86,8 до 85,6 кг, не достигшее статистической значимости (p = 0,08), однако уменьшение окружности талии (для ранее не получавших тестостерон и ранее леченных пациентов) с исходных 100 до 96 см к моменту 5-й инъекции было статистически значимым (p < 0,0001). В нашем исследовании произошло снижение массы тела с 109,2 ± 22,6 до 103,5 ± 22,6 кг (р < 0,005), а окружность талии уменьшилась с 116,1 ± 14,6 до 110,3 ± 11,2 см (р = 0,0005).
Вопросы безопасности терапии
В исследовании IPASS нежелательные лекарственные реакции встречались относительно редко: у 83 (5,8%) пациентов. Лишь в одном случае было зарегистрировано увеличение предстательной железы и задержка мочи (0,1%). Средний уровень ПСА в целом возрастал с 1,1 ± 0,9 до 1,3 ± 1,2 нг/мл, после чего оставался стабильным (p < 0,0001). У 11 мужчин уровень ПСА поднялся выше 4 нг/мл. В четырех случаях имелись клинические обоснования проведения биопсии предстательной железы, но ни в одном из них рак предстательной железы обнаружен не был. Предстательная железа – это орган-мишень для андрогенов, поэтому некоторое повышение уровня ПСА на фоне терапии тестостероном вполне объяснимо известным фармакологическим механизмом.
В нашем исследовании средние значения ПСА достоверно не увеличивались. Так, средний уровень ПСА исходно составил 0,9 ± 0,7 нг/мл, а через 30 недель – 1,1 ± 0,9 нг/мл (р = 0,3). Лишь у одного пациента уровень ПСА составил 4 нг/мл, тем не менее лечение было продолжено. Объем предстательной железы увеличивался незначительно, но оставался в физиологических пределах. У 16 пациентов, получавших тестостерон, до начала терапии была выявлена доброкачественная гиперплазия предстательной железы. На фоне терапии тестостероном у них оценивалась клиническая симптоматика расстройств мочеиспускания с использованием Международной шкалы оценки простатических симптомов (IPSS, International Prostatic Symptom Score). До начала терапии средний балл по шкале составил 6,2 ± 2,7, при повторном опросе через 30 недель терапии выраженность симптомов со стороны нижних мочевых путей значительно уменьшилась – средний балл по IPSS составил 2,1 ± 0,7 (р = 0,00002). Все пациенты отметили улучшение мочеиспускания, сокращение количества ночных мочеиспусканий.
Уровень гематокрита, оцениваемый в исследовании IPASS, повышался с исходных 42,8 ± 6,6% до 44,5 ± 6,1% после 5 инъекций (p < 0,0001). Изменение этого показателя в пределах диапазона нормы не может рассматриваться в качестве нежелательного явления. 75-й перцентиль был равен 46,4% на момент исходной оценки и 48,8% на момент 5-й инъекции. Нежелательные явления со стороны сердца были установлены у семи пациентов исследования IPASS. Случаи сердечной недостаточности и периферических отеков, связанных с сердечной недостаточностью, отсутствовали. Эти события развивались на фоне имеющихся сердечно-сосудистых нарушений. Острых сосудистых осложнений в нашем исследовании не отмечено.
Определено значимое улучшение балльных оценок психических и психо-сексуальных функций (либидо, уровень жизненных сил, общее настроение и способность к концентрации внимания), уменьшение окружности талии, а в нашем исследовании – и массы тела, так как все пациенты нашего исследования исходно имели ожирение (в отличие от исследования IPASS). Артериальное давление и показатели липидного спектра благоприятно и значимо улучшались. По истечении четырех интервалов между инъекциями тестостерона ундеканоата процентная доля пациентов с низким уровнем сексуального влечения / либидо, а также с ЭД различной степени тяжести снижалась. На момент последнего наблюдения подавляющее число пациентов были «довольны» или «очень довольны» лечением Небидо. Нежелательные явления и нежелательные лекарственные реакции наблюдались у 12% и 6% пациентов соответственно и имели в основном легкую или среднюю тяжесть. Случаев развития рака предстательной железы не наблюдалось ни в одном исследовании.
В обоих исследованиях инъекционной формы тестостерона ундеканоата длительного действия в крупной международной выборке мужчин с гипогонадизмом была продемонстрирована эффективность и хорошая переносимость такого лечения в ежедневной клинической практике в различных странах мира. Результаты позволяют говорить о клинически значимой эффективности терапии, особенно в отношении сексуальной функции. При применении тестостерона ундеканоата в режиме монотерапии по поводу ЭД было определено значимое улучшение состояния. Перевод мужчин, ранее получавших другие лекарственные формы тестостерона, на тестостерона ундеканоат сопровождался дополнительным благоприятным эффектом. В случае одновременного применения тестостерона ундеканоата с ингибиторами ФДЭ-5 наблюдалась еще более высокая терапевтическая эффективность.
Значимого снижения веса на фоне лечения тестостерона ундеканоатом не происходило (исследование IPASS), однако наблюдалась отрицательная динамика массы тела у пациентов с исходно высоким весом; охват талии значимо снижался в обоих исследованиях. Были зарегистрированы значительные благоприятные изменения липидного спектра, которые касались ТГ, общего холестерина и холестерина ЛПНП в сыворотке. Согласно некоторым сообщениям, лечение тестостероном сопровождается снижением уровня холестерина ЛПВП, однако это наблюдение обычно регистрируется в исследованиях с более высоким исходным средним уровнем тестостерона. В нашем исследовании подобное изменение отсутствовало – уровень холестерина ЛПВП оставался стабильным во время лечения. Исходно повышенный уровень HbA1c значимо снижался (повышенный уровень HbA1c свидетельствует о неблагоприятном или нарушенном обмене глюкозы / инсулинорезистентности).
В условиях тщательного наблюдения за пациентами случаев рака предстательной железы зарегистрировано не было, хотя мы предполагали, что в столь крупном исследовании могут встретиться такие пациенты. На этом показателе, а также на оценках суррогатных маркеров, таких как изменение уровня ПСА и гематокрита, основана оценка общей безопасности препаратов тестостерона. Экзогенный тестостерон не оказал значимого действия на предстательную железу в данном относительно краткосрочном исследовании в широких слоях населения.
Заключение
Применение инъекционной формы тестостерона ундеканоата в рамках ежедневной клинической практики продемонстрировало возможность подбора дозы и индивидуализации терапии у пациентов с гипогонадизмом. Благодаря способу применения, обеспечивающему стабильную концентрацию тестостерона в сыворотке и высокий уровень приверженности лечению, выводы, сделанные на основании результатов обоих анализировавшихся исследований, подкрепляют современный взгляд на целесообразность и эффективность заместительной терапии у мужчин с подтвержденным гипогонадным состоянием в условиях реальной клинической практики. Обширный опыт, полученный в обоих исследованиях, включает важные наблюдения и сведения для врачей, предлагающих своим пациентам лечение тестостероном.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.Для мужчинДля потенции
Содержание статьи
- Небидо: состав
- Небидо: МНН
- Небидо: рецепт
- Краткое содержание
- Задайте вопрос эксперту по теме статьи
По оценкам Всемирной организации здравоохранения, проблема бесплодия касается от 48 миллионов пар до 186 миллионов человек в мире. Одна из возможных причин бесплодия у мужчин: гормональные расстройства. В частности, недостаточная выработка полового гормона – тестостерона, который отвечает за секрецию и развитие сперматозоидов. Однако, отчаиваться не стоит. В настоящее время произведены препараты для коррекции гормонального уровня и других нарушений.
Провизор Анна Суменкова расскажет о препарате Небидо: ознакомит с его составом, применением и побочными эффектами.
Небидо: состав
Небидо – препарат с тестостерона ундеканоатом в роли действующего вещества. Лекарство применяется для заместительной терапии, то есть для восполнения уровня тестостерона при недостаточной его выработке.
Вследствие физико-химических особенностей тестостерона, препарат выпускается в форме масляного раствора для внутримышечного введения. Вспомогательные вещества Небидо: бензилбензоат и очищенное касторовое масло. Такой состав сказывается на способе введения препарата: инъекцию проводят медленно в течение 2 минут.
Небидо: МНН
Небидо – это международное непатентованное название препарата. Лекарство производится немецкой компанией Байер АГ в единственной лекарственной форме: растворе для инъекций.
Тестостерон отвечает за формирование первичных и вторичных мужских признаков во время внутриутробного развития, в раннем детстве и во время полового созревания. Во взрослом возрасте гормон поддерживает мужские характеристики и половые функции. Например, сперматогенез – развитие сперматозоидов.
Как говорит инструкция по применению Небидо, для мужчин тестостерон важен и для поддержания функций других органов. Например, кожи и предстательной железы. Дефицит тестостерона носит название гипогонадизм и во взрослом возрасте проявляется следующими симптомами:
- Жировые отложения по женскому типу: на животе и бедрах
- Гинекомастия – увеличение грудной железы
- Потеря волос на лице, теле и голове
- Истончение кожи и потеря ее эластичности
- Недостаточная выработка гормонов других органов: щитовидной железы и надпочечников
- Эректильная дисфункция
- Бесплодие
Небидо: рецепт
Купить тестостерон Небидо можно только по рецепту врача. Перед применением препарата необходимо убедиться в дефиците гормона путем биохимического исследования. В противном случае существует риск повысить уровень тестостерона выше нормы, что приведет к атрофии яичек и развитию гормонозависимых опухолей. Кроме того, тестостерон может вызвать побочные эффекты, такие как:
- Нарушения в эмоциональной сфере: агрессивность, раздражительность, беспокойство
- Повышение содержания клеток крови: гемоглобина и эритроцитов
- Повышение концентрации холестерина в крови
- Доброкачественная гиперплазия предстательной железы
- Увеличение массы тела
- Головная боль и мигрень
- Боль в суставах и мышцах
- Повышение артериального давления
- Развитие акне
- Нарушение функций мочевыводящих путей
- Реакция в месте введения инъекции: покраснение, зуд и боль
Краткое содержание
- Небидо – препарат с тестостерона ундеканоатов в роли действующего вещества.
- Вследствие физико-химических особенностей тестостерона, препарат выпускается в форме масляного раствора для внутримышечного введения.
- Небидо – это международное непатентованное название препарата.
- Дефицит тестостерона носит название гипогонадизм.
- Перед применением препарата необходимо убедиться в дефиците гормона путем биохимического исследования.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
Выпускающий редактор
Эксперт-провизор
Поделиться мегасоветом
Понравилась статья? Расскажите маме, папе, бабушке и тете Гале из третьего подъезда