Фенолфталеин — всем известный кислотно-основный 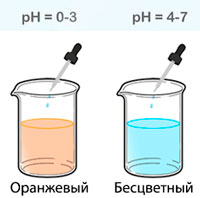
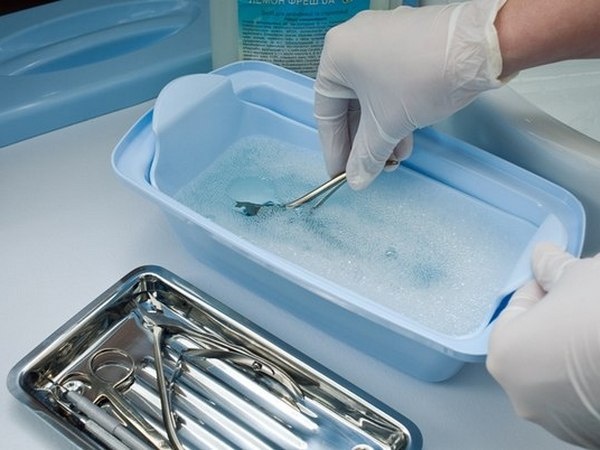
Кроме аналитической химии индикаторные свойства фенолфталеина востребованы и в других областях. Пропитанная реактивом индикаторная бумага может пригодиться на производствах для обнаружения посторонних веществ в воздухе рабочей зоны; для определения кислотности воды, крема, шампуня и т. п.; почвы в поле, на огороде, в цветочном горшке. Реактив также применяется в медицине для проверки чистоты медицинского инструментария, процедура называется «фенолфталеиновая проба».
Что такое фенолфталеиновая проба и зачем она нужна
Фенолфталеиновая проба — тест, показывающий качество помывки медицинских инструментов, принадлежностей или оборудования. С ее помощью можно определить, полностью ли смыто моющее средство с поверхности. Так как большинство средств, используемых для мытья инструментов, имеет щелочную основу, то фенолфталеиновая проба просто показывает наличие или отсутствие остатков щелочной среды. Если моющее средство не щелочное, то применяют другие тесты.
Использование пробы позволяет обнаруживать даже небольшие остатки моющих средств, показывая, что на исследуемой поверхности обнаружена щелочная среда с уровнем кислотности рН более 7.
Как проводится тестирование
Для того, чтобы проверить качество мытья инструментов или других медицинских принадлежностей, из партии предметов выбирают несколько штук (по согласованным для данного учреждения нормам). Поверхность инструмента протирают ватным тампоном или ватной палочкой, смоченными в растворе фенолфталеина. Если в инструменте есть каналы (у шприцов, например), то раствор пропускают по каналу. Далее в течение полуминуты наблюдают за обработанной поверхностью. Если она окрасилась в розовый цвет, значит инструмент промыт недостаточно тщательно и всю партию отправляют на повторную обработку. После этого тестирование проводят заново. Если поверхность осталась чистой, то партию можно отправлять на стерилизацию. Наблюдение должно ограничиваться 30-ю секундами. Любые результаты через минуту или две значения уже не имеют.
Фенолфталеиновая проба также позволяет получить дополнительную информацию о виде загрязнений. Если поверхность окрасилась в бурый цвет, то это говорит о примесях ржавчины или хлорсодержащих веществ.
Подготовка раствора фенолфталеина
В сухом кристаллическом виде фенолфталеин может 
Меры предосторожности
Фенолфталеин относится к веществам 2-й категории опасности для человека. Он может вызывать раздражение кожи или слизистых оболочек глаз, поэтому работать с реактивом следует в халате, резиновых перчатках (подходят и смотровые), в защитных очках и маске.
Фенолфталеиновая проба.
Готовят
1% спиртовой раствор фенолфталеина на
95% этиловом спирте; раствор хранят во
флаконе с притертой пробкой в холодильнике
в течение месяца.
Методика
постановки проб.
Контролируемое
изделие протирают марлевой салфеткой,
смоченной реактивом, или наносят 2-3
капли реактива на изделие с помощью
пипетки.
В
шприцы вносят 3-4 капли рабочего раствора
реактива и несколько раз продвигают
поршнем для того, чтобы смочить реактивом
внутреннюю поверхность шприца, особенно
места соединения стекла с металлом, где
чаще всего остается кровь; реактив
оставляют в шприце на 1 мин, а затем
вытесняют на марлевую салфетку. При
проверке качества очистки игл реактив
набирают в чистый, не имеющий следов
коррозии шприц. Последовательно меняя
иглы, через них пропускают реактив,
вытесняя 3-4 капли на марлевую салфетку.
Качество
очистки катетеров и других полых изделий
оценивают путем введения реактива
внутрь изделия с помощью чистого шприца
или пипетки. Реактив оставляют внутри
изделий на 1 мин, после чего сливают на
марлевую салфетку. Количество реактива,
вносимого внутрь изделия, зависит от
величины изделия.
Учет
результатов постановки проб.
При
положительной азопирамовой пробе
в присутствии следов крови немедленно
или не позднее, чем через 1 мин, появляется
вначале фиолетовое, затем быстро в
течение нескольких секунд переходящее
в розово — сиреневое или буроватое
окрашивание реактива.
Азопирам,
кроме гемоглобина, выявляет наличие на
изделиях остаточных количеств пероксидаз
растительного происхождения (растительных
остатков), окислителей (хлорамина,
хлорной извести, стирального порошка
с отбеливателем, хромовой смеси для
обработки посуды и др.), а также ржавчины
(окислов и солей железа) и кислот. При
наличии на исследуемых изделиях ржавчины
и указанных окислителей наблюдается
бурое окрашивание реактива, в остальных
случаях происходит окрашивание в розово
— сиреневый цвет.
При
постановке азопирамовой пробы окрашивание
реактивов, наступившее позже чем через
1 мин после постановки пробы, не
учитывается.
При
положительной фенолфталеиновой пробе
о наличии на изделиях остаточных
количеств щелочных компонентов моющего
средства свидетельствует появление
розового окрашивания реактива.
В
случае положительной пробы на кровь
или на остаточные количества щелочных
компонентов моющих средств, всю группу
контролируемых изделий, от которой
отбирали контроль, подвергают повторной
очистке до получения отрицательных
результатов.
Результаты
контроля отражают в журнале по форме N
366/у.
Уборка процедурного кабинета.
СЭР
процедурного кабинета и оперблока
регламентируют следующие документы:
-
СанПин
2.1.3.2630-10 «Санитарно-эпидемиологические
требования к организациям, осуществляющим
медицинскую деятельность». -
Приказ
720 «Об улучшении мед.помощи с гнойными
хирургическими заболеваниями и усилении
мероприятий по борьбе с ВБИ».
Процедурные
кабинеты, операционные блоки должны
быть размещены в помещениях, оборудованных
автономной системой приточно-вытяжной
вентиляции и кондиционирования,
обеспечивающей нормируемые параметры
микроклимата, чистоту воздуха. В
процедурных кабинетах предусматривается
зонирование на стерильную и нестерильную
зоны. В стерильной зоне находится
стерильный стол, рабочий стол. Нахождение
в стерильной зоне без стерильной одежды
строго запрещено. Стерильная зона
процедурного кабинета отделяется от
нестерильной зоны «красной чертой».
В
операционных блоках предусматривается
строгое зонирование внутренних помещений
на стерильную зону (операционные), зону
строгого режима (предоперационные,
помещение подготовки больного — наркозная,
помещения хранения стерильных материалов
и другие вспомогательные помещения,
для которых соблюдается режим санитарного
пропускника для входа персонала), зону
общебольничного режима (шлюз). В шлюзе
персонал отделения, сопровождающий
пациента, перекладывает его с каталки
отделения на каталку операционного
блока. Далее персонал операционного
блока перевозит пациента в операционную.
Зона общебольничного режима (после
шлюза) отделяется от остальных помещений
операционного блока «красной чертой».
Вход
персонала других отделений за «красную
черту» запрещен. При необходимости,
персонал других отделений должен
проходить в операционный блок через
санитарные пропускники, с соблюдением
всех требований санитарной обработки.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Медицинский инструментарий многократного назначения в процессе использования в лечебных и поликлинических учреждениях должен после каждого пациента подвергаться дезинфекционной очистке и стерилизации. Перед этапом стерилизации проводится предстерилизационная обработка инструментов с помощью моющего раствора определённой концентрации. Основная цель предварительной обработки — добиться удаления жировых и белковых отложений с поверхности предметов. После выдержки в моющем растворе инструменты промываются в проточной воде из-под крана и затем в дистиллированной. Постановка азопирамовой и фенолфталеиновой пробы проводится для оценки качества очистки и по СанПину должна проводиться перед каждым этапом стерилизации. Фенолфталеиновая проба определяет наличие остатков моющих веществ. Азопирамовая проводится с целью выявления хлорсодержащих компонентов, остатков крови, ржавчины, кислот.
В медицинских учреждениях для азопирамовой пробы приобретается аптечный раствор, который перед использованием смешивается с перекисью водорода. Оценка реакции определяется путём нанесения нескольких капель на поверхность инструмента, на сложные соединения деталей обрабатываемых приборов, в иглы шприцов. Инструмент держится над белым тампоном, результат окрашивания определяется в течение одной минуты. Оценка реакции после этого срока считается недостоверной. В полостях, иглах, катетерах раствор оставляют на одну минуту, после чего выдавливают на тампон. Появившееся розово – фиолетовое окрашивание говорит о наличии остатков крови. Буроватое окрашивание реактива происходит при наличии на инструментах следов ржавчины, хлорсодержащих препаратов, окислителей.
Не всегда в медицинских учреждениях существует возможность приобрести азопирам готовый раствор, а процесс самостоятельного изготовления может быть не точен. В этом случае можно приобрести заводской набор реагентов, предназначенный для приготовления азопирама и хранящийся до 2-х месяцев. При необходимости с помощью этого раствора готовят рабочий, добавляя в него 3% аптечную перекись водорода. Соотношения перекиси и азопирама соблюдают 1:1.
Азопирам комплект винар состоит из флакона солянокислого анилина и флакона амидопирина. Приготовить рабочий раствор достаточно просто, для этого анилин смешивается с амидопирином, и полученная масса доводится до 100 миллилитров этиловым спиртом в 95%. Полученного флакона хватает примерно на 6000 исследований, при условии использования за один раз 1-2-х миллилитров. Приготовленный раствор хранится в холодильнике до 2-х месяцев, при комнатной температуре в тёмном месте до одного месяца.
Постановка фенолфталеиновой и азопирамовой пробы проводится на одном проценте инструментов, подвергшихся предстерилизационной очистке, но при любом количестве исследуемых предметов их не должно быть меньше 3-5 штук. Результаты проведения проб заносятся в специально оформленные журналы с указанием даты, времени, количества инструментов и наличии реакции. Несоблюдение проведения проб может привести к возникновению аллергий разной степени тяжести, а при использовании инструментов в хирургии и на станциях переливания крови и к пирогенным реакциям организма.
В современных условиях высокого уровня инфицированности населения возбудителями гемоконтактных инфекций особенно актуальной является проблема обеспечения безопасности пациентов и персонала лечебно-профилактических организаций. Медицинская помощь сопряжена с необходимостью проведения многочисленных инвазивных манипуляций, при этом технологии не всегда позволяют использовать одноразовый медицинский инструментарий.
Как известно, инфицированные инструменты и материалы являются приоритетными факторами передачи гемоконтактных инфекций. Снижение риска заражения достигается применением одноразовых расходных материалов, а также путем трехступенчатой обработки медицинских изделий многоразового использования (дезинфекция, предстерилизационная очистка, стерилизация).
Извлечение
из СанПиН 2.1.3.2630-10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность»[1]
<…>
II. Организация дезинфекционных и стерилизационных мероприятий в организациях, осуществляющих медицинскую деятельность
<…>
2.1. Медицинские изделия многократного применения подлежат последовательно: дезинфекции, предстерилизационной очистке, стерилизации, последующему хранению в условиях, исключающих вторичную контаминацию микроорганизмами.
<…>
Наиболее критичным этапом обработки является предстерилизационная очистка, предусматривающая непосредственный контакт персонала с изделием. Именно на этом этапе довольно часто возникают аварийные ситуации (уколы, порезы), которыми нередко пренебрегают, поэтому не принимают экстренных мер профилактики. Однако инструментарий, прошедший только один этап обработки — дезинфекцию, не является биологически безопасным. Докажем это утверждение, перечислив типичные ошибки, допускаемые при дезинфекции:
•использование неразрешенных к применению средств и методов дезинфекции (на средство не оформлена необходимая разрешительная документация либо оно не может использоваться в лечебно-профилактических организациях, является фальсификатом и др.);
•нарушение условий хранения и транспортировки дезинфекционных средств (несоблюдение температурного режима хранения, воздействие прямых солнечных лучей, истекший срок годности исходного препарата и др.);
•неправильный выбор средства дезинфекции (не предназначено для уничтожения возбудителей вирусных гепатитов В, С и ВИЧ);
•неправильно выбранный режим дезинфекции (не обеспечивает гибель возбудителей гемоконтактных инфекций);
•некорректно проведенная дезинфекция (при изготовлении раствора дезинфектанта допущена ошибка в расчете концентрации, не выдержано время экспозиции, истек срок годности рабочего раствора и др.).
Извлечение
из СП 3.5.1378-03 «Санитарно-эпидемиологические требования
к организации и осуществлению дезинфекционной деятельности»[2]
<…>
III. Требования к осуществлению дезинфекционной деятельности
<…>
3.6.5. Не допускается применение для обеззараживания изделий медицинского назначения дезинфицирующих средств, не обладающих вирулицидным действием.
<…>
Наличие одной или нескольких ошибок сводит качество дезинфекции практически к нулю, как следствие, на этапе предстерилизационной очистки персонал имеет дело с опасным в биологическом плане инструментарием.
Кроме того, риск заражения персонала на втором этапе обработки инструментария обусловлен следующими факторами:
•непосредственный контакт персонала с медицинскими изделиями. В большей степени это относится к очистке вручную, однако и при механизации процесса персонал контактирует с изделиями при их перекладывании и сортировке;
•пренебрежение средствами индивидуальной защиты, в первую очередь перчатками.
Еще одна проблема связана с недостаточной информированностью персонала. Большинство современных средств дезинфекции содержат моющий компонент и предназначаются для проведения дезинфекции, совмещенной с предстерилизационной очисткой. Однако это не значит, что при погружении в раствор такого средства изделие одновременно проходит два этапа обработки. По окончании времени дезинфекции обязательно должна быть проведена очистка каждого изделия ручным или механизированным способом. Ручной способ подразумевает обработку каждого изделия в моющем растворе ершом или ватно-марлевым тампоном в течение 0,5–1 минуты. Механизированная очистка осуществляется с использованием специального оборудования, разрешенного к применению на территории Российской Федерации, имеющего сертификат соответствия и инструкцию по эксплуатации.
В чем же заключается суть совмещения дезинфекции с предстерилизационной очисткой? Ответ прост: между двумя этапами не требуется смена раствора дезинфектанта, содержащего моющий компонент. Иными словами, предстерилизацияонная очистка изделий осуществляется в том же растворе, в котором проводилась их дезинфекция. Все это, как правило, отражается в инструкции по применению средств дезинфекции, однако на практике ошибки в совмещении двух этапов обработки все же встречаются.
На схемах 1, 2, 3 представлены этапы предстерилизационной очистки, осуществляемой ручным способом, а также совмещенной с дезинфекцией.
Схема 1. Этапы проведения предстерилизационной очистки ручным способом[3]
|
1-й этап |
⇒ |
Промывание проточной водой после дезинфекции |
|
2-й этап |
⇒ |
Замачивание в моющем растворе при полном погружении изделия в разобранном виде с заполнением всех каналов и полостей на 15–60 минут в зависимости от применяемого средства |
|
3-й этап |
⇒ |
Мойка каждого изделия в моющем растворе ершом или ватно-марлевым тампоном в течение 0,5–1 минуты (обращаем внимание на температуру раствора моющего средства, если данное условие оговаривается в инструкции по применению моющего средства) |
|
4-й этап |
⇒ |
Ополаскивание проточной водой в течение времени, предусмотренного инструкцией к применяемому средству (раковина для ополаскивания инструментов не должна применяться для мытья рук медицинского персонала) |
|
5-й этап |
⇒ |
Ополаскивание дистиллированной водой с последующей сушкой горячим воздухом |
Схема 2. Этапы проведения предстерилизационной очистки, совмещенной с дезинфекцией, ручным способом
|
1-й этап |
⇒ |
Замачивание в растворе средства, обладающего дезинфицирующими и моющими свойствами |
|
2-й этап |
⇒ |
Мойка каждого изделия в моющем растворе ершом или ватно-марлевым тампоном в течение 0,5–1 минуты (обращаем внимание на температуру раствора, если данное условие оговаривается в инструкции по применению средства) |
|
3-й этап |
⇒ |
Ополаскивание проточной водой в течение времени, предусмотренного инструкцией к применяемому средству (раковина для ополаскивания инструментов не должна применяться для мытья рук медицинского персонала) |
|
4-й этап |
⇒ |
Ополаскивание дистиллированной водой с последующей сушкой горячим воздухом |
Схема 3. Этапы проведения предстерилизационной очистки, совмещенной с дезинфекцией, механизированным способом
|
1-й этап |
⇒ |
Помещение изделий в оборудование, предназначенное для дезинфекции и предстерилизационной очистки. Используются средства дезинфекции с моющим эффектом; или отдельно средства дезинфекции и моющие средства; или только моющие средства, а дезинфекция осуществляется термическим способом; или другое в соответствии с инструкцией по эксплуатации оборудования |
|
2-й этап |
⇒ |
Ополаскивание проточной водой в течение времени, предусмотренного инструкцией к применяемому средству. Режим использования может быть включен в цикл работы оборудования |
|
3-й этап |
⇒ |
Ополаскивание дистиллированной водой с последующей сушкой горячим воздухом. Режим ополаскивания дистиллированной водой и сушки может быть включен в цикл работы оборудования |
Наиболее перспективной является предстерилизационная очистка механизированным способом, среди преимуществ которой:
•сокращение тактильного контакта рук медицинского персонала с обрабатываемым инструментарием (биологическая безопасность персонала);
•сокращение времени обработки большого объема медицинских изделий (экономическая эффективность);
•предотвращение повреждения дорогостоящих изделий и инструментов, увеличение срока их службы (экономическая эффективность);
•значительное улучшение качества очистки медицинских инструментов и изделий сложной конфигурации (биологическая безопасность пациента).
В настоящее время на территории Российской Федерации зарегистрировано два существенно отличающихся друг от друга типа оборудования для предстерилизационной очистки. Первый основан на применении ультразвука, второй представлен так называемыми термодезинфекторами, в которых дезинфекция осуществляется термическим методом, а предстерилизационная очистка производится с использованием моющих средств, как правило, не содержащих дезинфекционного компонента. Преимуществом использования второго типа оборудования является обеспечение полного цикла дезинфекционно-предстерилизационных мероприятий, поскольку термодезинфектор последовательно производит дезинфекцию, очистку, ополаскивание и сушку изделий. От персонала лишь требуется правильно осуществить загрузку и извлечение инструментария.
Важный момент — выбор средств для предстерилизационной очистки. Современный рынок предлагает нам два принципиально разных подхода. Первый предполагает использование моющих средств на основе поверхностно-активных веществ (ПАВ), второй — на основе ферментов. Препараты обеих групп зарегистрированы на российском рынке. Наиболее широкое применение нашли средства для предстерилизационной очистки на основе ПАВ, обладающие высокими моющими свойствами. К недостаткам таких средств относятся:
•высокое пенообразование (при использовании механизированного способа предстерилизационной очистки этот фактор может быть критичным ввиду несовместимости оборудования с моющим средством);
•образование пленки на поверхности обрабатываемых изделий, что требует тщательного смывания препарата;
•достижение максимального моющего эффекта возможно лишь при определенной заданной температуре, что обуславливает необходимость поддержания температуры раствора при проведении предстерилизационной очистки.
Препараты на основе ферментов содержат бактериальные протеазы, которые способны разрушать не только клеточные стенки бактерий и белковые оболочки вирусов, но и биопленки. При этом такие моющие средства, как правило, активны при комнатной температуре и обладают низким пенообразованием. Широкое применение данных препаратов ограничивает более высокая стоимость по сравнению со средствами на основе ПАВ.
Контроль качества предстерилизационной очистки изделий медицинского назначения осуществляется посредством постановки азопирамовой (амидопириновой) и фенолфталеиновой проб. Наличие остаточных количеств крови оценивается с помощью азопирамовой или амидопириновой, моющих средств — фенолфталеиновой проб. Обратим внимание, что фенолфталеиновая проба работает только в щелочной среде и пригодна для контроля в том случае, если для предстерилизационной очистки использовалось моющее средство, pH которого более 8,5. Показатель pH, как правило, указывается в инструкции к каждому конкретному средству. Контроль качества предстерилизационной очистки изделий медицинского назначения является неотъемлемой частью системы производственного контроля, действующей в лечебно-профилактической организации. Документом, доказывающим факт проведения такого контроля, является журнал учета качества предстерилизационной обработки 
Извлечение
из СанПиН 2.1.3.2630-10
<…>
II. Организация дезинфекционных и стерилизационных мероприятий в организациях, осуществляющих медицинскую деятельность
<…>
2.14. Контроль качества предстерилизационной очистки проводят ежедневно. Контролю подлежат: в стерилизационной — 1 % от каждого наименования изделий, обработанных за смену; при децентрализованной обработке — 1 % одновременно обработанных изделий каждого наименования, но не менее трех единиц. Результаты контроля регистрируют в журнале.
<…>
Таким образом, от правильно организованной предстерилизационной обработки многоразового инструментария зависит биологическая безопасность как пациентов, так и персонала клиники. Повышению уровня безопасности способствует внедрение в практику новых средств, методов и технологий, которые существенно улучшают качество обработки изделий и сокращают контакт персонала с потенциально опасными изделиями. Контрольные мероприятия необходимо рассматривать как элемент системы менеджмента качества медицинской помощи, а не как рутинный процесс, которым можно пренебречь.
[1] Утверждены Постановлением Главного государственного санитарного врача РФ от 18.05.2010 № 58.
[2] Утверждены Постановлением Главного государственного санитарного врача РФ от 09.06.2003 № 131.
[3] В соответствии с ОСТ 42-21-2-85 «Стерилизация и дезинфекция изделий медицинского назначения. Методы, средства, режимы», введенным в действие Приказом Минздрава СССР от 10.06.1985 № 770.
Статья опубликована в журнале «Санэпидконтроль. Охрана труда» № 3, 2015.
Стерилизация и дезинфекция — важные этапы обработки инструментов и рабочих поверхностей, позволяющие сделать любые процедуры безопасными для пациентов.
Дезинфекция — это уничтожение патогенных и условно-патогенных микроорганизмов — вирусов, бактерий, грибов на инструментах и оборудовании до приемлемого санитарно-эпидемиологическими нормами уровня.
Стерилизация — это полное умерщвление микроорганизмов всех видов, включая споровые формы, на поверхностях и внутри изделий.
Для обеспечения всех санитарных норм и правил необходимо придерживаться СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней», а также СП 2.1.3678-20 «Санитарно-эпидемиологические требования к эксплуатации помещений, зданий, сооружений, оборудования и транспорта, а также условиям деятельности хозяйствующих субъектов, осуществляющих продажу товаров, выполнение работ или оказание услуг».
Врач обязательно должен работать в сопровождении среднего медицинского персонала, осуществляющего обработку рабочих мест, дезинфекцию, а также, в случае отсутствия централизованной стерилизационной, предстерилизационную очистку и стерилизацию медицинских изделий.
Дезинфекцию поверхностей предметов, находящихся в зоне лечения (столик для инструментов, кнопки управления, клавиатура, воздушный пистолет, светильник, плевательница, подголовник и подлокотники стоматологического кресла) проводят после каждого пациента. Для этих целей используют дезинфицирующие средства, разрешенные к применению в присутствии пациентов, обладающие широким спектром антимикробного действия.
Все одноразовые инструменты и расходные материалы после каждого пациента собираются и утилизируются как отходы класса Б.
Стерилизации подвергают все многоразовые инструменты и изделия, контактирующие с раневой поверхностью, со слизистой оболочкой, кровью или инъекционными препаратами.
Стерилизационная обработка инструментов и других медицинских изделий в обязательном порядке включает в себя следующие этапы:
- Дезинфекция
- Предстерилизационная очистка
- Сушка
- Стерилизация
- Хранение
Этап №1. Дезинфекция
Инструменты необходимо аккуратно поместить в дезинфицирующий раствор. Перед дезинфекцией все инструменты или приборы раскрывают, раскручивают сложные механизмы и затем погружают в дезинфицирующий раствор. Необходимо обратить внимание, чтобы на поверхностях не осталось пузырьков воздуха или пустот, препятствующих попаданию средства. При погружении в дезраствор замковых инструментов (щипцы, кусачки, ножницы и т.п.) следует сделать ими несколько рабочих движений в дезрастворе.
Жидкость должна покрывать инструменты на 1-2 см над ними для должной обработки.
Дезинфицирующие средства должны иметь широкий спектр воздействия в отношении бактерий, вирусов и грибов.
Качественные дезинфицирующие средства должны содержать антикоррозийные добавки, чтобы не повреждать инструменты.
Емкости с готовыми или приготовленными растворами должны иметь крышки и стикеры с названием дезинфицирующего средства, концентрацией и датой приготовления раствора. При приготовлении нового дезинфицирующего раствора стикер на емкости заполняется соответствующими данными.
Следует контролировать правильность приготовления дезинфицирующий раствора и сохранение его дезинфицирующих свойств до конца срока использования, который прописывается на этикетке при приготовлении раствора, либо до выпадения осадка. Для этой цели служат специальные индикаторы (тест-полоски), с помощью которых можно быстро и оперативно определить пригодность дезинфицирующего раствора к применению. Индикатор необходимо применять сразу после приготовления дезраствора, чтобы убедиться, что раствор приготовлен в правильной концентрации, а также осуществлять периодический контроль этого раствора для подтверждения, что он не утратил своих дезинфицирующих свойств. Для каждого дезсредства применяются свои индикаторы, смотрите инструкцию к дезсредству и индикаторам.
Обратите внимание, что стоматологические наконечники нельзя дезинфицировать методом погружения, только методом протирания. Про обработку наконечников мы поговорим далее отдельно.
Этап №2. Предстерилизационная очистка (ПСО)
После завершения времени дезинфекционной выдержки, проводят мойку каждого изделия в том же растворе, в котором проводили замачивание, с помощью ерша, ватно-марлевого тампона или тканевой (марлевой) салфетки, после чего ополаскивают проточной водой, либо проводят чистку в ультразвуковой мойке. Смывается не только грязь и мелкие частицы, но и само дезинфицирующее средство, которое портит инструменты при длительном воздействии.
Изделия с ребристой поверхностью (например, алмазные боры) и полостями обязательно должны проходить очистку в ультразвуковой мойке, при этом очищаются самые мелкие щели на инструментах и их полости.
После этого инструменты необходимо промыть дистиллированной водой, чтобы смыть с них остатки проточной воды. Если этого не сделать, то во время стерилизации, которая является следующим этапом, на инструментах будет осаждаться известковый налет от минеральных остатков проточной воды, со временем это приведет к ухудшению качества инструментов, а также будет препятствовать качественной дезинфекции и стерилизации.
При качественно проведенной ПСО на инструментах не должно остаться никаких биологических тканей и дезраствор должен также полностью смыться. Для оценки качества ПСО применяется азопирамовая проба, для ее проведения берется не менее 1% инструмента, прошедшего одновременную процедуру очистки, а если инструментов не много, то не менее 3 инструментов разного вида. Если азопирамовая проба показала наличие остатков биологических тканей или дезсредства, то все инструменты подлежат повторной дезинфекции и ПСО. Если азопирамовая проба не показала наличие остатков биологических тканей или дезсредства, то инструменты допускаются к дальнейшей обработке. Также необходимо провести фенолфталеиновую пробу, если это указано в инструкции к используемому дезсредству.
Этап №3. Сушка
После качественно проведенной ПСО инструменты необходимо тщательно высушить перед стерилизацией. Для этого их раскладывают в разобранном и раскрытом виде на чистой сухой салфетке и сушат до исчезновения видимой влаги, либо используют для этой цели специальные аппараты, ускоряющие сушку, например, сушильный бокс «РЭЛМА-БС-500», либо сушильный шкаф.
Нельзя подвергать стерилизации непросушенный инструмент!
После тщательной сушки инструменты направляются на стерилизацию.
Обработка стоматологических наконечников.
Процесс ручной обработки стоматологических наконечников проходит в несколько этапов:
- Промывают канал наконечника водой (при помощи мандренов или иных устройств) и затем продувают воздухом.
- Отсоединяют наконечник от стоматологической установки, протирают наружные поверхности салфеткой, смоченной водой до удаления видимых загрязнений.
- Обрабатывают наружные поверхности наконечника специальными дезинфицирующими средствами, разрешенными к применению для этих целей (с учетом рекомендаций фирмы — производителя наконечника).
- Разбирают разъемные части наконечника и вынимают инструмент (бор, фрезу, диск и т.д.).
- Смазывают наконечник специальными смазками, предназначенными для этих целей. Удаляют остатки смазки протиранием чистой салфеткой.
Все операции по промывке, продувке и смазке можно проводить вручную, но предпочтительно использовать аппараты для чистки и смазки, т.к. в них происходит более тщательная обработка наконечников. Перед загрузкой в такие аппараты, наконечники также необходимо протереть чистой влажной салфеткой для удаления видимых загрязнений и обработать салфеткой, смоченной специальным дезинфицирующим средством.
Далее наконечники направляются на стерилизацию.
Этап №4. Стерилизация
После прохождения всех предыдущих этапов стоматологические инструменты (в том числе наконечники) готовы к стерилизации.
Стерилизация может осуществляться в упакованном виде, при этом инструменты размещают в индивидуальные одноразовые или многоразовые упаковки.
Также стерилизация может проходить в неупакованном виде, при этом инструменты должны быть сразу использованы по назначению, либо могут храниться в УФ-камере в течение срока, указанного в инструкции к УФ-камере.
Для стерилизации стоматологических инструментов рекомендуется использовать паровой стерилизатор – автоклав и инфракрасный стерилизатор (ИК-стерилизатор).
Стерилизация в автоклаве происходит благодаря воздействию пара и высокой температуры (от 121 до 134°С, при давлении 1,1-2,1 кгс/см2 ). Полный цикл стерилизации (нагрев-предварительное удаление воздуха-стерилизация-сушка) занимает около 25-50 минут (в зависимости от выбранного режима стерилизации). Для работы автоклава используется дистиллированная вода.
В автоклаве стерилизуют изделия из коррозионно-стойких металлов, стекла, изделия из текстиля (132-134°С), при температуре 120°С изделия из резин, латекса, отдельных видов пластмасс.
При этом нужно понимать, что насыщенный пар под высоким давлением – это достаточно агрессивный химический агент, который оказывает коррозионное воздействие на металлы. В инструкции к некоторым стоматологическим инструментам даже специально указывают, что их не рекомендуется автоклавировать, хотя эти инструменты выполнены из нержавеющей стали. То же самое касается инструментов, имеющих режущие кромки (особенно много их в ортодонтии), они достаточно быстро тупятся при стерилизации в автоклаве. Потому для стерилизации подобных инструментов рекомендуется использовать ИК-стерилизатор, который производит стерилизацию наиболее щадящим образом за счет кратковременного теплового воздействия и отсутствия агрессивных химических агентов.
В ИК-стерилизаторах используется экологически безопасный термический агент — лучистая энергия оптического диапазона (мощное видимое и инфракрасное импульсное воздействие). При данном способе передачи тепловой энергии нагрев стерилизуемых изделий происходит быстро и эффективно. Стерилизация длится от 4 до 10 мин. Стерилизуются изделия из металлов и стекла.
Более подробно об ИК-стерилизаторе читайте в нашей следующей статье.
Для контроля режимов стерилизации обязательно при каждом цикле стерилизации нужно использовать химические индикаторы, которые раскладывают внутри камеры стерилизатора и закладывают внутрь каждой упаковки (если стерилизуется в упакованном виде).
Этап №5. Хранение
Если инструменты стерилизовались в упакованном виде (крафт-пакеты, контейнеры и т.д.), то они сохраняют стерильность в течение срока, указанного в инструкции к упаковке при соблюдении необходимых условий хранения (место хранения должно быть чистым и сухим, без условий, которые могут приводить к образованию конденсата).
Если инструменты стерилизовались в неупакованном виде, то их нужно либо сразу использовать по назначению (в течение 1 часа после извлечения из стерилизатора), либо хранить в специальной ультрафиолетовой камере (УФ-камере) в течение времени, указанного в инструкции к УФ-камере.
Обратите внимание, что в УФ-камере нельзя хранить инструменты в упаковках, которые имеют прозрачную пленку, т.к. эта пленка разрушается под воздействием УФ-излучения.