Содержание
-
Русское название
-
Английское название
-
Латинское название
-
Фармакологическая группа вещества Авелумаб
-
Нозологическая классификация
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Авелумаб
-
Противопоказания
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Авелумаб
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Авелумаб
Русское название
Авелумаб
Английское название
Avelumab
Латинское название
Avelumabum (род. Avelumabi)
Фармакологическая группа вещества Авелумаб
Нозологическая классификация
Фармакологическое действие
—
противоопухолевое.
Характеристика
Человеческое моноклональное антитело IgG1.
Фармакология
Фармакодинамика
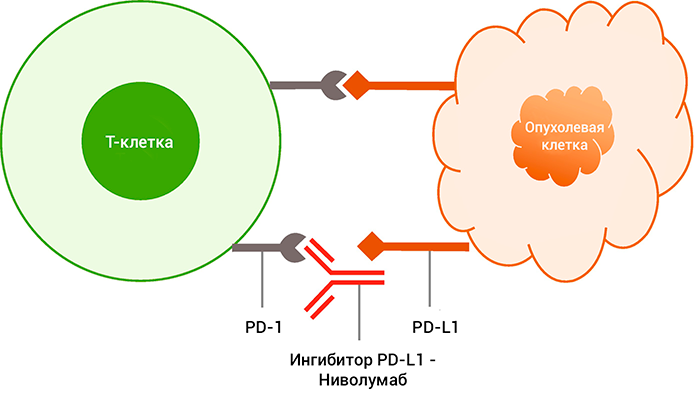
Действие авелумаба направлено против лиганда программируемой клеточной смерти 1 (PD-L1). Авелумаб непосредственно связывается с PD-L1 и блокирует его взаимодействие с рецепторами PD-1 и В7.1. Таким образом, авелумаб устраняет подавляющие эффекты PD-L1 в отношении цитотоксических Т-лимфоцитов CD8+, что приводит к восстановлению противоопухолевого Т-клеточного ответа. Авелумаб индуцирует опосредуемый натуральными клетками киллерами прямой лизис клетки опухоли с помощью активации антителозависимой клеточно-опосредованной цитотоксичности.
Фармакокинетика
Распределение
Авелумаб распределяется в общем кровотоке и в меньшей степени — во внеклеточном пространстве. В связи с ограниченным внесосудистым распределением Vss является небольшим и составляет 4,72 л. Как и для других антител, для авелумаба не характерно специфическое связывание с белками плазмы.
Выведение
Общий системный клиренс составляет 0,59 л/день. Согласно результатам анализа, общий системный клиренс авелумаба снижается с течением времени, наиболее выраженное среднее максимальное снижение по сравнению с исходным состоянием среди разных типов опухолей составляло приблизительно 32,1% (коэффициент вариации 36,2%).
Css авелумаба достигалась приблизительно через 4–6 нед (2–3 цикла) повторного применения в дозе 10 мг/кг каждые 2 нед с системным накоплением примерно в 1,25 раза. Т1/2 при рекомендуемой дозе составляет 6,1 дня, по данным популяционного фармакокинетического анализа
Особые группы пациентов
Результаты популяционного фармакокинетического анализа свидетельствуют об отсутствии различий в общем системном клиренсе авелумаба в зависимости от возраста, пола, расовой принадлежности, статуса PD-L1, опухолевой нагрузки, нарушения функции почек и наличия печеночной недостаточности легкой или средней степени тяжести.
Общий системный клиренс повышался по мере увеличения массы тела. Экспозиция в равновесном состоянии была практически одинаковой в широком диапазоне показателей массы тела (30–204 кг) при нормализации дозы в соответствии с массой тела.
Нарушение функции почек. В ходе исследований не было выявлено клинически значимых различий в клиренсе авелумаба между пациентами с легкой (СКФ 60–89 мл/мин по формуле Кокрофта-Голта, n=623), умеренной (СКФ 30–59 мл/мин, n=320) почечной недостаточностью и нормальной (СКФ >90 мл/мин, n=671) функцией почек. У пациентов с тяжелой почечной недостаточностью (СКФ 15–29 мл/мин) применение авелумаба не изучалось.
Нарушение функции печени. В популяционном фармакокинетическом анализе не было выявлено клинически значимых различий в клиренсе авелумаба между пациентами с печеночной недостаточностью легкой (билирубин ≥ВГН или ACT >ВГН, или билирубин в 1–1,5 раза выше ВГН, n=217) степени и пациентами с нормальной функцией печени (билирубин и ACT ≥ВГН, n= 1388). Печеночная недостаточность устанавливалась в соответствии с критериями нарушения функции печени Национального института рака (NCI). У пациентов с печеночной недостаточностью средней (уровень билирубина в 1,5–3 раза выше ВГН) и тяжелой (уровень билирубина в >3 раза выше ВГН) степени применение авелумаба не изучалось.
Применение вещества Авелумаб
Монотерапия метастатической карциномы Меркеля у взрослых ранее леченных пациентов.
Противопоказания
Гиперчувствительность к авелумабу; нарушение функции почек и печени тяжелой степени тяжести; детский возраст до 18 лет.
Применение при беременности и кормлении грудью
Данные относительно применения авелумаба у беременных женщин ограничены или отсутствуют.
Исследования по влиянию авелумаба на репродуктивную функцию у животных не проводились. Тем не менее в моделях у беременных мышей было обнаружено, что ингибирование пути PD-L1/PD-1 приводит к снижению толерантности материнского организма к тканям плода, что сопровождается повышением частоты выкидышей. Эти результаты указывают на риск того, что применение авелумаба во время беременности может оказать неблагоприятное воздействие на плод, включая повышение частоты выкидышей и мертворожденных детей. Известно, что IgG1 человека проникают через плацентарный барьер. В связи с этим существует возможность проникновения авелумаба из организма матери в развивающийся плод. Авелумаб не рекомендуется применять во время беременности, за исключением тех случаев, когда клиническое состояние женщины требует его назначения.
Отсутствуют данные по секреции авелумаба в грудное молоко. Поскольку известно, что антитела могут секретироваться в грудное молоко, нельзя исключить риск для новорожденных и детей грудного возраста. Кормящим женщинам рекомендуется прекратить грудное вскармливание на время лечения авелумабом и минимум на 1 мес после введения последней дозы в связи с возможностью развития серьезных нежелательных реакций у детей грудного возраста.
Побочные действия вещества Авелумаб
Применение авелумаба чаще всего сопровождается развитием иммуноопосредованных нежелательных реакций. Большинство из них, в т.ч. выраженной степени тяжести, разрешались после назначения соответствующей медикаментозной терапии или отмены авелумаба.
Безопасность авелумаба оценивалась в клинических исследованиях у пациентов с сóлидными опухолями, в т.ч. метастатической карциномой Меркеля (МКМ), которые получали его в дозе 10 мг/кг каждые 2 нед. В этой популяции пациентов наиболее частыми нежелательными реакциями на фоне применения авелумаба были утомляемость, тошнота, диарея, снижение аппетита, запор, инфузионные реакции, снижение массы тела и рвота. Наиболее частыми нежелательными реакциями ≥3-й степени тяжести были анемия, одышка и боль в животе. Серьезными нежелательными реакциями были иммуноопосредованные и инфузионные реакции.
Ниже представлены объединенные данные о нежелательных реакциях. Частота нежелательных реакций классифицирована как очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000).
Со стороны крови и лимфатической системы: очень часто — анемия; часто — лимфопения; нечасто — тромбоцитопения, эозинофилия1.
Со стороны иммунной системы: нечасто — лекарственная реакция гиперчувствительности, анафилактическая реакция гиперчувствительности, реакция гиперчувствительности.
Со стороны эндокринной системы: часто — гипотиреоз2; нечасто — надпочечниковая недостаточность2, гипертиреоз2, аутоиммунный гипотиреоз2, тиреоидит2, аутоиммунный тиреоидит, острая недостаточность коры надпочечников2, недостаточность функции гипофиза2 сахарный диабет2, сахарный диабет типа 12.
Со стороны нервной системы: часто — головная боль, головокружение, периферическая нейропатия; нечасто — синдром Гийена-Барре2.
Со стороны органа зрения: нечасто — увеит2.
Со стороны ССС: редко — миокардит2; часто — гипертензия, гипотензия.
Со стороны дыхательной системы, органов грудной клетки и средостения: очень часто — кашель, одышка; часто — пневмонит2.
Со стороны ЖКТ: очень часто — тошнота, снижение аппетита, диарея, запор, рвота, боль в животе; часто — сухость во рту; нечасто — колит2, аутоиммунный колит2, энтероколит2, кишечная непроходимость.
Со стороны печени и желчевыводящих путей: нечасто — аутоиммунный гепатит2, острая печеночная недостаточность2, печеночная недостаточность2, гепатит2.
Со стороны кожи подкожных тканей: часто — сыпь2, зуд2, пятнисто-папулезная сыпь2, сухость кожи; нечасто — зудящая сыпь2, гиперемия кожи, эритема2, генерализованная сыпь2, псориаз2, эритематозная сыпь2, пятнистая сыпь2, папулезная сыпь2, эксфолиативный дерматит2, полиморфная эритема2, пемфигоид2, генерализованный зуд2, экзема, дерматит.
Со стороны костно-мышечной системы и соединительной ткани: очень часто — боль в спине, артралгия; часто — миалгия; нечасто — миозит2.
Со стороны почек и мочевыводящих путей: нечасто — тубулоинтерстициальный нефрит2.
Общие расстройства и нарушения в месте введения: очень часто — утомляемость, повышение температуры тела, периферический отек; часто — астения, озноб, гриппоподобное заболевание; нечасто — синдром системной воспалительной реакции2.
Влияние на результаты лабораторных и инструментальных исследований: очень часто — снижение массы тела; часто — повышение уровня ГГТ, ЩФ, амилазы, липазы, креатинина крови; нечасто — повышение уровня ACT2, АЛТ2, КФК2, трансаминаз2.
Травмы. интоксикации и осложнения манипуляции: очень часто — инфузионные реакции.
1 Частота нежелательных реакций была установлена в клиническом исследовании EMR 100070-003 (часть В) после завершения сбора данных для объединенного анализа.
2 Иммуноопосредованные нежелательные реакции на основании медицинского анализа.
Описание отдельных нежелательных реакций
Данные относительно описанных ниже иммуноопосредованных нежелательных реакций основаны на результатах клинических исследований, полученных у пациентов с другими сóлидными опухолями, получавших авелумаб.
Иммуноопосредованный пневмонит
В клинических исследованиях иммуноопосредованный пневмонит развился у 1,2% пациентов. Из этих пациентов у одного (0,1%) зарегистрирован летальный исход. У одного пациента (0,1%) развился пневмонит 4-й и у 5 пациентов (0,3%) 3-й степени тяжести.
Медиана времени до начала проявления признаков пневмонита составляла 2,5 мес (диапазон 3 дня—11 мес). Медиана длительности течения пневмонита составила 7 нед (диапазон от 4 дней до более 4 мес).
У 0,3% пациентов пневмонит стал причиной отмены авелумаба. Все 21 пациент с иммуноопосредованным пневмонитом получали лечение ГКС, 17 (81%) из них получали высокие дозы ГКС в течение периода времени, медиана которого составляла 8 дней (диапазон 1 день—2,3 мес). Иммуноопосредованный пневмонит разрешился у 12 (57%) из 21 пациента на момент прекращения сбора данных.
Иммуноопосредованный гепатит
В клинических исследованиях иммуноопосредованный гепатит развился у 0,9% пациентов. Из них у 2 (0,1%) пациентов был зарегистрирован летальный исход. У 11 (0,6%) развился иммуноопосредованный гепатит 3-й степени. Медиана времени до начала проявления признаков гепатита составляла 3,2 мес (диапазон 1 нед—15 мес). Медиана длительности течения гепатита составила 2,5 мес (диапазон от 1 дня до более 7,4 мес). У 0,5% пациентов гепатит стал причиной отмены авелумаба. Все 16 пациентов с иммуноопосредованным гепатитом получали лечение ГКС, 15 (94%) из них получали высокие дозы ГКС в течение периода времени, медиана которого составляла 14 дней (диапазон 1 день—2,5 мес). Иммуноопосредованный гепатит разрешился у 9 (56%) из 16 пациентов на момент прекращения сбора данных.
Иммуноопосредованный колит
В клинических исследованиях иммуноопосредованный колит развился у 1,5% пациентов. Из них у 7 (0,4%) развился иммуноопосредованный колит 3-й степени. Медиана времени до начала проявления признаков колита составляла 2,1 мес (диапазон 2 дня—11 мес). Медиана длительности течения колита составила 6 нед (диапазон от 1 дня до более 14 мес). У 0,5% пациентов колит стал причиной отмены авелумаба. Все 26 пациентов с иммуноопосредованным колитом получали лечение ГКС, 15 (58%) из них получали высокие дозы ГКС в течение периода времени, медиана которого составляла 19 дней (диапазон 1 день—2,3 мес). Иммуноопосредованный колит разрешился у 18 (70%) из 26 пациентов на момент прекращения сбора данных.
Иммуноопосредованные эндокринопатии
Заболевания щитовидной железы. В клинических исследованиях иммуноопосредованные нарушения функции щитовидной железы развились у 6% пациентов. Из них у 90 (5%) пациентов развился гипотиреоз, у 7 (0,4%) — гипертиреоз, у 4 (0,2%) — тиреоидит. Из этих пациентов у 3 (0,2%) были зарегистрированы иммуноопосредованные нарушения функции щитовидной железы 3-й степени. Медиана времени до начала проявления признаков нарушений функции щитовидной железы составляла 2,8 мес (диапазон 2 нед—13 мес). Медиана длительности была неопределяемой (диапазон от 1 дня до более 26 мес). У 0,1% пациентов нарушение функции щитовидной железы стало причиной отмены авелумаба. Нарушения функции щитовидной железы разрешились у 7 (7%) из 98 пациентов на момент прекращения сбора данных.
Надпочечниковая недостаточность. В клинических исследованиях иммуноопосредованная недостаточность надпочечников развилась у 0,5% пациентов. Из них у 1 (0,1%) пациента была зарегистрирована недостаточность надпочечников 3-й степени. Медиана времени до начала проявления признаков недостаточности надпочечников составляла 2,5 мес (диапазон 1 день— 8 мес). Медиана длительности течения была неопределяемой (диапазон от 2 дней до более 6 мес). У 0,1% пациентов, недостаточность надпочечников стала причиной отмены авелумаба. Все 8 пациентов с иммуноопосредованной недостаточностью надпочечников получали ГКС, 4 из 8 пациентов (50%) получали высокие дозы системных ГКС (>40 мг преднизона или эквивалентную дозу другого ЛС) с последующим снижением с медианой времени 1 день (диапазон 1 день—24 дня). У 1 пациента недостаточность надпочечников разрешилась на фоне терапии ГКС на момент завершения сбора данных.
Сахарный диабет типа 1. Сахарный диабет типа 1 альтернативной этиологии развился у 0,1% пациентов, включая 2 реакции 3-й степени, которые стали причиной отмены авелумаба.
Иммуноопосредованный нефрит и нарушение функции почек
У 0,1% пациентов иммуноопосредованный нефрит стал причиной отмены авелумаба.
Иммуногенность
Из 1738 пациентов, получавших авелумаб в дозе 10 мг/кг в виде в/в инфузий каждые 2 нед, 1627 были обследованы на наличие антител. У 96 (5,9%) из них были получены положительные результаты. У положительных пациентов возможно повышение риска развития инфузионных реакций (около 40% и 25% у пациентов, у которых хоть раз были выявлены или никогда не выявлялись антитела к авелумабу соответственно). На основании имеющихся данных, включая низкую частоту иммуногенности, влияние антител к авелумабу на фармакокинетику, эффективность и безопасность не определено, при этом воздействие нейтрализующих антител неизвестно.
Взаимодействие
Отдельных исследований взаимодействия авелумаба с другими ЛС не проводилось. Поскольку авелумаб выводится посредством катаболизма, ФКВ с другими ЛС не ожидается.
Передозировка
У троих пациентов было зарегистрировано увеличение дозы авелумаба на 5 и 10%. У пациентов отсутствовали симптомы, не требовалось лечения передозировки, и они продолжили терапию.
Лечение: в случае передозировки следует тщательно наблюдать за состоянием пациентов для выявления симптомов развития нежелательных реакций. Лечение направлено на устранение симптомов.
Способ применения и дозы
В/в, в виде инфузии в течение 60 мин, каждые 2 нед.
Меры предосторожности
Инфузионные реакции
У пациентов, получавших авелумаб, были зарегистрированы инфузионные реакции, часть из которых были тяжелыми. У пациентов следует контролировать появление симптомов и признаков развития инфузионных реакций, в т.ч. повышение температуры тела, озноб, покраснение кожи, снижение АД, появление одышки, свистящего дыхания, боль в спине, боль в животе и сыпь. При развитии инфузионных реакций 3-й и 4-й степени тяжести следует прекратить инфузию и отменить авелумаб.
При развитии инфузионных реакций 1-й степени тяжести необходимо уменьшить скорость инфузии на 50%. У пациентов с инфузионными реакциями 2-й степени тяжести инфузию следует временно приостановить до снижения выраженности реакции до 1-й степени тяжести или ее разрешения. После этого инфузию следует возобновить, но скорость ее уменьшить на 50%.
В случае рецидива инфузионных реакций 1-й или 2-й степени тяжести пациент может продолжать получать авелумаб под тщательным наблюдением после коррекции скорости инфузии и проведения премедикации с помощью антигистаминных ЛС и парацетамола.
В клинических исследованиях у 98,6% пациентов с инфузионными реакциями первая реакция развилась в течение первых 4 инфузий, из них 2,7% реакций были ≥3-й степени тяжести. У остальных 1,4% пациентов инфузионные реакции возникали после первых 4 инфузий и были 1-й или 2-й степени тяжести.
Иммуноопосредованные реакции
Большинство иммуноопосредованных нежелательных реакций на фоне применения авелумаба были обратимыми и прекращались после кратковременного или длительного прерывания терапии, применения ГКС и/или поддерживающей терапии.
При подозрении на иммуноопосредованные нежелательные реакции следует провести полноценное обследование для подтверждения этиологии и исключения других причин. С учетом тяжести нежелательной реакции следует отменить авелумаб и назначить ГКС. Если для лечения нежелательной реакции применяются ГКС, дозу гормонов следует снижать в течение минимум 1 мес после улучшения. Если иммуноопосредованные реакции невозможно контролировать с помощью ГКС, необходимо рассмотреть возможность назначения других системных иммунодепрессантов.
Иммуноопосредованный пневмонит
У пациентов, получавших авелумаб, наблюдались случаи развития пневмонита, в т.ч. один с летальным исходом. У пациентов необходимо контролировать появление признаков и симптомов пневмонита и исключить другие причины, кроме пневмонита. При подозрении на пневмонит диагноз следует подтвердить с помощью рентгенографии. В случае развития пневмонита ≥2-й степени тяжести следует назначить ГКС (начальная доза 1–2 мг/кг/сут преднизона или другого ЛС в эквивалентной дозе с последующим постепенным снижением). Применение авелумаба следует временно прекратить при развитии пневмонита 2-й степени тяжести до устранения симптомов и полностью отменить при развитии пневмонита 3-й и 4-й степени тяжести или рецидиве пневмонита 2-й степени тяжести.
Иммуноопосредованный гепатит
У пациентов, получавших авелумаб, наблюдались случаи гепатита, в т.ч. два с летальным исходом. У пациентов необходимо контролировать появление признаков и симптомов изменения функции печени, появления симптомов гепатита и исключить другие причины кроме гепатита. В случае развития гепатита ≥2-й степени тяжести следует назначить ГКС (начальная доза 1–2 мг/кг/сут преднизона или другого ЛС в эквивалентной дозе с последующим постепенным снижением).
Применение авелумаба следует временно прекратить при развитии гепатита 2-й степени тяжести до его разрешения и полностью отменить при развитии гепатита 3-й и 4-й степени тяжести.
Иммуноопосредованный колит
У пациентов, получавших авелумаб, наблюдались случаи развития колита. У пациентов необходимо контролировать появление признаков и симптомов развития колита и исключить другие причины кроме колита. В случае развития колита ≥2-й степени тяжести следует назначить ГКС (начальная доза 1–2 мг/кг/сут преднизона или другого ЛС в эквивалентной дозе с последующим постепенным снижением). Применение авелумаба следует временно прекратить при развитии колита 2-й или 3-й степени тяжести до разрешения состояния и полностью отменить при развитии колита 4-й степени или рецидиве колита 3-й степени тяжести.
Иммуноопосредованные эндокринопатии
У пациентов, получавших авелумаб, наблюдались случаи нарушения функции щитовидной железы, недостаточности надпочечников и сахарного диабета типа 1.
У пациентов необходимо контролировать появление признаков и симптомов развития эндокринопатии. Авелумаб следует временно отменить при развитии эндокринопатии 3-й и 4-й степени тяжести до устранения симптомов.
Нарушение функции щитовидной железы (гипотиреоз, гипертиреоз). Нарушения функции щитовидной железы могут возникнуть в любое время в ходе лечения. Требуется наблюдение за изменениями функции щитовидной железы до начала терапии и периодически в ходе лечения (на основании данных клинического обследования), а также выявление симптомов и признаков заболеваний. При гипотиреозе применяют заместительную терапию, при гипертиреозе — антитиреоидные ЛС по мере необходимости.
Применение авелумаба следует временно прекратить при развитии нарушений функции щитовидной железы 3-й или 4-й степени тяжести.
Надпочечниковая недостаточность. У пациентов необходимо контролировать появление признаков и симптомов надпочечниковой недостаточности в процессе терапии и после ее завершения. При развитии надпочечниковой недостаточности ≥3-й степени тяжести следует назначить ГКС (1–2 мг/кг/сут преднизона в/в или эквивалентную дозу внутрь) с последующим постепенным снижением до достижения дозы 10 мг/сут или менее. При развитии надпочечниковой недостаточности 3-й или 4-й степени тяжести авелумаб следует временно отменить.
Сахарный диабет типа 1. Авелумаб может вызвать развитие сахарного диабета типа 1, включая диабетический кетоацидоз. У пациентов следует контролировать появление гипергликемии или других симптомов сахарного диабета. При развитии сахарного диабета типа 1 следует назначить инсулин. У пациентов с гипергликемией ≥3-й степени тяжести следует временно прервать терапию авелумабом и назначить гипогликемические ЛС. После достижения контроля гликемии на фоне применения заместительной терапии инсулином лечение авелумабом следует возобновить.
Иммуноопосредованный нефрит и нарушение функции почек
Авелумаб может вызвать развитие нефрита. У пациентов следует контролировать повышение уровня креатинина в сыворотке крови до начала терапии и периодически в ходе лечения. При нефрите ≥2-й степени тяжести следует назначить ГКС (начальная доза 1–2 мг/кг/сут преднизона или другого ЛС в эквивалентной дозе с последующим постепенным снижением). При развитии нефрита 2-й или 3-й степени тяжести терапию авелумабом следует временно прекратить до разрешения нефрита до ≥1-й степени, а при развитии нефрита 4-й степени тяжести авелумаб следует отменить.
Другие иммуноопосредованные нежелательные реакции
Другие клинически значимые нежелательные реакции были зарегистрированы менее чем у 1% пациентов и включали миокардит, в т.ч. с летальным исходом, миозит, недостаточность функции гипофиза, увеит и синдром Гийена-Барре. При подозрении на другие нежелательные реакции следует провести полноценное обследование для подтверждения этиологии и исключения других причин. С учетом тяжести других нежелательной реакций авелумаб следует отменить и назначить ГКС. При уменьшении выраженности других нежелательных реакций до 1-й степени тяжести или менее после снижения дозы ГКС следует возобновить терапию авелумабом. При развитии рецидивов других нежелательных реакций 3-й степени тяжести или развитии реакций 4-й степени тяжести авелумаб следует полностью отменить.
Пациенты, исключенные из клинических исследований
Пациенты, имеющие метастазы в ЦНС (активные или в анамнезе), аутоиммунные заболевания (активные или в анамнезе), другие злокачественные образования в течение предшествовавших 5 лет, состояния, требующие терапевтической иммуносупрессии, или активные инфекции ВИЧ, гепатит В или С и перенесшие трансплантацию органов, исключались из исследования.
Влияние на способность управлять транспортными средствами и механизмами. Авелумаб оказывает незначительное влияние на способность управлять транспортными средствами и механизмами. На фоне применения авелумаба была зарегистрирована утомляемость. Пациентам рекомендуется соблюдать осторожность при вождении автотранспорта или работе с механизмами, пока они не убедятся, что авелумаб не вызывает нежелательной реакции.
Источники информации
Обобщенные материалы www.grls.rosminzdrav.ru, 2019.
Торговые названия с действующим веществом Авелумаб
Фармакологическое действие
Противоопухолевое средство, человеческий иммуноглобулин G1 (IgGl), моноклональное антитело, направленное против лиганда программируемой клеточной смерти 1 (PDL1). Авелумаб непосредственно связывается с PD-L1 и блокирует его взаимодействие с рецепторами PD-1 и В7.1. Таким образом, авелумаб устраняет подавляющие эффекты PD-L1 в отношении цитотоксических Т лимфоцитов CD8+, что приводит к восстановлению противоопухолевого Т-клеточного ответа. Авелумаб индуцирует опосредуемый натуральными клетками киллерами (NK) прямой лизис клетки опухоли с помощью активации антитело-зависимой клеточно-опосредованной цитотоксичности (АЗКЦ).
Фармакокинетика
Авелумаб распределяется в общем кровотоке и в меньшей степени — во внеклеточном пространстве. Vd в равновесном состоянии составлял 4.72 л. В связи с ограниченным внесосудистым распределением Vd авелумаба в равновесном состоянии является небольшим. Как и для других антител, для авелумаба не характерно специфическое связывание с белками плазмы.
Общий системный клиренс составляет 0.59 л/сут. Согласно результатам анализа общий системный клиренс авелумаба снижается с течением времени: наиболее выраженное среднее максимальное снижение (коэффициент вариации), по сравнению с исходным состоянием среди разных типов опухолей составлял приблизительно 32.1% (КВ 36.2%).
Равновесная концентрация авелумаба достигалась приблизительно через 4-6 недель (2-3 цикла) повторного применения в дозах 10 мг/кг каждые 2 недели, с системным накоплением примерно в 1.25 раза. T1/2 при рекомендуемой дозе составляет 6.1 сут, по данным популяционного фармакокинетического анализа.
Показания активного вещества
АВЕЛУМАБ
Монотерапия у взрослых ранее леченных пациентов с метастатической карциномой Меркеля (МКМ).
Режим дозирования
Терапия должен назначать и контролировать врач, имеющий опыт лечения онкологических заболеваний.
Рекомендуемая доза составляет 10 мг/кг в/в в течение 60 мин каждые 2 недели.
Применение авелумаба следует продолжать в соответствии с рекомендуемой схемой до тех пор, пока наблюдается эффект или не возникнут неприемлемые токсические эффекты. Пациенты с прогрессирующим заболеванием по результатам рентгеновского обследования, не связанным клиническим ухудшением, которое определялось, как отсутствие новых или усиления уже существовавших симптомов, отсутствие ухудшения общего состояния более 2 недель и отсутствие потребности в применении резервной терапии, могут продолжать лечение.
Побочное действие
Со стороны крови и лимфатической системы: очень часто — анемия, часто — лимфопения; нечасто — тромбоцитопения, эозинофилия.
Со стороны иммунной системы: нечасто — лекарственная реакция гиперчувствительности.
Аллергические реакции: нечасто — анафилактическая реакция гиперчувствительности, реакция гиперчувствительности.
Со стороны эндокринной системы: часто — гипотиреоз; нечасто — надпочечниковая недостаточность, гипертиреоз, аутоиммунный гипотиреоз, тиреоидит, аутоиммунный тиреоидит, острая недостаточность коры надпочечников, недостаточность функции гипофиза.
Со стороны обмена веществ: очень часто — снижение аппетита, уменьшение массы тела; нечасто — сахарный диабет, сахарный диабет 1 типа.
Со стороны нервной системы: часто — головная боль, головокружение, периферическая невропатия; нечасто — синдром Гийена-Барре.
Со стороны органа зрения: нечасто — увеит.
Со стороны сердечно-сосудистой системы: редко — миокардит; часто — артериальная гипертензия, артериальная гипотензия; нечасто — гиперемия кожи.
Со стороны дыхательной системы: очень часто — кашель, одышка; часто — пневмонит.
Со стороны пищеварительной системы: очень часто — тошнота, диарея, запор, рвота, боль в животе; часто — снижение аппетита, сухость во рту; нечасто — колит, аутоиммунный колит, энтероколит, кишечная непроходимость.
Со стороны печени и желчевыводящих путей: нечасто — аутоиммунный гепатит, печеночная недостаточность острой степени тяжести, печеночная недостаточность, гепатит.
Со стороны костно-мышечной системы: очень часто — боль в спине, артралгия; часто — миалгия; нечасто — миозит.
Со стороны кожи и или подкожных тканей: часто — сыпь, зуд, пятнисто-папулезная сыпь, сухость кожи; нечасто — зудящая сыпь, эритема, генерализованная сыпь, псориаз, эритематозная сыпь, пятнистая сыпь, папулезная сыпь, эксфолиативный дерматит, многоформная эритема, пемфигоид, генерализованный зуд, экзема, дерматит.
Со стороны мочевыделительной системы: нечасто — тубулоинтерстициальный нефрит.
Общие расстройства: очень часто — утомляемость, повышение температуры тела, периферические отеки; часто — астения, озноб, гриппоподобное заболевание; нечасто — синдром системной воспалительной реакции.
Результаты лабораторных исследований: часто — повышение активности ГГТ, ЩФ, амилазы, липазы, концентрации креатинина в крови; нечасто — повышение активности АСТ, АЛТ, КФК.
Противопоказания к применению
Повышенная чувствительность к авелумабу; детский возраст до 18 лет; нарушение функции почек и печени тяжелой степени тяжести.
Применение при беременности и кормлении грудью
Исследований по влиянию авелумаба на репродуктивную функции у животных не проводилось. Тем не менее, на моделях у беременных мышей было обнаружено, что ингибирование пути PD-L1/PD-1 приводит к снижению толерантности материнского организма к тканям плода, что сопровождается повышением частоты выкидышей. Эти результаты указывают на риск того, что применение авелумаба во время беременности может оказать неблагоприятное воздействие на плод, включая повышение частоты выкидышей и мертворожденных детей. Известно, что иммуноглобулины человека IgG1 проникают через плацентарный барьер. В связи с этим существует возможность проникновения авелумаба из организма матери в развивающийся плод. Авелумаб не рекомендуется применять при беременности, за исключением тех случаев, когда клиническое состояние женщины требует его назначения.
Неизвестно, выделяется ли авелумаб с грудным молоком у человека. Поскольку известно, что антитела могут секретироваться в грудное молоко, нельзя исключить риск для новорожденных и детей грудного возраста. Кормящим женщинам рекомендуется прекратить грудное вскармливание на время лечения авелумабом и минимум на 1 месяц после введения последней дозы в связи с возможностью развития серьезных нежелательных реакций у детей грудного возраста.
Применение при нарушениях функции печени
Противопоказание: нарушение функции печени тяжелой степени тяжести.
Применение при нарушениях функции почек
Противопоказание: нарушение функции почек.
Применение у детей
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет.
Особые указания
У пациентов следует контролировать появление симптомов и признаков инфузионных реакций, в т.ч. повышения температуры тела, озноба, покраснения кожи, снижения АД, одышки, свистящего дыхания, боли в спине, боли в животе и сыпи. При развитии инфузионных реакций 3-й и 4-й степени тяжести следует прекратить инфузию и отменить авелумаб.
Большинство иммуноопосредованных нежелательных реакций на фоне применения авелумаба были обратимыми и прекращались после кратковременного или длительного прерывания терапии авелумабом, применения кортикостероидов и/или поддерживающей терапии.
При подозрении на иммуноопосредованные нежелательные реакции, следует провести полноценное обследование для подтверждения этиологии и исключения других причин. С учетом тяжести нежелательной реакции следует отменить авелумаб и назначить кортикостероиды. Если для лечения нежелательной реакции применяются кортикостероиды, дозу гормонов следует снижать в течение минимум 1 месяца после улучшения. У пациентов, у которых иммуноопосредованные реакции невозможно контролировать с помощью кортикостероидов, необходимо рассмотреть возможность назначения других системных иммунодепрессантов.
У пациентов, получавших авелумаб, наблюдались случаи пневмонита, в т.ч. один с летальным исходом. У пациентов необходимо контролировать появление признаков и симптомов пневмонита и исключить другие причины, кроме пневмонита. При подозрении на пневмонит диагноз следует подтвердить с помощью рентгенографии. В случае развития пневмонита > 2-й степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг/сут преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением). Применение авелумаба следует временно прекратить при развитии пневмонита 2-ой степени тяжести до устранения симптомов. И полностью отменить при развитии пневмонита 3-ей и 4-ой степени тяжести или рецидиве пневмонита 2-ой степени тяжести.
У пациентов, получавших авелумаб, наблюдались случаи гепатита, в т.ч. два с летальным исходом. У пациентов необходимо контролировать появление признаков и симптомов изменения функции печени, появления симптомов гепатита, и исключить другие причины кроме гепатита. В случае развития гепатита > 2-й степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг/сут преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением).
Применение авелумаба следует временно прекратить при развитии гепатита 2 степени тяжести до его разрешения и полностью отменить при развитии гепатита 3 и 4 степени тяжести.
У пациентов, получавших авелумаб, наблюдались случаи колита. У пациентов необходимо контролировать появление признаков и симптомов колита, и исключить другие причины кроме колита. В случае развития колита >2 степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг/сут преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением). Применение авелумаба следует временно прекратить при развитии колита 2 или 3 степени тяжести до разрешения состояния, и полностью отменить при развитии колита 4 степени тяжести или рецидиве колита 3 степени тяжести.
У пациентов необходимо контролировать появление признаков и симптомов эндокринопатий. Авелумаб следует временно отменить при развитии эндокринопатий 3 и 4 степени тяжести до устранения симптомов.
Нарушения функции щитовидной железы могут возникнуть в любое время в ходе лечения. Требуется наблюдение за изменениями функции щитовидной железы до начала терапии и периодически в ходе лечения (на основании данных клинического обследования), а также выявлять симптомы и признаки заболеваний. При гипотиреозе применяют заместительную терапию, при гипертиреозе — антитиреоидные препараты по мере необходимости.
Применение авелумаб следует временно прекратить при развитии нарушений функции щитовидной железы 3 или 4 степени тяжести.
У пациентов необходимо контролировать появление признаков и симптомов надпочечниковой недостаточности в процессе терапии и после ее завершения. При развитии надпочечниковой недостаточности >3 степени тяжести следует назначить кортикостероиды (1-2 мг/кг/сут преднизона внутривенно или эквивалентную дозу внутрь) с последующим постепенным снижением до достижения дозы 10 мг/сут или менее. При развитии надпочечниковой недостаточности 3 или 4 степени тяжести следует временно отменить.
Авелумаб может вызвать развитие сахарного диабета 1 типа, включая диабетический кетоацидоз. У пациентов следует контролировать появление гипергликемии или других симптомов сахарного диабета. При развитии сахарного диабета 1 типа следует назначить инсулин. У пациентов с гипергликемией > 3-ей степени тяжести следует временно прервать терапию авелумабом и назначить гипогликемические препараты. После достижения контроля гликемии на фоне применения заместительной терапии инсулином лечение авелумабом следует возобновить.
Авелумаб может вызвать развитие нефрита. У пациентов следует контролировать повышение уровня креатинина в сыворотке крови до начала терапии и периодически в ходе лечения. При нефрите >2 степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг/сут преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением). При развитии нефрита 2 или 3 степени тяжести терапию авелумабом следует временно прекратить до разрешения нефрита до >1 степени, а при развитии нефрита 4 степени тяжести, авелумаб следует отменить.
Другие клинически значимые нежелательные реакции были зарегистрированы менее чем у 1% пациентов: миокардит, в том числе миокардит с летальным исходом, миозит, недостаточность функции гипофиза, увеит и синдром Гийена-Барре. При подозрении на другие нежелательные реакции следует провести полноценное обследование для подтверждения этиологии и исключения других причин. С учетом тяжести других нежелательной реакции авелумаб следует отменить и назначить кортикостероиды. При уменьшении выраженности других нежелательных реакций до 1 степени тяжести или менее после снижения дозы кортикостероидов следует возобновить терапию авелумабом. При развитии рецидивов других нежелательных реакций 3 степени тяжести или развитии реакций 4 степени тяжести авелумаб следует полностью отменить.
Авелумаб оказывает незначительное влияние на способность управлять транспортными средствами и механизмами. На фоне применения была зарегистрирована утомляемость. Пациентам рекомендуется соблюдать осторожность при вождении автотранспорта или работе с механизмами, пока они не убедятся, что авелумаб не вызывает нежелательной реакции.
Лекарственное взаимодействие
Отдельных исследований взаимодействия авелумаба с другими лекарственными средствами не проводилось. Поскольку авелумаб выводится посредством катаболизма, фармакокинетическое взаимодействия с другими лекарственными препаратами не ожидается.
Бавенсио — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005886
Торговое наименование
Бавенсио®
Международное непатентованное наименование
Авелумаб
Лекарственная форма
концентрат для приготовления раствора для инфузий
Состав
1 флакон содержит
действующее вещество: авелумаб 200,0 мг;
вспомогательные вещества: D-маннитол 510,0 мг, ледяная уксусная кислота 6,0 мг, полисорбат 20 5,0 мг, натрия гидроксид 3,0 мг, вода для инъекции до 10 мл
Описание
От бесцветного до желтоватого цвета прозрачная жидкость.
Фармакотерапевтическая группа
Противоопухолевое средство – антитела моноклональные
Код ATX:
[L01XC31]
Фармакологические свойства
Фармакодинамика
Авелумаб – человеческий иммуноглобулин G1 (IgGl), моноклональное антитело, направленное против лиганда программируемой клеточной смерти 1 (PD L1). Авелумаб непосредственно связывается с PD-L1 и блокирует его взаимодействие с рецепторами PD-1 и В7.1. Таким образом, авелумаб устраняет подавляющие эффекты PD-L1 в отношении цитотоксических Т лимфоцитов CD8+, что приводит к восстановлению противоопухолевого Т-клеточного ответа. Авелумаб индуцирует опосредуемый натуральными клетками киллерами (NK) прямой лизис клетки опухоли с помощью активации антителозависимой клеточно-опосредованной цитотоксичности (АЗКЦ).
Фармакокинетика
Распределение
Авелумаб распределяется в общем кровотоке и в меньшей степени – во внеклеточном пространстве. Объем распределения в равновесном состоянии составлял 4,72 л. В связи с ограниченным внесосудистым распределением объем распределения авелумаба в равновесном состоянии является небольшим. Как и для других антител, для авелумаба не характерно специфическое связывание с белками плазмы.
Выведение
Общий системный клиренс составляет 0,59 л/день. Согласно результатам анализа общий системный клиренс авелумаба снижается с течением времени: наиболее выраженное среднее максимальное снижение коэффициент вариации, по сравнению с исходным состоянием среди разных типов опухолей составлял приблизительно 32,1% (КВ 36,2%).
Равновесная концентрация авелумаба достигалась приблизительно через 4-6 недель (2-3 цикла) повторного применения в дозах 10 мг/кг каждые 2 недели, с системным накоплением примерно в 1,25 раза. Период полувыведения (Т1/2) при рекомендуемой дозе составляет 6,1 дня, по данным популяционного фармакокинетического (ФК) анализа
Особые группы пациентов
Результаты популяционного фармакокинетического анализа свидетельствуют об отсутствии разницы в общем системном клиренсе авелумаба в зависимости от возраста, пола, расовой принадлежности, статуса PD-L1, опухолевой нагрузки, нарушения функции почек и наличия печеночной недостаточности легкой или средней степени тяжести.
Общий системный клиренс повышался по мере увеличения массы тела. Экспозиция в равновесном состоянии была практически одинаковой в широком диапазоне показателей массы тела (30-204 кг) при нормализации дозы в соответствии с массой тела.
Пациенты с нарушением функции почек
В ходе исследований не было выявлено клинически значимых различий в клиренсе авелумаба между пациентами с легкой (скорость клубочковой фильтрации (СКФ) 60-89 мл/мин, клиренс креатинина по формуле Кокрофга-Голта (КлКр); n=673), умеренной (СКФ 30-59 мл/мин, n=320) почечной недостаточностью и пациентами с нормальной (СКФ ≥90 мл/мин, n=671) функцией почек. У пациентов с тяжелой почечной недостаточностью (СКФ 15-29 мл/мин) применение авелумаба не изучалось.
Пациенты с нарушением функции печени
В популяционном ФК анализе не было выявлено клинически значимых различий в клиренсе авелумаба между пациентами с печеночной недостаточностью легкой (билирубин ≥ВГН или ACT >ВГН, или билирубин в 1-1,5 раз выше ВГН, n=217) степени и пациентами с нормальной функцией печени (билирубин и АСТ≥ ВГН, n=1388). Печеночная недостаточность устанавливалась в соответствии с критериями нарушения функции печени Национального Института Рака (NСI). У пациентов с печеночной недостаточностью средней (уровень билирубина в 1,5-3 раза выше ВГН) и тяжелой степенью (уровень билирубина в >3 раза выше BГН) применение авелумаба не изучалось.
Показания к применению
Монотерапия у взрослых ранее леченных пациентов с метастатической карциномой Меркеля (МКМ).
Противопоказания
- Гиперчувствительность к препарату БАВЕНСИО® или любому компоненту препарата в анамнезе;
- Детский возраст до 18 лет;
- Нарушение функции почек и печени тяжелой степени тяжести.
Применение во время беременности и в период грудного вскармливания
Беременность
Данные относительно применения препарата БАВЕНСИО® у беременных женщин ограничены или отсутствуют.
Исследований по влиянию авелумаба на репродуктивную функции у животных не проводилось. Тем не менее, в моделях у беременных мышей было обнаружено, что ингибирование пути PD-L1/PD-1 приводит к снижению толерантности материнского организма к тканям плода, что сопровождается повышением частоты выкидышей. Эти результаты указывают на риск того, что применение авелумаба во время беременности может оказать неблагоприятное воздействие на плод, включая повышение частоты выкидышей и мертворожденных детей. Известно, что иммоноглобулины человека IgG1 проникают через плацентарный барьер. В связи с этим существует возможность проникновения авелумаба из организма матери в развивающийся плод. Авелумаб не рекомендуется применять во время беременности, за исключением тех случаев, когда клиническое состояние женщины требует его назначения.
Период грудного вскармливания
Данные относительно секреции препарата БАВЕНСИО® в грудное молоко отсутствуют. Поскольку известно, что антитела могут секретироваться в грудное молоко, нельзя исключить риск для новорожденных и детей грудного возраста. Кормящим женщинам рекомендуется прекратить грудное вскармливание на время лечения авелумабом и минимум на 1 месяц после введения последней дозы в связи с возможностью развития серьезных нежелательных реакций у детей грудного возраста.
Способ применения и дозы
Терапия должна назначаться и контролироваться врачом, имеющим опыт лечения онкологических заболеваний.
Рекомендуемая доза препарата БАВЕНСИО® составляет 10 мг/кг массы тела внутривенно в течение 60 минут каждые 2 недели.
Применение препарата БАВЕНСИО® следует продолжать в соответствии с рекомендуемой схемой до тех пор, пока наблюдается эффект или не возникнут неприемлемые токсические эффекты. Пациенты с прогрессирующим заболеванием по результатам рентгеновского обследования, не связанным клиническим ухудшением, которое определялось, как отсутствие новых или усиления уже существовавших симптомов, отсутствие ухудшения общего состояния более 2 недель и отсутствие потребности в применении резервной терапии, могут продолжать лечение.
Премедикация
Перед первыми 4 инфузиями препарата БАВЕНСИО® пациенту следует провести премедикацию антигистаминными средствами и парацетамолом. Если четвертая инфузия завершается без развития инфузионных реакций, премедикация перед введением последующих доз назначается по усмотрению врача.
Коррекция дозы
Повышение или снижение дозы препарата БАВЕНСИО® не рекомендуется. С учетом индивидуальной безопасности и переносимости возможна задержка введения очередной дозы препарата или прерывание лечения.
Рекомендации по приостановки терапии или полной отмене препарата БАВЕНСИО®
Таблица 1.
Рекомендации по коррекции режима дозирования при отдельных нежелательных реакциях
| Нежелательная реакция | Степень тяжести | Коррекция терапии |
| Инфузионные реакции | 1-я степень | Снизить скорость инфузии на 50% |
| 2-я степень | Приостановить инфузию до снижения тяжести явления 0-ой или 1-ой степени; возобновить инфузию со снижением скорости на 50% | |
| 3-я или 4-я степень | Прекратить терапию | |
| Пневмонит | 2-я степень | Приостановить терапию до снижения тяжести явления 0-ой или 1-ой степени |
| 3-я или 4-я степень, или рецидив пневмонита 2-ой степени | Прекратить терапию | |
| Гепатит | Уровень аспартатаминотрансферазы (ACT) или аланинаминотрансферазы (АЛТ) в 3-5 раз превышает верхнюю границу нормы (ВГН) или билирубин в крови в 1,5-3 раза превышает ВГН | Приостановить терапию до снижения тяжести явления 0-ой или 1-ой степени |
| Уровень ACT или АЛТ в >5 раз превышает ВГН или билирубин в крови в >3 раза превышает ВГН | Прекратить терапию | |
| Колит | Колит или диарея 2-ой, или 3-ей степени | Приостановить терапию до снижения тяжести явления 0-ой или 1-ой степени |
| Колит или диарея 4 ой степени или рецидив колита 3-ей степени | Прекратить терапию | |
| Эндокринопатии (гипотиреоз, гипертиреоз, надпочечниковая недостаточность, гипергликемия) | Эндокринопатии 3-ей или 4-ой степени | Приостановить терапию до снижения тяжести явления 0-ой или 1-ой степени |
| Нефрит и нарушение функции почек | Уровень креатинина в сыворотке крови, в 1,5-6 раз превышающий ВГН | Приостановить терапию до снижения тяжести явления 0-ой или 1-ой степени |
| Уровень креатинина в сыворотке крови, в более чем 6 раз превышающий ВГН | Прекратить терапию | |
| Другие иммуноопосредованные нежелательные реакции (включая миокардит, миозит, недостаточность функции гипофиза, увеит, синдром Гийена-Барре) | Для любого состояния из следующих: Клинические признаки неописанных выше иммуноопосредованных нежелательных реакций 2-ой или 3-ей степени |
Приостановить терапию до снижения тяжести явления 0-ой или 1-ой степени |
| Для любого состояния из следующих: — нежелательные реакции 4-ой степени или угрожающие жизни реакции (за исключением эндокринопатий, которые контролируются с помощью заместительной гормональной терапии); — рецидивирующие иммуноопосредованные нежелательные реакции 3-ей степени; — потребность в дозе преднизона 10 мг или выше, или эквивалентной дозе другого аналогичного препарата в течение более 12 недель; — персистирующие иммуноопосредованные реакции 2-ой или 3-ей степени, сохраняющиеся в течение 12 недель или более. |
Прекратить терапию |
Критерии токсичности указаны в соответствии с общими критериями терминологии Национального института рака для нежелательных явлений, в. 4.0.
Особые группы пациентов
Пожилой возраст
Коррекция дозы препарата БАВЕНСИО® у пациентов пожилого возраста ≥65 лет не требуется.
Дети
Эффективность и безопасность применения препарата БАВЕНСИО® у детей и подростков <18 лет не изучалась.
Нарушение функции почек
Коррекция дозы у пациентов с нарушением функции почек легкой и средней степени тяжести не требуется. Данных о применении препарата БАВЕНСИО® с нарушением функции почек тяжелой степени тяжести недостаточно для рекомендации по применению.
Нарушение функции печени
Коррекция дозы у пациентов с нарушением функции печени легкой степени тяжести не требуется. Данных о применении препарата БАВЕНСИО® с нарушением функции печени средней и тяжелой степеней тяжести недостаточно для рекомендации по применению.
Правила приготовления и храпения раствора для инфузии
Препарат БАВЕНСИО® применяется только для внутривенного введения. Его не следует вводить внутривенно струйно (болюсно).
Препарат БАВЕНСИО® разводится 0,9% или 0,45% раствором натрия хлорида. Препарат вводится в течение более 60 минут в виде внутривенной инфузии с использованием стерильного непирогенного встроенного или дополнительного фильтра с низким связыванием белков с размером пор 0,2 мкм.
Препарат БАВЕНСИО® совместим с инфузионными пакетами из полипропилена и этиленвинилацетата, стеклянными флаконами, инфузионными системами из поливинилхлорида и внутривенными катетерами с полиэфирсульфоновыми мембранами с размером пор 0,2 мкм.
Готовый раствор может храниться не более 24 часов при температуре 2-8 °С или не более 8 часов при комнатной температуре 20-25 °С. Если раствор хранился при температуре 2-8 °С, перед введением препарата необходимо довести до комнатной температуры.
Раствор для инфузий следует готовить в асептических условиях.
- Раствор для парентерального введения перед использованием следует визуально проверить на наличие частиц и изменение цвета. Если раствор мутный, или в случае обнаружения частиц, или изменения цвета, раствор использовать нельзя.
- Отобрать необходимый объем препарата БАВЕНСИО® из флакона и развести в 0,9% или 0,45% растворе натрия хлорида для инъекций в инфузионном пакете объемом 250 мл.
- Разведенный раствор необходимо перемешать, осторожно переворачивая пакет, чтобы избежать образования пены или избыточной фрагментации раствора.
- Раствор следует осмотреть, чтобы убедиться, что он является прозрачным, бесцветным и не содержит видимых частиц. Разведенный раствор следует использовать сразу после приготовления.
- Не вводите другие препараты через тот же внутривенный катетер.
После инфузии препарата БАВЕНСИО® необходимо промыть катетер с помощью 0,9% или 0,45% раствора натрия хлорида для инъекций.
Разбавленный раствор не подлежит замораживанию или встряхиванию.
Побочное действие
Применение препарата БАВЕНСИО® чаще всего сопровождается развитием иммуноопосредованных нежелательных реакций. Большинство из них, в том числе выраженной степени тяжести, разрешались после назначения соответствующей медикаментозной терапии или отмены препарата БАВЕНСИО®.
Безопасность препарата БАВЕНСИО® оценивалась в клинических исследованиях у пациентов с солидными опухолями, в том числе, МКМ, которые получали препарат в дозе 10 мг/кг каждые 2 недели. В этой популяции пациентов наиболее частыми нежелательными реакциями на фоне применения препарата БАВЕНСИО® были утомляемость, тошнота, диарея, снижение аппетита, запор, инфузионные реакции, снижение массы тела и рвота. Наиболее частыми нежелательными реакциями ≥3 степени тяжести были анемия, одышка и боль в животе. Серьезными нежелательными реакциями были иммуноопосредованные реакции и инфузионные реакции.
В таблице 2 представлены объединенные данные о нежелательных реакциях (НР).
Для описания частоты нежелательных реакций используется следующая классификация:
очень часто (≥1/10); часто (≥1/100 <1/10); нечасто (≥1/1000 <1/100); редко (≥1/10000 <1/1000); очень редко (<1/10000).
Таблица 2.
НP у пациентов, получавших терапию препаратом БАВЕНСИО® в ходе клинических исследовании.
| Частота | Нежелательные реакции |
| Нарушения со стороны крови и лимфатической системы | |
| Очень часто | Анемия |
| Часто | Лимфопения |
| Нечасто | Тромбоцитопения, эозинофилия§ |
| Нарушения со стороны иммунной системы | |
| Нечасто | Лекарственная реакция гиперчувствительности, анафилактическая реакция гиперчувствительности, реакция гиперчувствительности |
| Нарушения со стороны эндокринной системы | |
| Часто | Гипотиреоз* |
| Нечасто | Надпочечниковая недостаточность*, гипертиреоз*, аутоиммунный гипотиреоз*, тиреоидит*, аутоиммунный тиреоидит, острая недостаточность коры надпочечников*, недостаточность функции гипофиза* |
| Нарушения со стороны обмена веществ и питания | |
| Очень часто | Снижение аппетита |
| Нечасто | Сахарный диабет*, сахарный диабет 1 типа* |
| Нарушения со стороны нервной системы | |
| Часто | Головная боль, головокружение, периферическая нейропатия |
| Нечасто | Синдром Гийена-Барре* |
| Нарушения со стороны органа зрения | |
| Нечасто | Увеит* |
| Нарушения со стороны сердечно-сосудистой системы | |
| Редко | Миокардит* |
| Часто | Гипертензия, гипотензия |
| Нечасто | Гиперемия кожи |
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | |
| Очень часто | Кашель, одышка |
| Часто | Пневмонит* |
| Нарушения со стороны желудочно-кишечного тракта | |
| Очень часто | Тошнота, диарея, запор, рвота, боль в животе |
| Часто | Сухость во рту |
| Нечасто | Колит*, аутоиммунный колит*, энтероколит*, кишечная непроходимость |
| Нарушения со стороны печени и желчевыводящих путей | |
| Нечасто | Аутоиммунный гепатит*, печеночная недостаточность острой степени тяжести*, печеночная недостаточность*, гепатит* |
| Реакции со стороны кожи или подкожных тканей | |
| Часто | Сыпь*, зуд*, пятнисто-папулезная сыпь*, сухость кожи |
| Нечасто | Зудящая сыпь*, эритема*, генерализованная сыпь*, псориаз*, эритематозная сыпь*, пятнистая сыпь*, папулезная сыпь*, эксфолиативный дерматит*, полиморфная эритема*, пемфигоид*, генерализованный зуд*, экзема, дерматит |
| Нарушения со стороны костно-мышечной и соединительной ткани | |
| Очень часто | Боль в спине,артралгия |
| Часто | Миалгия |
| Нечасто | Миозит* |
| Нарушения со стороны почек и мочевыводящих путей | |
| Нечасто | Тубулоинтерстициальный нефрит* |
| Общие расстройства и нарушения в месте введения | |
| Очень часто | Утомляемость, повышение температуры тела, периферические отеки |
| Часто | Астения, озноб, гриппоgнодобное заболевание |
| Нечасто | Синдром системной воспалительной реакции* |
| Влияние на результаты лабораторных и инструментальных исследований | |
| Очень часто | Снижение массы тела |
| Часто | Повышение уровней гамма-глутамилтрансферазы, щелочной фосфатазы, амилазы, липазы, креатинина крови |
| Нечасто | Повышение уровней аспартатаминотрансферазы (ACT)*, аланинаминотрансферазы (АЛТ)*, креатинфосфокиназы*, трансаминаз* |
| Травмы, интоксикации и осложнения манипуляции | |
| Очень часто | Инфузионные реакции |
* – Иммуноопосредованные нежелательные реакции на основании медицинского анализа
§ – Частота нежелательных реакций была установлена в клиническом исследовании EMR 100070-003 (часть В) после завершения сбора данных для объединенного анализа.
Описание отдельных нежелательных реакций
Данные относительно описанных ниже иммуноопосредованных нежелательных реакций основаны на результатах клинических исследований, полученных у пациентов с другими солидными опухолями, принимавших авелумаб.
Иммуноопосредованный пневмонит
В клинических исследованиях иммуноопосредованный пневмонит развился у 1,2% пациентов. Из этих пациентов у одного (0,1%) зарегистрирован летальный исход. У одного пациента (0,1%) развился пневмонит 4-ой степени, и у 5 пациентов (0,3%) развился иммуноопосредованный пневмонит 3-ей степени.
Медиана времени до начала проявления признаков пневмонита составляла 2,5 месяца (диапазон: 3 дня-11 месяцев). Медиана длительности течения пневмонита составила 7 недель (диапазон: от 4 дней до более 4 месяцев).
У 0,3% пациентов пневмонит стал причиной отмены препарата БАВЕНСИО®. Все 21 пациента с иммуноопосредованным пневмонитом получали лечение кортикостероидами, 17 (81%) из них получали высокие дозы кортикостероидов в течение периода времени, медиана которого составляла 8 дней (диапазон: 1 день-2,3 месяца). Иммуноопосредованный пневмонит разрешился у 12 (57%) из 21 пациентов на момент прекращения сбора данных.
Иммуноопосредованный гепатит
В клинических исследованиях иммуноопосредованный гепатит развился у 0,9% пациентов. Из них у 2 (0,1%) пациентов был зарегистрирован летальный исход. У 11 (0,6%) развился иммуноопосредованный гепатит 3 степени.
Медиана времени до начала проявления признаков гепатита составляла 3,2 месяца (диапазон: 1 неделя – 15 месяцев). Медиана длительности течения гепатита составила 2,5 месяцев (диапазон: от 1 дня до более 7,4 месяца). У 0,5% пациентов гепатит стал причиной отмены препарата БАВЕНСИО®. Все 16 пациентов с иммуноопосредованным гепатитом получали лечение кортикостероидами, 15 (94%) из них получали высокие дозы кортикостероидов в течение периода времени, медиана которого составляла 14 дней (диапазон: 1 день – 2,5 месяца). Иммуноопосредованный гепатит разрешился у 9 (56%) из 16 пациентов на момент прекращения сбора данных.
Иммуноопосредованный колит
В клинических исследованиях иммуноопосредованный колит развился у 1,5% пациентов. Из них у 7 (0,4%) развился иммуноопосредованный колит 3 степени. Медиана времени до начала проявления признаков колита составляла 2,1 месяца (диапазон: 2 дня-11 месяцев). Медиана длительности течения колита составила 6 недель (диапазон: от 1 дня до более 14 месяцев). У 0,5% пациентов колит стал причиной отмены препарата БАВЕНСИО® Все 26 пациентов с иммуноопосредованным колитом получали лечение кортикостероидами, 15 (58%) из них получали высокие дозы кортикостероидов в течение периода времени, медиана которого составляла 19 дней (диапазон: 1 день – 2,3 месяца). Иммуноопосредованный колит разрешился у 18 (70%) из 26 пациентов на момент прекращения сбора данных.
Иммуноопосредованные эндокринопатии
Заболевания щитовидной железы
В клинических исследованиях иммуноопосредованные нарушения функции щитовидной железы развились у 6% пациентов. Из них у 90 (5%) пациентов развился гипотиреоз, у 7 (0,4%) – гипертиреоз, у 4 (0,2%) – тиреоидит. Из этих пациентов у 3 (0,2%) были зарегистрированы иммуноопосредованные нарушения функции щитовидной железы 3 степени. Медиана времени до начала проявления признаков нарушений функции щитовидной железы составляла 2,8 месяца (диапазон: 2 недели-13 месяцев). Медиана длительности была неопределяемой (диапазон: от 1 дня до более 26 месяцев). У 0,1% пациентов нарушение функции щитовидной железы стало причиной отмены препарата БАВЕНСИО® Нарушения функции щитовидной железы разрешились у 7 (7%) из 98 пациентов на момент прекращения сбора данных.
Надпочечниковая недостаточность
В клинических исследованиях иммуноопосредованная недостаточность надпочечников развилась у 0,5% пациентов. Из них у 1 (0,1%) пациента была зарегистрирована недостаточность надпочечников 3 степени. Медиана времени до начала проявления признаков нарушений недостаточности надпочечников составляла 2,5 месяца (диапазон: 1 день-8 месяцев). Медиана длительности течения была неопределяемой (диапазон: от 2 дней до более 6 месяцев). У 0,1% пациентов, недостаточность надпочечников стала причиной отмены препарата БАВЕНСИО®. Все 8 пациентов с иммуноопосредованной недостаточностью надпочечников получали кортикостероиды. 4 из 8 пациентов (50%) получали высокие дозы системных кортикостероидов (≥ 40 мг преднизона или эквивалентную дозу другого препарата) с последующим снижением в течение медианы времени I день (диапазон: 1 день-24 дня).
У 1 пациента недостаточность надпочечников разрешилась на фоне терапии кортикостероидами на момент завершения сбора данных.
Сахарный диабет 1 типа
Сахарный диабет 1 типа без альтернативной этиологии развился у 0,1% пациентов, включая 2 реакции 3 степени, которые стали причиной отмены препарата БАВЕНСИО®.
Иммуноопосредованный нефрит и нарушение функции почек
У 0,1% пациентов иммуноопосредованный нефрит, стал причиной отмены препарата БАВЕНСИО®.
Иммуногенность
Из 1738 пациентов, получавших препарат БАВЕНСИО® в дозе 10 мг/кг в виде внутривенных инфузий каждые 2 недели, 1627 было обследованы на наличие антител к лекарственному препарату. У 96 (5,9%) из них были получены положительные результаты. У положительных пациентов возможно повышение риска развития инфузионных реакций (около 40% и 25% у пациентов, у которых хоть раз были выявлены или никогда не выявлялись наличие антител к лекарственному препарату соответственно). На основании имеющихся данных, включая низкую частоту иммуногенности, влияние антител к лекарственному препарату на фармакокинетику, эффективность и безопасность не определено, при этом воздействие нейтрализующих антител неизвестно.
Передозировка
У троих пациентов было зарегистрировано увеличение дозы препарата БАВЕНСИО® на 5% и 10%. У пациентов отсутствовали симптомы, не требовалось лечения передозировки, и они продолжили терапию препаратом БАВЕНСИО®.
В случае передозировки следует тщательно наблюдать за пациентами для выявления симптомов развития нежелательных реакций. Лечение направлено на устранение симптомов.
Взаимодействие с другими лекарственными средствами
Отдельных исследований взаимодействия авелумаба с другими лекарственными средствами не проводилось. Поскольку авелумаб выводится посредством катаболизма, фармакокинетическое взаимодействие с другими лекарственными препаратами не ожидается.
Особые указания
Инфузионные реакции
У пациентов, получающих препарат БАВЕНСИО®, были зарегистрированы инфузионные реакции, часть из которых были тяжелыми. У пациентов следует контролировать появление симптомов и признаков инфузионных реакций, в том числе повышения температуры тела, озноба, покраснения кожи, снижения артериального давления, одышки, свистящего дыхания, боли в спине, боли в животе и сыпи. При развитии инфузионных реакций 3-ей и 4-ой степени тяжести следует прекратить инфузию и отменить препарат БАВЕНСИО®.
При развитии инфузионных реакций 1-ой степени тяжести необходимо уменьшить скорость инфузии на 50%. У пациентов с инфузионными реакциями 2-ой степени тяжести, инфузию препарата следует временно приостановить до снижения выраженности реакции до 1-ой степени тяжести или ее разрешения. После этого инфузию следует возобновить, но скорость ее уменьшить на 50%.
В случае рецидива инфузионных реакций 1-ой или 2-ой степени тяжести, пациент может продолжать получать препарат БАВЕНСИО® под тщательным наблюдением после коррекции скорости инфузии и проведения премедикации, с помощью антигистаминных препаратов и парацетамола.
В клинических исследованиях у 98,6% пациентов с инфузионными реакциями, первая реакция развилась в течение первых 4 инфузий, из них 2,7% реакций были ≥3-ей степени тяжести. У остальных 1,4% пациентов инфузионные реакции возникали после первых 4 инфузий и были 1-ой или 2-ой степени тяжести.
Иммуноопосредованные реакции
Большинство иммуноопосредованных нежелательных реакций на фоне приема препарата БАВЕНСИО® были обратимыми и прекращались после кратковременного или длительного прерывания терапии препаратом БАВЕНСИО®, применения кортикостероидов и/или поддерживающей терапии.
При подозрении на иммуноопосредованные нежелательные реакции, следует провести полноценное обследование для подтверждения этиологии и исключения других причин. С учетом тяжести нежелательной реакции следует отменить препарат БАВЕНСИО® и назначить кортикостероиды. Если для лечения нежелательной реакции применяются кортикостероиды, дозу гормонов следует снижать в течение минимум 1 месяца после улучшения. У пациентов, у которых иммуноопосредованные реакции невозможно контролировать с помощью кортикостероидов, необходимо рассмотреть возможность назначения других системных иммунодепрессантов.
Иммуноопосредованный пневмонит
У пациентов, получавших препаратом БАВЕНСИО®, наблюдались случаи пневмонита, в том числе один с летальным исходом. У пациентов необходимо контролировать появление признаков и симптомов пневмонита и исключить другие причины, кроме пневмонита. При подозрении на пневмонит диагноз следует подтвердить с помощью рентгенографии. В случае развития пневмонита ≥2-ой степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг в сутки преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением). Применение препарата БАВЕНСИО® следует временно прекратить при развитии пневмонита 2-ой степени тяжести до устранения симптомов. И полностью отменить при развитии пневмонита 3-ей и 4-ой степени тяжести или рецидиве пневмонита 2-ой степени тяжести.
Иммуноопосредованный гепатит
У пациентов, получавших препарат БАВЕНСИО®, наблюдались случаи гепатита, в том числе два с летальным исходом. У пациентов необходимо контролировать появление признаков и симптомов изменения функции печени, появления симптомов гепатита, и исключить другие причины кроме гепатита. В случае развития гепатита ≥2-ой степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг в сутки преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением).
Применение препарата БАВЕНСИО® следует временно прекратить при развитии гепатита 2-ой степени тяжести до его разрешения и полностью отменить при развитии гепатита 3-ей и 4-ой степени тяжести.
Иммуноопосредованный колит
У пациентов, получавших препарат БАВЕНСИО®, наблюдались случаи колита, У пациентов необходимо контролировать появление признаков и симптомов колита, и исключить другие причины кроме колита. В случае развития колита ≥2-ой степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг в сутки преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением). Применение препарата БАВЕНСИО® следует временно прекратить при развитии колита 2-ой или 3-ей степени тяжести до разрешения состояния, и полностью отменить при развитии колита 4-ой степени тяжести или рецидиве колита 3-ей степени тяжести.
Иммуноопосредованные эндокринопатии
У пациентов, получавших препарат БАВЕНСИО®, наблюдались случаи нарушений функции щитовидной железы недостаточности надпочечников и сахарного диабета 1 типа.
У пациентов необходимо контролировать появление признаков и симптомов эндокринопатий. Препарат БАВЕНСИО® следует временно отменить при развитии эндокринопатий 3-ей и 4-ой степени тяжести до устранения симптомов.
Нарушения функции щитовидной железы (гипотиреоз, гипертиреоз)
Нарушения функции щитовидной железы могут возникнуть в любое время в ходе лечения. Требуется наблюдение за изменениями функции щитовидной железы до начала терапии и периодически в ходе лечения (на основании данных клинического обследования), а также выявлять симптомы и признаки заболеваний. При гипотиреозе применяют заместительную терапию, при гипертиреозе – антитиреоидные препараты по мере необходимости.
Применение препарата БАВЕНСИО® следует временно прекратить при развитии нарушений функции щитовидной железы 3-ей или 4-ой степени тяжести.
Надпочечниковая недостаточность
У пациентов необходимо контролировать появление признаков и симптомов надпочечниковой недостаточности в процессе терапии и после её завершения. При развитии надпочечниковой недостаточности ≥3 степени тяжести следует назначить кортикостероиды (1-2 мг/кг в сутки преднизона внутривенно или эквивалентную дозу внутрь) с последующим постепенным снижением до достижения дозы 10 мг в сутки или менее. При развитии надпочечниковой недостаточности 3-ей или 4-ой степени тяжести препарат БАВЕНСИО® следует временно отменить.
Сахарный диабет 1 типа
Препарат БАВЕНСИО® может вызвать развитие сахарного диабета 1 типа, включая диабетический кетоацидоз. У пациентов следует контролировать появление гипергликемии или других симптомов сахарного диабета. При развитии сахарного диабета 1 типа следует назначить инсулин. У пациентов с гипергликемией ≥3-ей степени тяжести следует временно прервать терапию препаратом БАВЕНСИО® и назначить гипогликемические препараты. После достижения контроля гликемии на фоне применения заместительной терапии инсулином лечение препаратом БАВЕНСИО® следует возобновить.
Иммуноопосредованный нефрит и нарушение функции почек
Препарат БАВЕНСИО® может вызвать развитие нефрита. У пациентов следует контролировать повышение уровня креатинина в сыворотке крови до начала терапии и периодически в ходе лечения. При нефрите ≥2-ой степени тяжести следует назначить кортикостероиды (начальная доза 1-2 мг/кг в сутки преднизона или другого препарата в эквивалентной дозе с последующим постепенным снижением). При развитии нефрита 2-ой или 3-ей степени тяжести терапию препаратом БАВЕНСИО® следует временно прекратить до разрешения нефрита до ≥1-ой степени, а при развитии нефрита 4-ой степени тяжести, препарат БАВЕНСИО® следует отменить.
Другие иммуноопосредованные нежелательные реакции
Другие клинически значимые нежелательные реакции были зарегистрированы менее чем у 1% пациентов: миокардит, в том числе миокардит с летальным исходом, миозит, недостаточность функции гипофиза, увеит и синдром Гийена-Барре. При подозрении на другие нежелательные реакции следует провести полноценное обследование для подтверждения этиологии и исключения других причин. С учетом тяжести других нежелательной реакции препарат БАВЕНСИО® следует отменить и назначить кортикостероиды. При уменьшении выраженности других нежелательных реакций до 1-ой степени тяжести или менее после снижения дозы кортикостероидов следует возобновить терапию препаратом БАВЕНСИО®. При развитии рецидивов других нежелательных реакций 3-ей степени тяжести или развитии реакций 4-ой степени тяжести препарат БАВЕНСИО® следует полностью отменить.
Пациенты, исключенные из клинических исследований
Пациенты, имеющие метастазы в центральную нервную систему (ЦНС) (активные или в анамнезе), аутоиммунные заболевания (активные или в анамнезе), другие злокачественные образования в течение предшествовавших 5 лет, трансплантацию органов, состояния, требующие терапевтической иммуносупрессии, или активные инфекции ВИЧ, гепатит В или С, исключались из исследования.
Содержание натрия
Лекарственный препарат содержит менее 1 ммоль натрия (23 мг) на дозу.
Влияние на способность управлять транспортными средствами и механизмами
Препарат БАВЕНСИО® оказывает незначительное влияние на способность управлять транспортными средствами и механизмами. На фоне применения препарата БАВЕНСИО® была зарегистрирована утомляемость. Пациентам рекомендуется соблюдать осторожность при вождении автотранспорта или работе с механизмами, пока они не убедятся, что препарат БАВЕНСИО® не вызывает нежелательной реакции.
Форма выпуска
Концентрат для приготовления раствора для инфузий 20 мг/мл.
По 10 мл препарата во флакон бесцветного стекла (гидролитический класс 1), укупоренный резиновой пробкой, под алюминиевой обкаткой с пластиковым колпачком.
1 флакон с препаратом вместе с инструкцией по применению помещают в картонную пачку с контролем первого вскрытия.
Срок годности
2 года.
Не использовать по истечении срока годности, указанного на упаковке.
Условия хранения
Хранить при температуре от 2 до 8 °С в оригинальной упаковке.
Не замораживать.
Хранить в недоступном для детей месте.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ООО «Мерк»,
115054, г, Москва, ул, Валовая, д, 35
Производитель
Мерк Сероно С.А., Филиал Обонн,
Индустриальная зона Урьеттаз,
1170 Обонн, Швейцария
Претензии потребителей и информацию о нежелательных явлениях следует направлять по адресу:
ООО «Мерк»,
115054, г. Москва, ул. Валовая, д. 35
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Авелумаб
Avelumab
Фармакологическое действие
Авелумаб — представляет собой антитело к белку PD-L1.
Механизм действия
PD-L1 может быть экспрессирован на опухолевых клетках и опухолепроникающих иммунных клетках и может способствовать ингибированию противоопухолевого иммунного ответа в микроокружении опухоли. Связывание PD-L1 с рецепторами PD-1 и B7.1, обнаруженное на Т-клетках и антигенпредставляющих клетках, подавляет активность цитотоксических Т-клеток, пролиферацию Т-клеток и продуцирование цитокинов. Авелумаб связывает PD-L1 и блокирует взаимодействие между PD-L1 и его рецепторами PD-1 и B7.1. Это взаимодействие блокирует ингибирующие эффекты PD-L1 на иммунный ответ, приводящее к восстановлению иммунных реакций, включая противоопухолевые иммунные ответы. Было также показано, что авелумаб индуцирует антителозависимую клеточно-опосредованную цитотоксичность in vitro. В сингенных опухолевых моделях мыши блокирование активности PD-L1 приводило к уменьшению роста опухоли.
Фармакокинетика
Фармакокинетика авелумаба изучалась у 1629 пациентов, получавших дозы от 1 до 20 мг/кг каждые 2 недели. Данные показали, что экспозиция авелумаба увеличивалась пропорционально дозе в диапазоне доз 10–20 мг/кг каждые 2 недели. Стабильные концентрации авелумаба достигались через приблизительно 4–6 недель (2–3 цикла) дозирования, а системное накопление было приблизительно в 1,25 раза.
Распределение
Геометрический средний объём распределения в стационарном состоянии после введения дозы 10 мг/кг, составлял 4,72 л.
Выведение
Основным механизмом элиминации авелумаба является протеолитическая деградация. На основе популяционного фармакокинетического анализа у пациентов с солидными опухолями общий системный клиренс составил 0,59 л/сут, а период полувыведения составил 6,1 дня у пациентов, получавших 10 мг/кг.
Показания
Метастатическая карцинома из клеток Меркеля у взрослых и детей старше.
Распространённый или метастатический рак мочевого пузыря у пациентов которые:
- проявляют прогрессирование заболевания во время или после проведения платиносодержащей химиотерапии;
- прогрессирование заболевания в течение 12 месяцев после проведения неоадъювантного или адъювантного лечения платиносодержащей химиотерапией.
Противопоказания
- Повышенная чувствительность к авелумабу;
- беременность;
- лактация.
Беременность и грудное вскармливание
Применение противопоказано.
Способ применения и дозы
Рекомендуемая доза авелумаба составляет 10 мг/кг в виде внутривенной инфузии в течение 60 минут каждые 2 недели до прогрессирования заболевания или развития неприемлемой токсичности.
Побочные действия
Побочные реакции у ≥10 % пациентов, получающих авелумаб в исследовании JAVELIN Merkel 200 Trial (метастатическая карцинома из клеток Меркеля): утомляемость, инфузионные реакции, периферические отеки, скелетно-мышечная боль, артралгия, понос, тошнота, запор, боль в животе, рвота, сыпь и зуд кожи, снижение аппетита, снижение веса, кашель, одышка, головокружение, головная боль, повышенное артериальное давление.
Побочные реакции в ≥10 % пациентов с распространённым или метастатическим раком мочевого пузыря в исследовании JAVELIN Solid Tumor: тошнота, боль в животе, понос, запор, рвота, утомляемость, инфузионные реакции, периферические отеки, лихорадка, инфекции мочевыводящих путей, снижение веса, скелетно-мышечная боль, одышка, кашель, сыпь и зуд кожи, повышенное артериальное давление/гипертонический криз.
Взаимодействие
Клинически значимых взаимодействий с другими лекарственными средствами не описано.
Особые указания
Иммуно-опосредованный побочные реакции
Авелумаб может вызывать иммуно-опосредованные побочные реакции в том числе с летальным исходом. Среди них иммуно-опосредованный пневмонит, иммуно-опосредованный колит, иммуно-опосредованный гепатит, иммуно-опосредованные эндокринопатии и поражения почек.
Инфузионные реакции
Авелумаб может вызывать серьёзные и опасные для жизни реакции, связанные с инфузией. Премедикация с антигистаминными препаратами и парацетамолом необходима перед первыми 4 инфузиями. Необходим мониторинг пациентов с признаками инфузионных реакций, включая пирексию, озноб, покраснение, гипотонию, одышку, боли в спине, боли в животе и крапивницу.
Условия хранения
Хранить в холодильнике при температуре от 2 °C до 8 °C, в оригинальной упаковке для защиты от света. Не замораживать и не встряхивать.
Классификация
-
АТХ
L01XC31, L01FF04
-
Фармакологическая группа
-
Коды МКБ 10
Информация о действующем веществе Авелумаб предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Авелумаб, содержатся в инструкции производителя, прилагаемой к упаковке.
Исследование
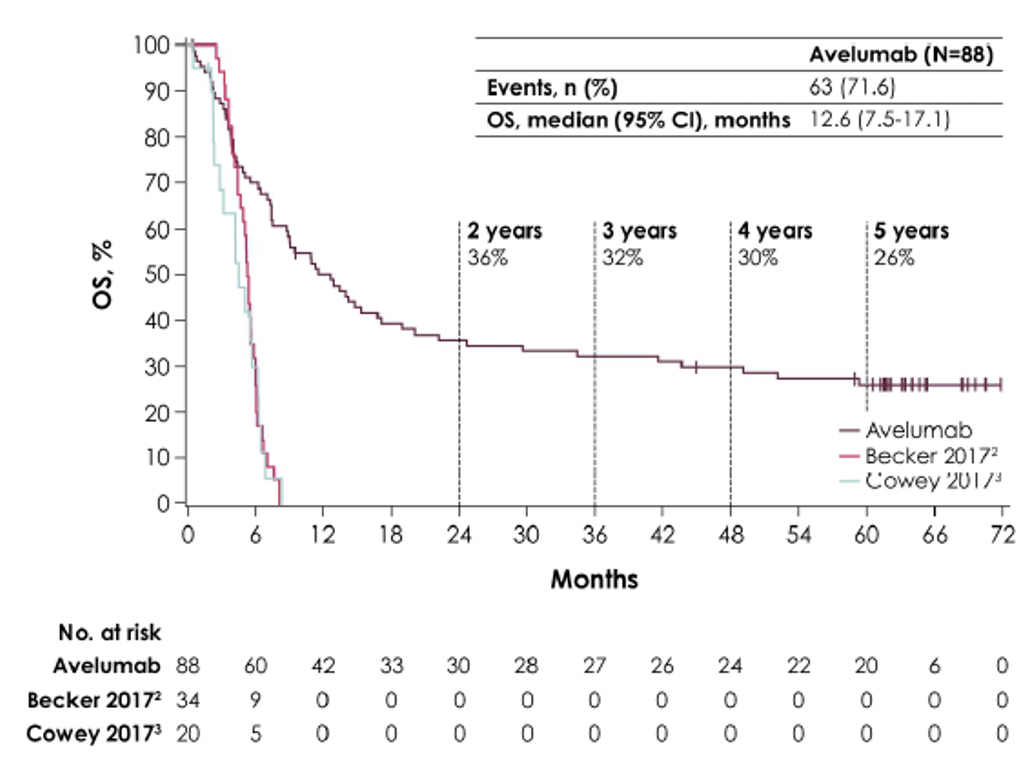
JAVELIN Merkel 200: обновленные данные общей выживаемости при периоде наблюдения > 5 лет
Авелумаб у пациентов, ранее получавших лекарственную терапию с метастатической и/или неоперабельной карциномой Меркеля: обновленные данные общей выживаемости при периоде наблюдения > 5 лет
Авторы: Paul Nghiem, Shailender Bhatia, Andrew S. Brohl, Omid Hamid, Janice M. Mehnert, Patrick Terheyden, Kent C. Shih, Isaac Brownell, Celeste Lebbe, Karl D. Lewis, Gerald P. Linette, Michele Milella, Huiling Xiong, Guelseren Guezel, Sandra P. D’Angelo
Ссылка на источник
Введение:
Карцинома Меркеля (КМ) — редкая и агрессивная форма рака кожи. Несмотря на то, что КМ считается химиочувствительной опухолью, эффективность химиотерапии ограничена. До одобрения ингибиторов иммунных контрольных точек пациенты с метастатической КМ (мКМ) имели плохой прогноз с историческим показателем 5-летней общей выживаемости (ОВ) примерно 14%. Авелумаб (анти-PD-L1) стал первым одобренным препаратом для лечения пациентов с мКМ, основываясь на данных эффективности и безопасности II фазы исследования JAVELIN Merkel 200 (NCT02155647), в котором пациенты с мКМ получали монотерапию авелумабом. Далее приводятся данные общей выживаемости при долгосрочном наблюдении для когорты пациентов с мКМ, заболевание которых прогрессировало после ≥1 линии предшествующей химиотерапии.
Методы:
Пациенты соответствовавшие критериям включения имели гистологически подтвержденный диагноз мКМ при наличии измеряемых очагов (согласно RECIST 1.1). Пациенты получали авелумаб в дозе 10 мг / кг внутривенно каждые 2 недели до подтверждения прогрессирования заболевания, неприемлемой токсичности или отмены. Была проанализирована долговременная ОВ. Обновленные данные для других конечных точек эффективности, включая ответ и выживаемость без прогрессирования, не были получены.
Результаты:
Всего в исследование было включено 88 пациентов, которые получали терапию авелумабом. По состоянию на 25 сентября 2020 г. (срез данных) медиана наблюдения составила 65,1 месяца (60,8-74,1 месяца). Медиана ОВ составила 12,6 месяцев (95% ДИ, 7,5-17,1 месяца); показатели 48-мес. и 60-мес. ОВ составили 30% (95% ДИ, 20-40%) и 26% (95% ДИ, 17%-36%), соответственно. На момент среза данных лечение продолжалось у 1 пациента (1,1%), а еще одному пациенту (1,1%) был повторно назначен авелумаб после прекращения лечения ранее. Причинами прекращения лечения были прогрессирование заболевания (n = 45 [51,1%]), нежелательное явление (НЯ; n = 11 [12,5%]), летальный исход (n = 10 [11,4%]), отзыв согласия (n = 9 [ 10,2%]), отказ от последующего наблюдения (n = 1 [1,1%]), несоблюдение протокола (n = 1 [1,1%]) и другие причины (n = 10 [11,4%]). На момент среза данных 19 пациентов (21,6%) прекратили лечение, но оставались на последующем наблюдении, а 63 пациента (71,6%) умерли; причинами смерти были прогрессирование заболевания (n = 49 [55,7%]), неизвестная причина (n = 9 [10,2%]), НЯ, не связанные с исследуемым лечением (n = 3 [3,4%]), и другие причины (n = 2 [2,3%]). Всего 26 пациентов (29,5%) получили последующую противоопухолевую терапию. Наиболее частыми видами терапии после прекращения исследования были авелумаб (n = 4 [4,5%]), карбоплатин и этопозид (n = 4 [4,5%]) и пембролизумаб (n = 4 [4,5%]).
Выводы:
Монотерапия авелумабом привела к значимому увеличению общей выживаемости в подгруппе пациентов с мКМ, заболевание которых прогрессировало после ≥1 линии предшествующей химиотерапии. Эти результаты дополнительно подтверждают роль авелумаба в качестве стандарта терапии пациентов с метастатической карциномой Меркеля. Информация о клиническом исследовании: NCT02155647 (https://clinicaltrials.gov/ct2/show/NCT02155647)
RU-AVEMCC-00011
Рис. 1. Общая выживаемость среди всех пациентов в исследовании по сравнению с историческими данными для химиотерапии.
Постер
Краткая инструкция БАВЕНСИО®
РУ: ЛП–005886
МНН: Авелумаб.
Лекарственная форма: концентрат для приготовления раствора для инфузий. Состав. 1 флакон содержит действующее вещество: авелумаб 200,0 мг, вспомогательные вещества: D–маннитол, ледяная уксусная кислота, полисорбат 20, натрия гидроксид, вода для инъекций.
Показания к применению: Монотерапия у взрослых ранее леченных пациентов с метастатической карциномой Меркеля (МКМ); В комбинации с акситинибом в качестве терапии первой линии при распространенном почечно-клеточном раке у взрослых; В качестве монотерапии для поддерживающей терапии первой линии взрослых пациентов с местнораспространенной или метастатической уротелиальной карциномой (УК), заболевание которых не прогрессировало при индукционной химиотерапии первой линии на основе платины.
Противопоказания. Гиперчувствительность к препарату БАВЕНСИО® или любому компоненту препарата в анамнезе; Детский возраст до 18 лет; Нарушение функции почек и печени тяжелой степени тяжести.
Способ применения и дозы. Терапия должна назначаться и контролироваться врачом, имеющим опыт лечения онкологических заболеваний.тРекомендуемая доза препарата БАВЕНСИО® при монотерапии составляет 800 мг внутривенно в течение 60 минут каждые 2 недели. Применение препарата БАВЕНСИО® следует продолжать в соответствии с рекомендуемой схемой до прогрессирования заболевания или возникновения неприемлемых токсических эффектов. Рекомендуемая доза в комбинации с препаратом акситиниб — 800 мг препарата БАВЕНСИО® внутривенно в течение 60 минут каждые 2 недели и 5 мг препарата акситиниб внутрь 2 раза в сутки (с интервалом между приемами 12 часов) вне зависимости от приема пищи, до прогрессирования заболевания или возникновения неприемлемых токсических эффектов. Для получения информации о способе применения и дозе акситиниба – смотри инструкцию по применению акситиниба. Премедикация. Перед первыми 4 инфузиями препарата БАВЕНСИО® пациенту следует провести премедикацию антигистаминными средствами и парацетамолом. Если четвертая инфузия завершается без развития инфузионных реакций, премедикация перед введением последующих доз назначается по усмотрению врача. Коррекция дозы. Повышение или снижение дозы препарата БАВЕНСИО® не рекомендуется. С учетом индивидуальной безопасности и переносимости возможна задержка введения очередной дозы препарата или прерывание лечения.
Побочное действие. НР у пациентов, получавших терапию препаратом БАВЕНСИО® в ходе клинических исследований. Cледующие побочные явления отмечались часто (≥1 % и <10 %) и очень часто (≥10 %): Нарушения со стороны крови и лимфатической системы — Очень часто анемия, часто лимфопения, тромбоцитопения, нечасто эозинофилия. Нарушения со стороны иммунной системы – нечасто Реакция гиперчувствительности, лекарственная реакция гиперчувствительности, редко анафилактическая реакция, реакция гиперчувствительности I типа. Нарушения со стороны эндокринной системы – часто гипотиреоз, гипертиреоз, нечасто надпочечниковая недостаточность, аутоиммунный гипотиреоз, тиреоидит, аутоиммунный тиреоидит, редко Острая недостаточность коры надпочечников*, недостаточность функции гипофиза. Нарушения со стороны обмена веществ и питания – очень часто снижение аппетита, часто гипонатриемия, нечасто гипергликемия,редко сахарный диабет, сахарный диабет 1 типа. Нарушения со стороны нервной системы – часто головная боль, головокружение, периферическая нейропатия, нечасто головная боль, головокружение, периферическая нейропатия, редко синдром Гийена-Барре, синдром Миллера-Фишера . Нарушения со стороны сердечно–сосудистой системы, часто гипертензия, нечасто гиперемия кожи, гипотензия, редко миокардит . Нарушения со стороны дыхательной системы, органов грудной клетки и средостения – очень часто кашель, одышка, часто пневмонит, редко интерстициальная болезнь лёгких . Нарушения со стороны желудочно–кишечного тракта – очень часто Тошнота, диарея, запор, рвота, боль в животе, часто колит, кишечная непроходимость, редко панкреатит, аутоиммунный колит, энтероколит, аутоиммунный панкреатит, энтерит, проктит. Нарушения со стороны печени и желчевыводящих путей – нечасто аутоимунный гепатит, редко острая печеночная недостаточность, печеночная недостаточность, гепатит, гепатотоксичность . Реакции со стороны кожи или подкожных тканей – часто сыпь, зуд, макулопапулезная сыпь, сухость кожи, нечасто экзема, дерматит, зудящая зудящая сыпь, псориаз, сыпь, эритематозная сыпь, эритема, генерализованная сыпь, пятнистая сыпь, папулезная сыпь, редко мультиформная эритема, гемморагическая сыпь, витилиго, генерализованный зуд, эксфолиативный дерматит, пемфигоид, псориазоподобный дерматит, медикаментозная сыпь, красный плоский лишай . Нарушения со стороны костно–мышечной и соединительной ткани – очень часто, боль в спине, артралгия, часто миалгия, нечасто миозит, ревматоидный артрит, редко артрит, полиартрит, олигоартрит. Нарушения со стороны почек и мочевыводящих путей – нечасто Ппочечная недостаточность, нефрит, редко тубулоинтерстициальный нефрит. Общие расстройства и нарушения в месте введения – очень часто утомляемость, повышение температуры тела, периферические отеки, часто Астения, озноб, гриппоподобное заболевание, редко Синдром системной воспалительной реакции. Влияние на результаты лабораторных и инструментальных исследований –очень часто снижение массы тела, повышение уровней АСТ, АЛТ, часто Повышение активности гамма-глутамилтрансферазы, щелочной фосфатазы, амилазы, липазы, концентрации креатинина крови, нечасто повышение активности аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), креатинфосфокиназы, редко повышение активности трансаминаз, снижение свободного тироксина, повышение тиреостимулирующего гормона в крови. Травмы, интоксикации и осложнения манипуляции –очень часто инфузионные реакции. Инфекции и инвазиинечасто пустулезная сыпь
Особые указания. Инфузионные реакции. У пациентов, получающих препарат БАВЕНСИО®, были зарегистрированы инфузионные реакции, часть из которых были тяжелыми. У пациентов следует контролировать появление симптомов и признаков инфузионных реакций, в том числе повышения температуры тела, озноба, покраснения кожи, снижения артериального давления, одышки, свистящего дыхания, боли в спине, боли в животе и сыпи. При развитии инфузионных реакций 3–ей и 4–ой степени тяжести следует прекратить инфузию и отменить препарат БАВЕНСИО®. Иммуноопосредованные реакции. Большинство иммуноопосредованных нежелательных реакций на фоне приема препарата БАВЕНСИО® были обратимыми и прекращались после кратковременного или длительного прерывания терапии препаратом БАВЕНСИО®, применения кортикостероидов и/или поддерживающей терапии.
Ознакомьтесь с полной информацией в инструкции по применению лекарственного препарата для медицинского применения Бавенсио®. Претензии потребителей и информацию о нежелательных явлениях следует направлять по адресу: ООО «Мерк», 115054, г. Москва, ул. Валовая, д. 35 , Тел.: +7(495) 937 33 04, Факс: +7(495) 937 33 05, e–mail: safety@merck.ru
(Variation № 3 29.07.2021 SmPC ver 20 June 2019. (CCDS 5.0)).
Новости онкологии
11.03.2019
Тимофеев Илья Валерьевич
Директор Бюро по изучению рака (Россия), член Международного комитета ASCO (США), член научного комитета Колледжа Европейской Школы Онкологии (ESCO)
Прошедший в Сан-Франциско симпозиум ASCO «Опухоли мочеполовой системы» (GU ASCO 2019) был насыщен исследованиями, результаты которых в ближайшее время изменят подходы к лечению метастатического почечно-клеточного рака (мПКР). Больше всего изменения затронут первую линию терапии светлоклеточного мПКР.
Пембролизумаб + Акситиниб
Одним из ожидаемых сообщений было представление результатов многоцентрового рандомизированного исследования 3 фазы KEYNOTE-426 [1]. В исследовании пациенты, не получавшие ранее терапию по поводу светлоклеточного мПКР, были рандомизированы в группу ингибитора контрольных точек пембролизумаба в комбинации с таргетным препаратом акситинибом (N=432), а также в группу сунитиниба, являющегося стандартом первой линии и выбранного в качестве препарата сравнения (N=429). Пембролизумаб назначался в стандартной дозе 200 мг, внутривенно, каждые 3 недели. Акситиниб также использовался в стандартной дозе 5 мг, 2 раза в день, перорально, ежедневно, с возможностью титрации дозы до 7 и 10 мг. Сунитиниб пациенты получали в режиме 4/2.
Группы были сопоставимы по основным клиническим характеристикам. Хотелось бы описать популяцию пациентов в группе комбинированного лечения. Медиана возраста в ней составила 62 года, при этом преобладающее большинство (60%) пациентов было младше 65 лет. На 71% группа была представлена мужчинами, на 83% – пациентами с нефрэктомией в анамнезе. Только 13% больных имели неблагоприятный прогноз согласно критериям IMDC. У 73% больных более двух органов было поражено метастазами: преимущественно легкие (73%), лимфатические узлы (46%) и кости (24%). У 51 из 285 пациентов с известной архитектоникой опухоли определялись признаки саркоматоидного мПКР. Экспрессия PD-L1 не являлась критерием включения и не влияла на статистическую гипотезу. CPS (combined positive score) ≥1 (то есть наличие экспрессии PD-L1) отмечался у 59,3% больных в группе комбинации и у 61,7% – в группе сунитиниба.
Первичными конечными точками в исследовании были общая выживаемость (ОВ) и выживаемость без прогрессирования (ВБП). Дополнительные критерии включали частоту объективных ответов, длительность ответа и безопасность. Оценка проводилась независимым комитетом.
При медиане наблюдения 12,8 мес. медиана ОВ не была достигнута. Риск смерти в группе пембролизумаба-акситиниба был ниже на 47% по сравнению с сунитинибом (HR=0,53). Различия оказались достоверными (P<0,0001, рисунок 1).
Рисунок 1. Кривые ОВ в исследовании KEYNOTE-426 (Rini et al. NEJM 2019 [2]).
Однолетняя ОВ составила 89,9% и 78,3% в этих группах, а 18-месячная ОВ – 82,3% и 72,1%, соответственно. Медиана ВБП была 15,1 мес. в группе комбинации и 11,1 мес. в группе сунитиниба (HR=0,69; P<0,001). Преимущества пембролизумаба-акситиниба наблюдались во всех подгруппах вне зависимости от прогноза пациента и статуса PD-L1. Следовательно, обе первичные конечные точки были достигнуты, исследование оказалось позитивным.
Частота ответов на лечение также выгодно отличалась в пользу комбинации (59,3% по сравнению с 35,7% для сунитиниба). 5,8% и 1,9% больных имели полные ответы, получая комбинацию и сунитиниб. Медиана длительности ответа не была достигнута в группе пембролизумаба-акситиниба и составила 15,2 мес. в контрольной группе.
По частоте развития нежелательных явлений группы не отличались. Практически у всех пациентов были зарегистрированы побочные эффекты (более 98%). Использование комбинации пембролизумаба и акситиниба сопровождалось развитием токсичности 3-4 степени у 75,8% больных, а назначение сунитиниба – у 70,6%. Наиболее частыми вариантами нежелательных явлений в группе комбинации были диарея, гипертензия, утомляемость, гипотиреоз, снижение аппетита и ладонно-подошвенный синдром. Токсичность привела к прекращению терапии одним из препаратов комбинации у 30,5% пациентов, обоими препаратами – у 10,7%. Кроме того, у 69,9% больных требовался перерыв в лечении и у 20,3% – снижение дозы.
Делая выводы, можно с уверенностью отметить высокую эффективность комбинации пембролизумаба и акситиниба у пациентов со светлоклеточным мПКР, ранее не получавших терапию. Более того, эта комбинация – прямое доказательство целесообразности сочетания ингибитора контрольных точек и таргетного препарата. Хочется напомнить, что в монотерапии пембролизумаб демонстрировал более скромные показатели. В исследовании 2 фазы KEYNOTE-427 с включением 110 пациентов частота объективных ответов составляла 38,2%, медиана ВБП – 8,7 мес. [3]. Добавление акситиниба к пембролизумабу привело к увеличению числа пациентов с ответом более чем на 20% и удлинению ВБП на 70% по сравнению с монотерапией пембролизумабом. За возросшую эффективность комбинация рассчиталась увеличенной токсичностью. Частота серьезных нежелательных явлений увеличилась в 3 раза (при монотерапии пембролизумабом была 22,7%). Однако частота отмены лечения из-за побочных эффектов уложилась в известный для терапии мПКР диапазон – 11-30%, что свидетельствует о возможности управления нежелательными явлениями комбинации.
Авелумаб + Акситиниб
Результаты исследования 3 фазы эффективности комбинации другого ингибитора контрольных точек – авелумаба и акситиниба были представлены еще на ESMO 2018 [4]. В исследовании JAVELIN Renal 101 пациенты со светлоклеточным мПКР были рандомизированы в группу авелумаба-акситиниба (N=442) или в группу сунитиниба (N=444) [5]. Главным отличием этого исследования от предыдущего было построение статистической гипотезы по оценке ВБП и ОВ в когорте пациентов, экспрессирующих PD-L1. 560 из 886 (63,2%) больных имели экспрессию PD-L1, оцениваемую как окрашивание ≥1% иммунных клеток в опухолевом образце с использованием иммуногистохимического теста SP263 (Ventana). Считается, что экспрессия PD-L1 у больных мПКР сопряжена с худшим прогнозом и снижением эффективности таргетной терапии.
На GU ASCO 2019 были представлены новые результаты эффективности комбинации в различных подгруппах. Прежде всего хочется отметить, что первичная конечная точка – ВБП – была достигнута: медиана ВБП составила 13,8 мес. в экспериментальной группе и 7,2 мес. – в контрольной (P<0,001, рисунок 2).
Рисунок 2. Кривые ВБП в группах пациентов с PD-L1 экспрессией
в исследовании JAVELIN Renal 101 (Motzer et al. NEJM 2019 [6]).
Что вызвало интерес, так это сохранившиеся различия по данному параметру и в общей когорте пациентов (как с экспрессией PD-L1, так и без): 13,8 мес. и 8,4 мес. для авелумаба-акситиниба и сунитиниба соответственно (P<0,001). Медиана ОВ – вторая главная конечная точка – в настоящее время в группах не достигнута и наблюдение продолжается.
Частота объективных ответов у пациентов с экспрессией PD-L1 была в 2 раза лучше в группе комбинированного лечения – 55,2% по сравнению с 25,5% для сунитиниба. Существенные различия также отмечались и в общей когорте – 51,4% и 25,7%. Полные ответы были зарегистрированы у 4,4% больных, получавших авелумаб-акситиниб, и у 2,1% получавших сунитиниб. Все объективные ответы оказались длительными, медиана не была достигнута.
Важнейшим моментом стала оценка эффективности комбинации в зависимости от прогноза по критериям IMDC и MSKCC. Комбинация двух препаратов сохранила свое превосходство над сунитинибом во всех прогностических группах. Однако ради справедливости нужно отметить, что пациентов с плохим прогнозом было не так много – 10-16%, что позволяет лишь сделать предварительный вывод об эффективности в этой когорте.
Если посмотреть на профиль токсичности комбинации, то снова нежелательные явления всех степеней были отмечены у 99,5% больных, а частота нежелательных явлений 3 степени и выше составила 71,2%. Профиль токсичности очень похож на профиль комбинации пембролизумаба-акситиниба. В группе авелумаба-акситиниба также наиболее часто встречались диарея, гипертензия, утомляемость, тошнота, ладонно-подошвенный синдром. У 7,6% больных пришлось отменить оба препарата из-за токсичности. Однако 10,8% пациентов имели даже эскалацию дозы акситиниба.
Таким образом, комбинация авелумаба и акситиниба показала значительные преимущества по сравнению с сунитинибом в когортах не получавших ранее терапию пациентов со светлоклеточным мПКР, как экспрессирующих PD-L1, так и вне зависимости от экспрессии PD-L1. Приведенные факты равной эффективности комбинации в группах с и без PD-L1 экспрессии являются интересными, но вряд ли стоит экстраполировать их на генеральную совокупность – ведь исследование было статистически спланировано доказать различия по основным точкам только в когорте экспрессирующих больных, а, следовательно, с позиций доказательной медицины мы не имеем достаточных оснований использовать препараты у всех пациентов, без знания уровня экспрессии. С другой стороны, стало совершенно очевидно, что назначение таргетных препаратов в монотерапии у пациентов с экспрессией PD-L1 не приводит к позитивному эффекту. Вот уже не в первый раз в этой когорте больных сунитиниб показывает медиану ВБП 7 мес. Те же цифры демонстрировались в исследовании IMMOTION 151 [7].
Ниволумаб + Ипилимумаб
Наконец, результаты 30-месячного наблюдения в исследовании CheckMate 214, в котором изучалась эффективность комбинации ниволумаба и ипилимумаба у пациентов с мПКР и промежуточным/плохим прогнозом, ранее не получавших терапию, были представлены на симпозиуме [8]. Комбинация продемонстрировала достоверные преимущества по общей выживаемости и частоте ответов по сравнению с сунитинибом, о чем писали ранее [9]. В настоящий момент комбинация ниволумаба и ипилимумаба наиболее близка к практическому использованию в России, так как была официально зарегистрирована для применения. Эта лечебная опция уже добавлена в практические рекомендации NCCN [10] и новую версию рекомендаций ESMO [11] как стандарт с наивысшим уровнем доказательности 1.
Отдаленные результаты эффективности и токсичности представляют большой интерес, отражая длительное воздействие на исходы. Медиана продолжительности жизни в группе комбинации так и не была достигнута – более 50% больных живы. В группе сунитиниба этот показатель составил 26,6 мес. Различия оказались существенными (HR=0,63; P<0,0001). 2-летняя ОВ составила 66% и 53% соответственно. Частота объективных ответов была как в абсолютных цифрах (42% по сравнению с 29%), так и статистически (P=0,0001) лучше при терапии ниволумабом и ипилимумабом. Представить раньше, что 11% таких прогностически тяжелых пациентов будут иметь полные ответы, то есть когда все метастазы исчезают, было сложно. Теперь это реальность.
В течение 30 месяцев число нежелательных явлений в группе комбинации существенно не изменилось. Так, 5 дополнительных пациентов, получавших комбинацию, и 7 пациентов, получавших сунитиниб, имели нежелательные явления 3-4 степени, при этом только у 1 и 3 пациентов из этих групп терапия была прервана из-за токсичности.
Значительным прорывом можно считать появление новой опции терапии пациентов с промежуточным и плохим прогнозом. Для последней группы лишь темсиролимус имел наивысшую категорию доказательности, обеспечивая медиану ОВ в 10,9 мес. [12]. Комбинация ниволумаба и ипилимумаба снижает риск смерти на 37% по сравнению с сунитинибом. Долгосрочное наблюдение за больными, получавшими комбинацию двух ингибиторов контрольных точек, подтверждает ее эффективность. Использование ипилимумаба в низкой дозе (1 мг/кг) привело к умеренной токсичности комбинации без потери эффективности. Качество жизни пациентов, получающих комбинацию, было также значимо лучшим; симптомы болезни регистрировались реже у этих пациентов [13].
Сравнение эффективности комбинаций.
Возможный алгоритм назначения препаратов в будущем
Итак, 3 новые комбинации входят в первую линию терапии светлоклеточного мПКР. Возникает вопрос, можно ли сравнивать эффективность этих комбинаций? Сопоставить цифры достаточно просто, но, с моей точки зрения, делать это не совсем правильно. Комбинация пембролизумаба/акситиниба изучалась в общей когорте больных вне зависимости от статуса экспрессии PD-L1. Комбинация авелумаба/акситиниба изучалась у пациентов с экспрессией PD-L1, что изменяет течение болезни. Обе комбинации достаточно хорошо изучены в группах благоприятного и промежуточного прогноза и недостаточно – в группе плохого прогноза (только 13% и 12% больных с плохим прогнозом включены в соответствующие исследования). Комбинация ниволумаба/ипилимумаба, наоборот, изучалась у пациентов с промежуточным и плохим прогнозом, но без оглядки на экспрессию PD-L1 как определяющий фактор.
Таким образом, картина складывается удачно: появление трех комбинаций позволит персонализировать терапию. Предположу следующий алгоритм (рисунок 3). На первом этапе всем пациентам со светлоклеточным раком определяется экспрессия PD-L1. В случае экспрессии пациентам назначается комбинация авелумаба и акситиниба. У пациентов с отсутствием экспрессии оценивается прогноз. При благоприятном прогнозе показанием будет комбинация пембролизумаба и акситиниба, при плохом – ниволумаба и ипилимумаба. При промежуточном прогнозе обе комбинации могут быть назначены пациенту. Таргетные препараты в монорежимах переместятся из первой линии в последующие.
Рисунок 3. Возможный алгоритм назначения препаратов в первой линии терапии мПКР.
Литература:
- Powles, et al. Pembrolizumab (pembro) plus axitinib (axi) versus sunitinib as first-line therapy for locally advanced or metastatic renal cell carcinoma (mRCC): phase III KEYNOTE-426 study. J Clin Oncol 37, 2019 (suppl.7S; abstr.543).
- Rini, et al. Pembrolizumab plus Axitinib versus Sunitinib for Advanced Renal-Cell Carcinoma. N Engl J Med. 2019 Feb 16. doi: 10.1056/NEJMoa1816714. [Epub ahead of print].
- McDermott, et al. Pembrolizumab monotherapy as first-line therapy in advanced clear cell renal cell carcinoma (accRCC): Results from cohort A of KEYNOTE-427. J Clin Oncol 36, 2018 (suppl; abstr.4500).
- Motzer, et al. JAVELIN Renal 101: A randomized, phase III study of avelumab + axitinib vs sunitinib as first-line treatment of advanced renal cell carcinoma (aRCC). Abstract LBA6_PR. Annals of Oncology, Volume 29, Supplement 8.
- Choueiri, et al. Subgroup analysis from JAVELIN Renal 101: Outcomes for avelumab plus axitinib (A + Ax) versus sunitinib (S) in advanced renal cell carcinoma (aRCC). J Clin Oncol 37, 2019 (suppl.7S; abstr.544).
- Motzer, et al. Avelumab plus Axitinib versus Sunitinib for Advanced Renal-Cell Carcinoma. N Engl J Med. 2019 Feb 16. doi: 10.1056/NEJMoa1816047. [Epub ahead of print].
- Motzer, et al. IMmotion151: A Randomized Phase III Study of Atezolizumab Plus Bevacizumab vs Sunitinib in Untreated Metastatic Renal Cell Carcinoma (mRCC). Journal of Clinical Oncology 36, no.6_suppl (February 20, 2018), p.578-578.
- Tannir, et al. Thirty-month follow-up of the phase III CheckMate 214 trial of first-line nivolumab + ipilimumab (N+I) or sunitinib (S) in patients (pts) with advanced renal cell carcinoma (aRCC). J Clin Oncol 37, 2019 (suppl.7S; abstr.547).
- Motzer, et al. Nivolumab plus Ipilimumab versus Sunitinib in Advanced Renal-Cell Carcinoma. N Engl J Med. 2018 Apr 5; 378(14): 1277-1290.
- NCCN Clinical Practice Guidelines in Oncology: Kidney Cancer, version 3.2019.
- Escudier, et al. Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2019 Feb 21. pii: mdz056. doi: 10.1093/annonc/mdz056. [Epub ahead of print].
- Hudes, et al. Temsirolimus, Interferon Alfa, or Both for Advanced Renal-Cell Carcinoma. N Engl J Med 2007; 356: 2271-81.
- Cella, et al. Patient-reported outcomes of patients with advanced renal cell carcinoma treated with nivolumab plus ipilimumab versus sunitinib (CheckMate 214): a randomised, phase 3 trial. Lancet Oncol. 2019 Feb; 20(2): 297-310.

Иммунотерапия препаратом Ниволумаб
Обновлено: 28 апреля 2022
27478
Как действует ниволумаб при раке? О клиническом применении препарата Опдиво, его преимуществах и побочных эффектах рассказывает онколог-химиотерапевт высшей категории Круглова Марина Сергеевна
- arrow_forward
Как действует Ниволумаб? - arrow_forward
Преимущества терапии ниволумабом - arrow_forward
Побочные эффекты ниволумаба
Ниволумаб — противоопухолевый препарат из группы ингибиторов контрольных точек и фактический стимулятор иммунитета. Опдиво — это торговое название, присвоенное компанией-производителем моноклональному человеческому антителу ниволумаб. Антитело представляет собой чистейший и абсолютно однородный по свойствам белок.
Как действует Ниволумаб?
Принцип действия Ниволумаба на опухоль диаметрально отличается от всех прочих иммунологических противоопухолевых препаратов. Доставшиеся нам из прошлого века и до настоящего времени используемые в онкологии цитокины — интерферон-альфа и интерлейкин-2 — синтезированные человеком продукты жизнедеятельности лимфоцитов, доставляемые в организм уже в готовом виде.
Ниволумаб также радикально отличается от механизма действия цитостатиков, суть которых уничтожить опухолевую клетку (цитотоксический эффект) или остановить ее пролиферативную активность (цитостатический эффект).
В конечном итоге Опдиво вынуждает лимфоциты вырабатывать цитокины, но не прямым способом, а помогая лимфоциту выйти из оцепенения, в которое его ввергает злокачественный процесс.
Ниволумаб блокирует взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами (PD-L1 и PD-L2).
PD-1-рецептор является негативным регулятором активности Т-клеток. Связывание PD-1 с лигандами PD-L1 и PD-L2, которые способны экспрессироваться клетками опухолей или иными клетками микроокружения опухолей, приводит к ингибированию пролиферации Т-клеток и секреции цитокинов. Ниволумаб потенцирует иммунный ответ посредством блокады связывания PD-1 с лигандами PD-L1 и PD-L2.
Выражаясь простыми словами, взаимодействие ниволумаба с лимфоцитом осуществляет через специальный рецептор на поверхностной мембране. Занятый им рецептор не может связаться с продуцируемыми опухолевыми клетками и их окружением — лигандами.
Лиганды специально синтезируются для обмана лимфоцита, чтобы он не замечал развитие злокачественного процесса. Связывание лигандов со специальным рецептором PD-1 на поверхности лимфоцита приводит к нарушению его работы и воспроизводства. В результате получается, что опухолевые клетки не замечаются «больным» лимфоцитом и могут спокойно воспроизводить себе подобных.
С помощью ниволумаба лимфоцит «прозревает» и вырабатывает смертельные для раковой клетки цитокины. Если интерферон и интерлейкин вводятся в огромных дозах, то активированный опдиво лимфоцит вырабатывает их без превышения своих функциональных возможностей.
О существовании рецептора можно узнать по присутствию специфического белка PD-1, который имеется у 10–15% больных.
Применение Ниволумаба
Ниволумаб при раке доказал свою эффективность в многочисленных клинических исследованиях по всему миру и сегодня зарегистрирован в России для лечения девяти нозологий:
- 1-я линия терапии почечно-клеточного рака;
- 2-я линия терапии почечно-клеточного рака;
- Метастатическая меланома;
- Адъювантная терапия меланомы;
- Опухоли головы и шеи;
- Мелкоклеточный рак легкого;
- Немелкоклеточный рак легкого;
- Рак желудка или пищеводно-желудочного перехода;
- Рак мочевого пузыря;
- Гепатоцеллюлярный рак;
- Колоректальный рак;
- Лимфома Ходжкина.
Преимущества терапии ниволумабом
Преимущество иммунотерапии состоит в том, что при показаниях, ее можно использовать у ослабленных, возрастных пациентов, с выраженной сопутствующей патологией ввиду меньшей токсичности и более легкой переносимостью.
То есть иммунотерапия дает новые возможности пациентам, которым химиотерапия противопоказана по состоянию здоровья.
Еще одним достоинством иммунотерапии является длительность ответа на лечение. Если по результатам контрольных обследований на иммунотерапии возникает регресс опухоли, то зачастую этот ответ может быть очень длительным.
Как проводится лечение Ниволумабом?
Препарат вводится в виде внутривенной инфузии в течение 30 или 60 минут согласно инструкции. Терапия ниволумабом должна продолжаться до прогрессирования или развития непереносимой токсичности.

Возможность назначать препарат одним из трех одобренных способов введения позволяет врачу подобрать оптимальный режим для каждого конкретного пациента:
- 3 мг/кг каждые 2 недели в течение 60 или 30 минут;
- 240 мг каждые 2 недели в течение 60 или 30 минут;
- 480 мг каждые 4 недели в течение 60 или 30 минут.
Отличие иммунотерапии от химиотерапии заключается в отсутствии специальной пре- и постмедикации. Пациент не нуждается в антиэметогенной терапии, глюкокортикостероидах, антигистаминных, гастропротективных препаратах. Не требуется принимать их для профилактики и между курсами иммунотерапии.
Побочные эффекты ниволумаба
Вторая сторона медали современной иммунотерапии – это побочные эффекты, осложнения, а также иммуноопосредованные нежелательные явления.
Токсичность на фоне иммунотерапии имеет другой профиль, нежели стандартная химиотерапия. Побочные действия ниволумаба связаны с аутоиммунными реакциями на фоне «гиперактивного» иммунитета. Они обусловлены избыточной активацией иммунной системы с аутоиммунным поражением нормальных тканей различных органов и систем.
Осложнения на терапии ниволумабом могут появиться уже в течение 1 недели или только через 54 недели от начала терапии, симптомы могут усиливаться в любой момент времени и приводить к фатальным последствиям.
Наиболее частыми побочными эффектами ниволумаба по результатам клинических исследований являются утомляемость (34%), сыпь (19%), зуд (14%), диарея (13%), тошнота (13%) и снижение аппетита (10%), а также – повышение температуры или озноб с лихорадочным состоянием. В большинстве случаев побочные реакции выражаются от легкой до средней степени тяжести.
Все побочные реакции, включая тяжелые, купируются или при помощи симптоматической терапии, или путем отмены иммунотерапии.
Что делать, если на лечении ниволумабом развились нежелательные явления?
Для того, чтобы устранить побочные эффекты иммунотерапии, необходимо не только знать весь анамнез и сопутствующие заболевания конкретного пациента, но и понимать природу и механизм иммуноопосредованной токсичности.
Крайне важно, чтобы лечение ниволумабом осуществлял онколог, который не только имеет опыт проведения иммунотерапии, но и умеет распознавать ее нежелательные явления на ранней стадии. Своевременное выявление осложнений позволит не только их купировать, но и не прерывать противоопухолевое лечение.
Например, когда мы проводим иммунотерапию в клинике, мы осуществляем тщательный мониторинг показателей систем организма, строго по графикам. Также мы информируем и обучаем пациентов, как оперативно выявить и вовремя среагировать на нежелательные явления, так как своевременная диагностика и надлежащая медикаментозная терапия может улучшить результаты и при этом не окажет негативного влияния на активность иммунного препарата.
Мы накопили большой клинический опыт применения ниволумаба и разработали собственные восстановительные программы и этапы действий для успешного устранения побочных эффектов иммунотерапии. Наш подход – сделать лечение не только эффективным, но и максимально комфортным для вас.
Запишитесь на прием к онкологу по телефону +7 (812) 952-83-73, и мы примем вас в день обращения.
Отзывы
Леонова О.П.
21 августа 2020
Хочу выразить благодарность сотрудникам клиники De Vita и особенно врачу-химиотерапевту Кругловой Марине Сергеевне за квалифицированную помощь, человечное отношение, высокий профессионализм. В тяжелые моменты онкологического лечения необходимы грамотные и своевременные консультации, психологическая помощь и поддержка. Все это было сделано в вашей клинике.
Спасибо вам за ваш опыт, профессионализм, грамотность и человеческое отношение. С уважением,
…
Читать полностью
семья Ивановых
20 августа 2020
Благодаря грамотному лечению, профессионализму и внимательному отношению врача с большой буквы Ирины Александровны, я вернулась к жизни! Спасибо Вам большое, что в самое сложное время для нашей семьи Вы были с нами! Отдельное спасибо хирургу Сергею Александровичу и всему медицинскому персоналу! С уважением, семья Ивановых. Желаем здоровья, долголетия и многомонетия!
…
Читать полностью
Замулина И.В.
7 августа 2020
Благодарю за чуткость, профессионализм, доброе отношение в клинике Де Вита. Очень серьезное лечение прошла легко и без побочных эффектов. Отдельное спасибо за профессионализм Анне Игоревне Буйняковой! С благодарностью,
…
Читать полностью
Вот и закончился мой 12-недельный курс химиотерапии в клинике De Vita.
Все это время сотрудники клиники помогали мне пройти лечение без осложнений и максимально комфортно .
Хочу поблагодарить:
— руководство за безупречную организацию работы и замечательно подобранных сотрудников;
— моего лечащего врача Круглову Марину Сергеевну за профессионализм, внимание и доброе отношение благодаря которому я поверила в лечение и смогла его выдержать;
— замечательных медсестер за золотые руки и сердечность, особенно Анастасию;
— улыбчивых и внимательных менеджеров, которые встречали и провожали меня каждый раз.
Желаю всем работникам крепкого здоровья, хорошего настроения и терпения в нелегком труде.
…
Читать полностью
Елена Викторовна
17 июля 2020
Хочу сказать большое спасибо всем сотрудникам клиники De VIta, это замечательные, внимательные, знающие свое дело люди. Отдельное спасибо моему лечащему врачу Буйняковой А.И. за ее помощь, поддержку и внимание. Доктора знаю уже больше 10 лет и очень ей благодарна за маму, которую она подняла на ноги. Судьба меня свела опять с Анной Игоревной, я очень рада, что эта замечательная женщина, мой лечащий врач. Она не просто профессионал своего дела, а красивая, чуткая женщина. И я от всего сердца хочу поблагодарить ее за все усилия и помощь в лечении. Так же огромное спасибо девочкам мед.сестрам и администраторам за четкую, слаженную работу. Всем сотрудникам клиники желаю успехов, процветания и конечно здоровья.
…
Читать полностью
Григорьева Л.Е.
26 июня 2020
Сегодня 26 июня 2020 года — моя последняя капельница!!! Позади долгий непростой путь длиной в 6 месяцев. И все это время я чувствовала огромную поддержку и внимание своего доктора Буйняковой Анны Игоревны.
Уважаемая, дорогая Анна Игоревна! Огромное Вам спасибо и низкий поклон за Вашу отзывчивость, Ваш профессионализм, чуткость, внимательность, ответственность, за позитивный настрой! Хочется поблагодарить медсестру Людмилу за ее «волшебные руки», внимательность, ответственное отношение к больным. Спасибо девушкам администраторам Яне и Марии, Вале за доброжелательность и внимание, четкую слаженную работу, а также психологу А.А. Ястребовой за моральную поддержку. Желаю всем сотрудникам ДеВита успехов, процветания, здоровья!
…
Читать полностью
семья Чаусовых
21 июня 2020
Наша семья выражает благодарность Уваровой Светлане Николаевне, Кругловой Марине Сергеевне и всему персоналу онкологического центра за отзывчивость, доброжелательность, высокий профессионализм. Поздравляем Вас с Днем Медицинского работника! Пусть всё сделанное Вами добро возвращается к Вам многократно в виде здоровья и долголетия!!
…
Читать полностью
Спасибо всей команде De Vita за работу и отношение. Особенно благодарю Андрея Сергеевича за профессионализм и поддержку! Спокойствие и уверенность врача передаётся пациенту, мне это очень помогло. В такой трудной ситуации сходишь с ума, здесь я получила помощь! А также все ответы на свои вопросы, заботу, хорошее лечение и только позитивный заряд. Спасибо!
…
Читать полностью
Поздравляю клинику с днём рождения и хочу сердечно поблагодарить химиотерапевта Анну Игоревну Буйнякову за высокий профессионализм, за помощь и поддержку в непростой «химический» период. Ни один вопрос не остался без ответа, Анна Игоревна практически провела меня за руку через всю химию. Спасибо Вам огромное за это!
Также благодарю и хочу отметить медсестру Людмилу, ее отличную работу и душевность. Очень хорошее и приятное впечатление от всех, с кем пришлось разговаривать и встречаться в клинике. Хорошие и комфортные условия для лечения такого коварного заболевания. Вы даёте уверенность в победе! Низкий поклон вам!
Татьяна, Великий Новгород.
…
Читать полностью
Юдина Наталия Андреевна
15 мая 2020
Всех сотрудников De Vita хочу поблагодарить за внимательное и чуткое отношение к запросам и потребностям клиентов. Отдельная огромная-преогромная благодарность лечащему врачу Буйняковой Анне Игоревне за профессионализм, отзывчивость, внимательность, за веру в возможности пациента, за готовность прийти на помощь а любое время суток. Здоровья Вам, успехов, всех благ.! Спасибо Вам большое.
С уважением,
…
Читать полностью